Clear Sky Science · es
Reprogramar el destino de las células de melanoma: moduladores de TRPM8 inducen apoptosis y potencian la citotoxicidad de las células NK
Por qué convertir un “sensor de frío” contra el cáncer de piel importa
El melanoma es una forma peligrosa de cáncer de piel que con frecuencia aprende a eludir tanto los fármacos como al sistema inmune. Este estudio explora una vulnerabilidad inesperada en las células de melanoma: una proteína llamada TRPM8, conocida principalmente como el sensor que permite a las neuronas percibir el frío o el mentol. Los investigadores muestran que fármacos diseñados para bloquear TRPM8 pueden empujar a las células de melanoma a autodestruirse y, al mismo tiempo, hacerlas más susceptibles al ataque de las células asesinas naturales (NK). Esta acción dual sugiere una nueva vía para tratar melanomas avanzados y resistentes.
Un interruptor oculto en las células de melanoma
Mediante el análisis de grandes bases de datos de cáncer y el examen de células de melanoma derivadas de pacientes en el laboratorio, el equipo encontró que TRPM8 es mucho más abundante en el melanoma metastásico que en la piel normal, incluidas las melanocitos sanos y los fibroblastos dérmicos. Con técnicas de imagen demostraron que TRPM8 se localiza tanto en la superficie celular como en membranas internas, colocándolo en puntos estratégicos para influir en el comportamiento celular. Al aplicar una batería de nuevas moléculas dirigidas a TRPM8, dos compuestos (denominados 4 y 9) destacaron de manera consistente: reducían drásticamente la supervivencia de las células de melanoma con el tiempo mientras dejaban en gran medida indemnes a las células de piel normales. Pruebas genéticas confirmaron que cuando TRPM8 se eliminaba, estos fármacos perdían su poder letal, y cuando TRPM8 se incrementaba, las células de melanoma se volvían aún más sensibles, demostrando que el efecto depende de este canal específico. 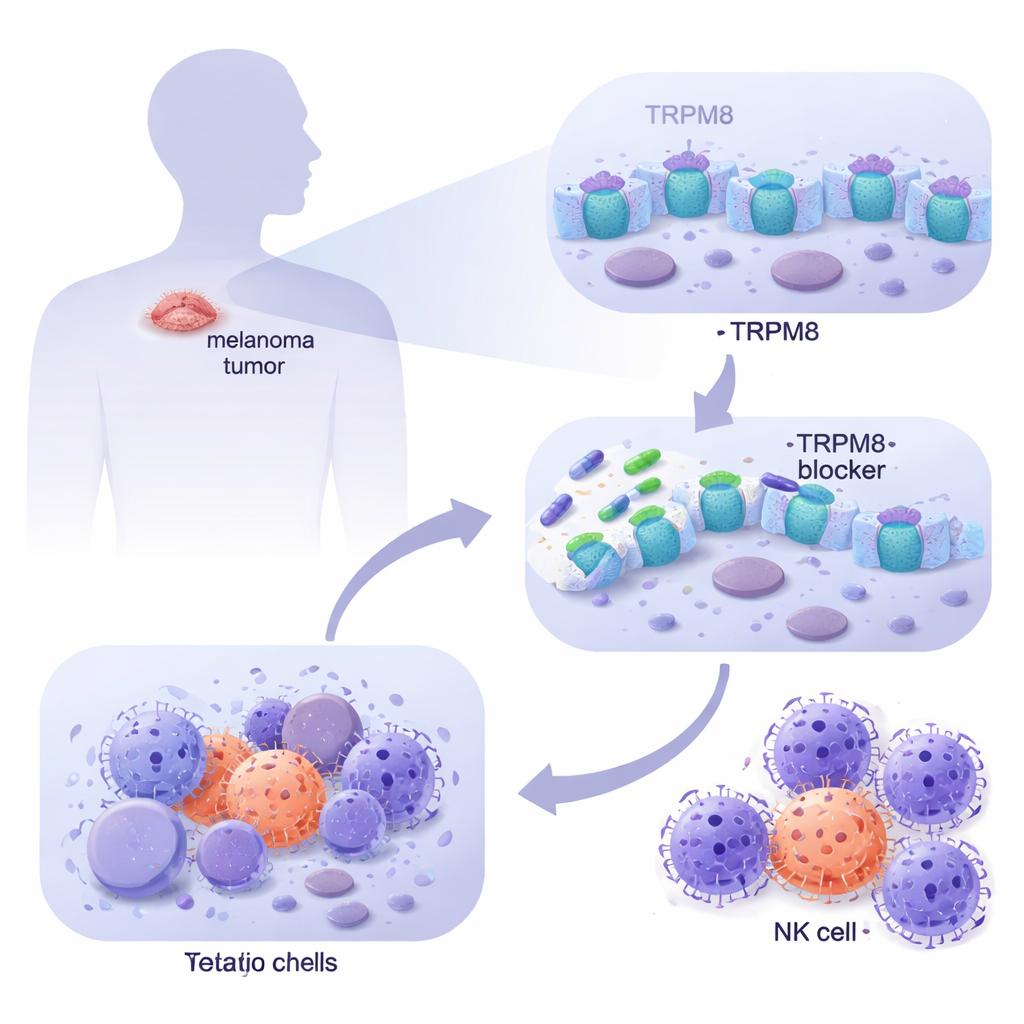
Forzar a las células cancerosas a una crisis energética
A diferencia de los activadores clásicos de TRPM8 como el mentol, que provocan una oleada de calcio en las células, estos nuevos bloqueadores no desencadenaron cambios en el calcio. En cambio, dispararon una ola de estrés oxidativo dentro de las células de melanoma. Los compuestos aumentaron rápidamente las especies reactivas de oxígeno, en especial dentro de las mitocondrias, las centrales energéticas de la célula. Este estallido oxidativo hizo que las mitocondrias perdieran su carga eléctrica, se fragmentaran y filtraran citocromo c, un paso clave para activar el programa interno de “suicidio” celular. Antioxidantes que eliminaban estas moléculas reactivas rescataron en gran medida a las células, mostrando que el desequilibrio redox no es un efecto secundario sino el motor de la muerte celular. A continuación, marcadores clásicos de muerte como la activación de caspasa‑3 y la escisión de PARP confirmaron que las células estaban sufriendo apoptosis programada en lugar de un daño aleatorio.
Desarmando señales de supervivencia y despertando a un guardián
El impacto oxidativo desencadenó una respuesta de estrés más amplia. Los fármacos activaron ATM, un sensor de daño en el ADN, y llevaron a la acumulación y activación de p53, la conocida proteína supresora tumoral que decide si una célula dañada debe repararse o morir. Al mismo tiempo, los compuestos debilitaron una de las principales rutas de supervivencia del melanoma: la vía PI3K–AKT. Normalmente, TRPM8 interactúa físicamente con componentes de PI3K para ayudar a mantener a AKT en su forma activa, promotora del crecimiento. Tras el tratamiento, esta asociación se rompió y la actividad de AKT cayó, inclinando aún más la balanza hacia la muerte celular. Es importante que estos cambios fueron pronunciados en células de melanoma pero no en células no cancerosas, lo que sugiere una ventana terapéutica en la que el tumor es golpeado con fuerza mientras el tejido sano se preserva.
Haciendo que los tumores sean más visibles para los “escuadrones” inmunitarios
El peligro del melanoma también radica en su talento para escapar de la vigilancia inmune. Los investigadores se preguntaron qué ocurría con las células tumorales que sobrevivían a dosis bajas de los bloqueadores de TRPM8 durante periodos más largos. Descubrieron que estas células persistentes empezaron a mostrar mayor cantidad de un marcador de superficie llamado ULBP1, que actúa como una señal de socorro reconocida por receptores NKG2D en las células NK. Otros marcadores relacionados no cambiaron, lo que indica un efecto selectivo. En esferoides de melanoma tridimensionales que imitan mejor los tumores reales, el pretratamiento con bloqueadores de TRPM8 no solo redujo el tamaño de las estructuras y aumentó la muerte celular, sino que también las hizo mucho más vulnerables al ataque de células NK. Cuando ULBP1 o NKG2D se bloquearon con anticuerpos, esta eliminación adicional desapareció en gran medida, mostrando que la mejora en la limpieza inmune pasa por este apretón de manos específico entre tumor y células NK. 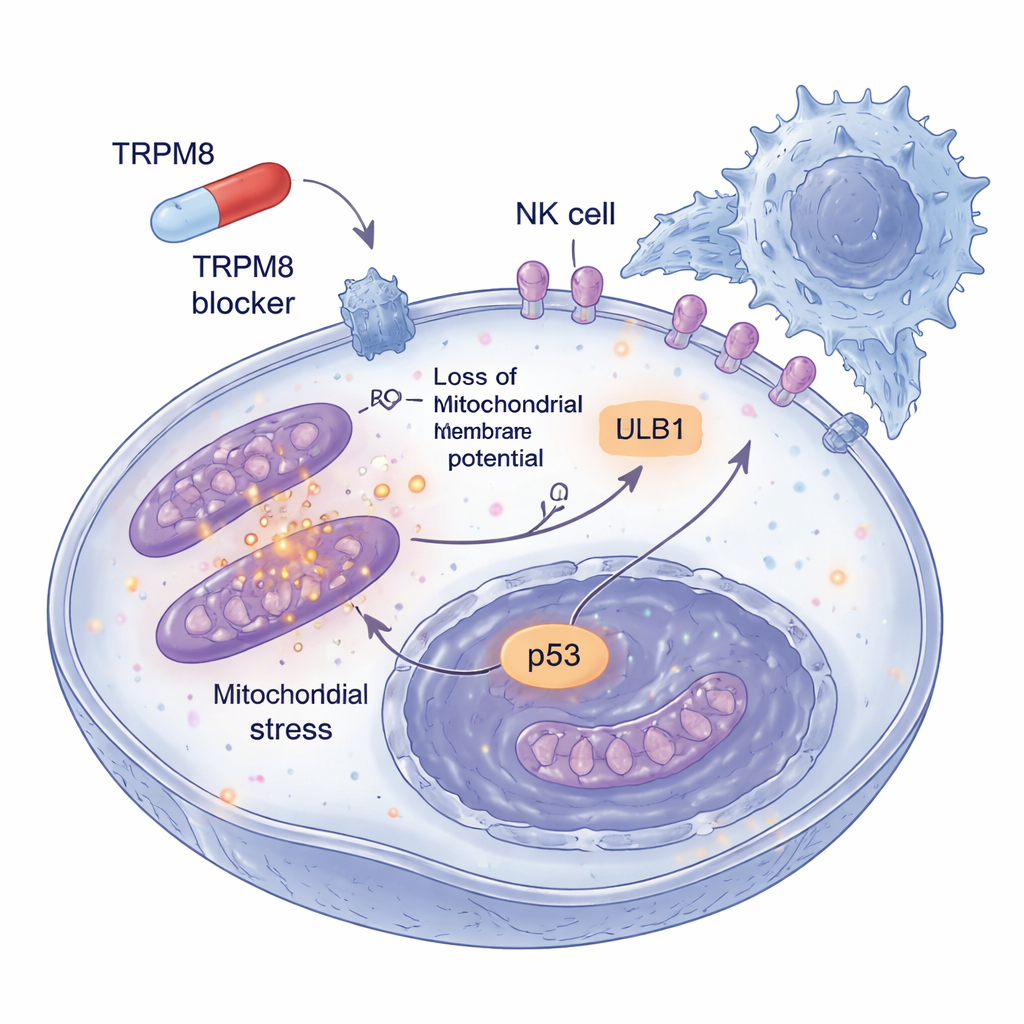
Qué podría significar esto para el cuidado futuro del melanoma
En términos simples, bloquear el “sensor de frío” TRPM8 lo convierte en una palanca terapéutica: empuja a las células de melanoma hacia una crisis mitocondrial y de ADN fatal mientras las marca para su destrucción por células NK. Dado que los fármacos respetan a las células de piel normales y no dañan a las células NK, ofrecen una base prometedora para nuevos tratamientos. Los autores sugieren que los bloqueadores de TRPM8 podrían combinarse con inmunoterapias existentes para atacar el melanoma avanzado y resistente a fármacos en dos frentes: matando directamente a las células tumorales y facilitando que el sistema inmune encuentre y elimine a las sobrevivientes.
Cita: Sorrentino, C., Lauretta, C., D’Angiolo, R. et al. Rewiring melanoma cell fate: TRPM8 modulators trigger apoptosis and boost NK cell cytotoxicity. Cell Death Dis 17, 223 (2026). https://doi.org/10.1038/s41419-026-08469-8
Palabras clave: melanoma, TRPM8, mitocondrias, estrés oxidativo, células asesinas naturales