Clear Sky Science · es
KIF20A inhibe la ubiquitinación dependiente de TRIM21 de DHX9 para aumentar la estabilidad de SOX2, potenciando la capacidad de células madre en COSC y la resistencia a la ferroptosis
Por qué esta investigación importa para pacientes con cáncer oral
El carcinoma de células escamosas oral, una forma frecuente de cáncer de boca, reaparece con frecuencia y muestra resistencia al tratamiento. Muchos fracasos de cirugía, quimioterapia y radioterapia se remontan a un pequeño y resistente grupo de "células madre cancerosas" que pueden volver a generar el tumor y resistir la muerte celular. Este estudio descubre un circuito molecular clave que ayuda a esas células a sobrevivir y a resistir una forma de muerte celular relativamente nueva llamada ferroptosis, y señala una estrategia farmacológica que podría hacer que la quimioterapia estándar funcione mejor.
Un impulsor oculto en los tumores bucales
Los investigadores comenzaron comparando muestras tumorales de pacientes con cáncer oral con tejido sano cercano. Hallaron que una proteína llamada KIF20A estaba consistentemente mucho más elevada en las células cancerosas. Al examinar conjuntos de datos de pacientes más amplios, las personas cuyos tumores presentaban niveles mayores de KIF20A tendían a vivir menos tiempo, lo que sugiere que esta proteína está ligada a una enfermedad agresiva. 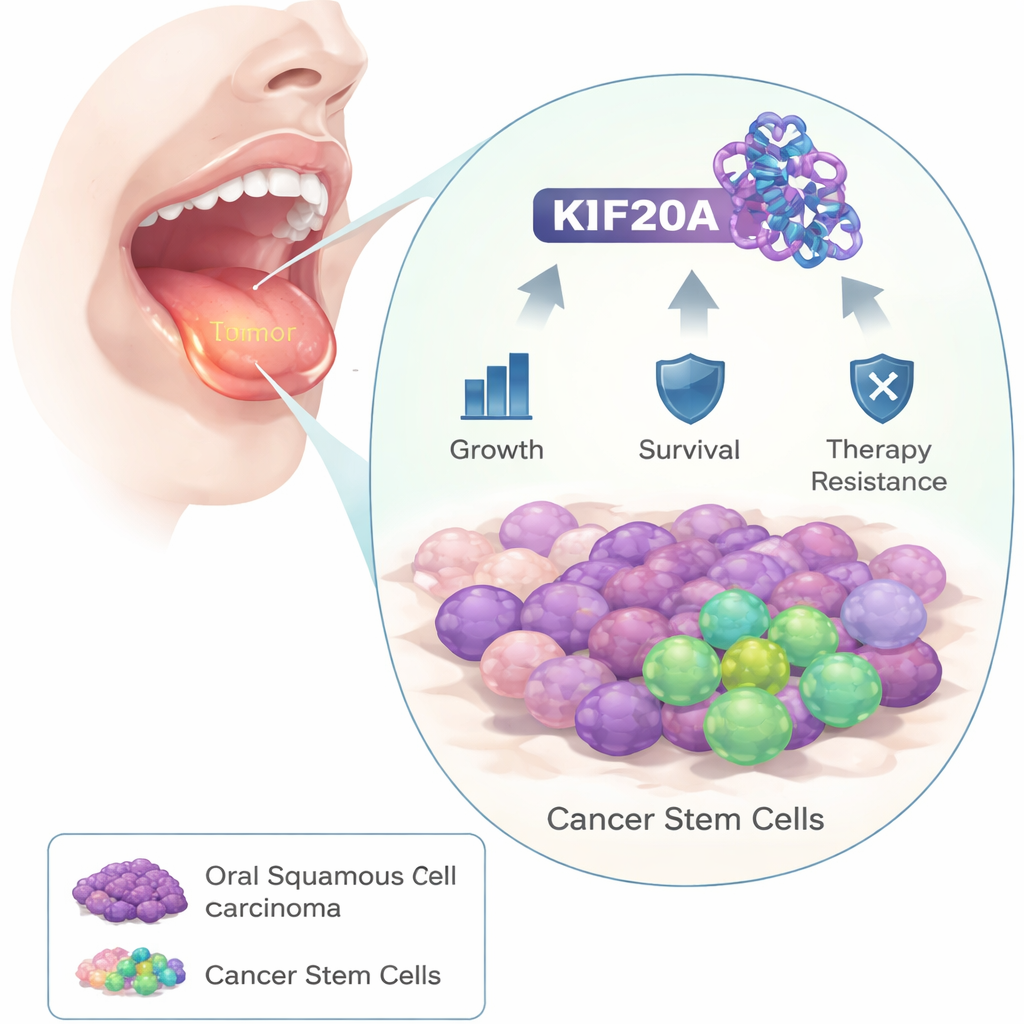
Cómo KIF20A protege a un coadyuvante clave del ARN
Para entender qué hace KIF20A, el equipo usó métodos de mapeo de proteínas para buscar sus socios dentro de las células cancerosas. Un socio central que emergió fue DHX9, una proteína que ayuda a gestionar moléculas de ARN e influye en la duración de ciertos mensajes en la célula. Los científicos descubrieron que KIF20A se une a DHX9 y evita que sea marcado para destrucción por otra proteína, la ligasa E3 TRIM21, que normalmente etiqueta a DHX9 con cadenas de ubiquitina que la envían al triturador de proteínas de la célula. Al bloquear este marcado, KIF20A frena la degradación de DHX9 y aumenta sus niveles, especialmente en el citoplasma de la célula, donde puede actuar sobre objetivos de ARN específicos.
De la estabilidad del ARN a las células madre cancerosas y la resistencia a la ferroptosis
Con DHX9 más estable, aparece otro actor crucial: SOX2, un gen maestro que ayuda a las células a mantener un estado similar al de las células madre y a resistir el tratamiento. El estudio muestra que DHX9 protege el mensaje de ARN de SOX2 frente a la degradación, permitiendo que se sintetice más proteína SOX2. En células de cáncer oral, KIF20A adicional condujo a niveles mayores de DHX9 y SOX2, más formación de esferoides tumorales en cultivo y una mayor fracción de células que expresan marcadores de células madre —señales de una mayor "capacidad de células madre cancerosas". KIF20A también hizo que las células fueran menos vulnerables a la ferroptosis, un tipo de muerte celular dependiente del hierro y relacionada con lípidos que se está explorando como vía para eliminar células cancerosas resistentes. Cuando se silenciaba KIF20A, los tumores en ratones se reducían con más facilidad y aumentaban los marcadores de ferroptosis, lo que indica que los tumores habían perdido este escudo protector.
Un circuito molecular con un punto débil susceptible de fármaco
Juntando las piezas, los autores proponen un eje KIF20A–DHX9–SOX2: KIF20A estabiliza DHX9, DHX9 estabiliza el ARN de SOX2, y SOX2 a su vez mantiene las células madre cancerosas y bloquea la ferroptosis. Este circuito también alimenta la vía PI3K–AKT, una ruta principal de crecimiento y supervivencia en muchos cánceres. 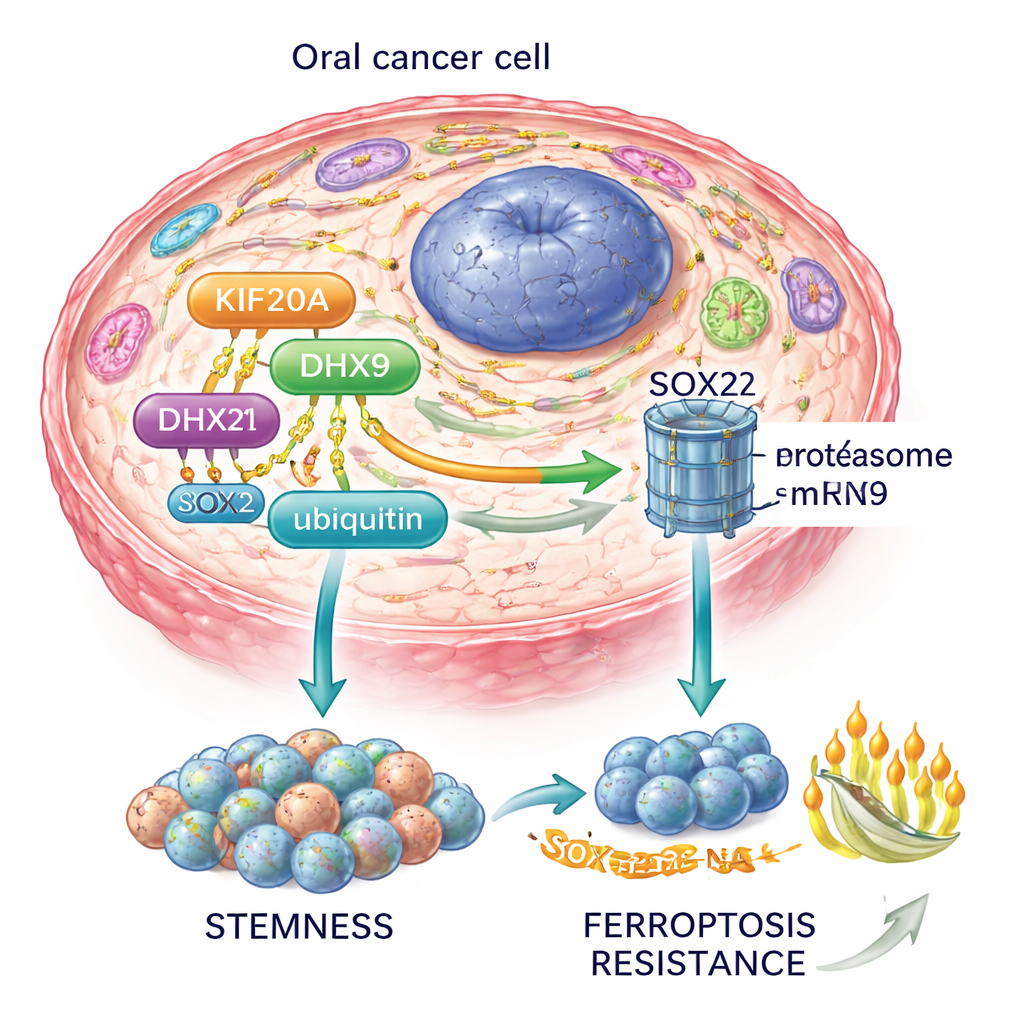
Un fármaco candidato para debilitar tumores resistentes
Para avanzar hacia el tratamiento, el equipo buscó en grandes bases de datos fármaco-gen gene compuestos predichos para contrarrestar los patrones génicos relacionados con KIF20A. Identificaron ENMD-2076, un inhibidor oral multitarget de quinasas ya probado en otros cánceres. En células de cáncer oral con altos niveles de KIF20A, ENMD-2076 redujo los niveles de KIF20A, DHX9 y SOX2, atenuó la señalización relacionada con la capacidad de células madre y ralentizó el crecimiento. Cuando se combinó con el fármaco de quimioterapia estándar cisplatino, ENMD-2076 produjo un efecto anticancerígeno más fuerte que cualquiera de los dos fármacos por separado tanto en cultivos celulares como en tumores de ratón, sin toxicidad añadida obvia.
Qué significa esto para futuras terapias
Para un público no especialista, la conclusión es que este estudio revela cómo una proteína sobreactivada, KIF20A, ayuda a los tumores bucales a mantener un pequeño grupo de células "semilla" vivas y protegidas frente a una forma prometedora de muerte celular. Al mapear esta cadena —de KIF20A a DHX9 a SOX2—, los investigadores resaltan nuevos objetivos farmacológicos y muestran que un fármaco experimental existente, ENMD-2076, puede debilitar este eje y hacer que el cisplatino sea más eficaz en modelos. Aunque se necesita más trabajo para evaluar seguridad y confirmar beneficios en pacientes, los hallazgos respaldan un futuro en el que bloquear este circuito podría ayudar a prevenir recaídas y superar la resistencia a fármacos en el cáncer oral.
Cita: Zhang, Z., Li, Y., Hu, J. et al. KIF20A inhibits TRIM21-dependent ubiquitination of DHX9 to boost SOX2 stability, enhancing OSCC stemness and ferroptosis resistance. Cell Death Dis 17, 218 (2026). https://doi.org/10.1038/s41419-026-08467-w
Palabras clave: carcinoma de células escamosas oral, células madre cancerosas, ferroptosis, KIF20A, SOX2