Clear Sky Science · es
Selenometionina como inhibidor de la ferroptosis de doble mecanismo: suministro de selenio que impulsa la biosíntesis de GPX4 más allá de la transsulfuración y eliminación de ROS mediada por capacidad reductora independiente de la actividad de GPX4
Por qué importa proteger nuestras células de una muerte “tipo óxido”
Las células de nuestro cuerpo pueden morir de muchas maneras, y una de las más recientes e interesantes se denomina ferroptosis: un tipo de daño impulsado por hierro, parecido a la “oxidación” de las membranas celulares. Este proceso se ha relacionado con enfermedades que van desde la lesión renal hasta la neurodegeneración. El oligoelemento selenio, conocido por muchos por su presencia en suplementos dietéticos, resulta jugar un papel clave en la detención de esta peligrosa forma de muerte celular. Este estudio explora cómo un aminoácido común que contiene selenio, la selenometionina, puede proteger a las células de la ferroptosis mediante no una, sino dos estrategias protectoras distintas.
Un nuevo defensor hallado tras una gran búsqueda farmacológica
Para encontrar moléculas pequeñas que pudieran bloquear la ferroptosis, los investigadores cribaron miles de compuestos procedentes de fármacos aprobados por la FDA y de productos naturales. Emplearon una sustancia química llamada RSL3 para desencadenar la ferroptosis en líneas celulares humanas de cáncer y monitorizaron la muerte celular y la acumulación de lípidos oxidados dañados en las membranas. Entre todos los candidatos, la selenometionina emergió como una protección eficaz: redujo tanto el daño lipídico como la muerte celular en distintos tipos de células y en dos modelos principales de ferroptosis —uno impulsado por la inhibición directa de GPX4 (con RSL3) y otro por la privación de cistina, un precursor del antioxidante glutatión. Estos resultados situaron a la selenometionina como un inhibidor de ferroptosis amplio y robusto. 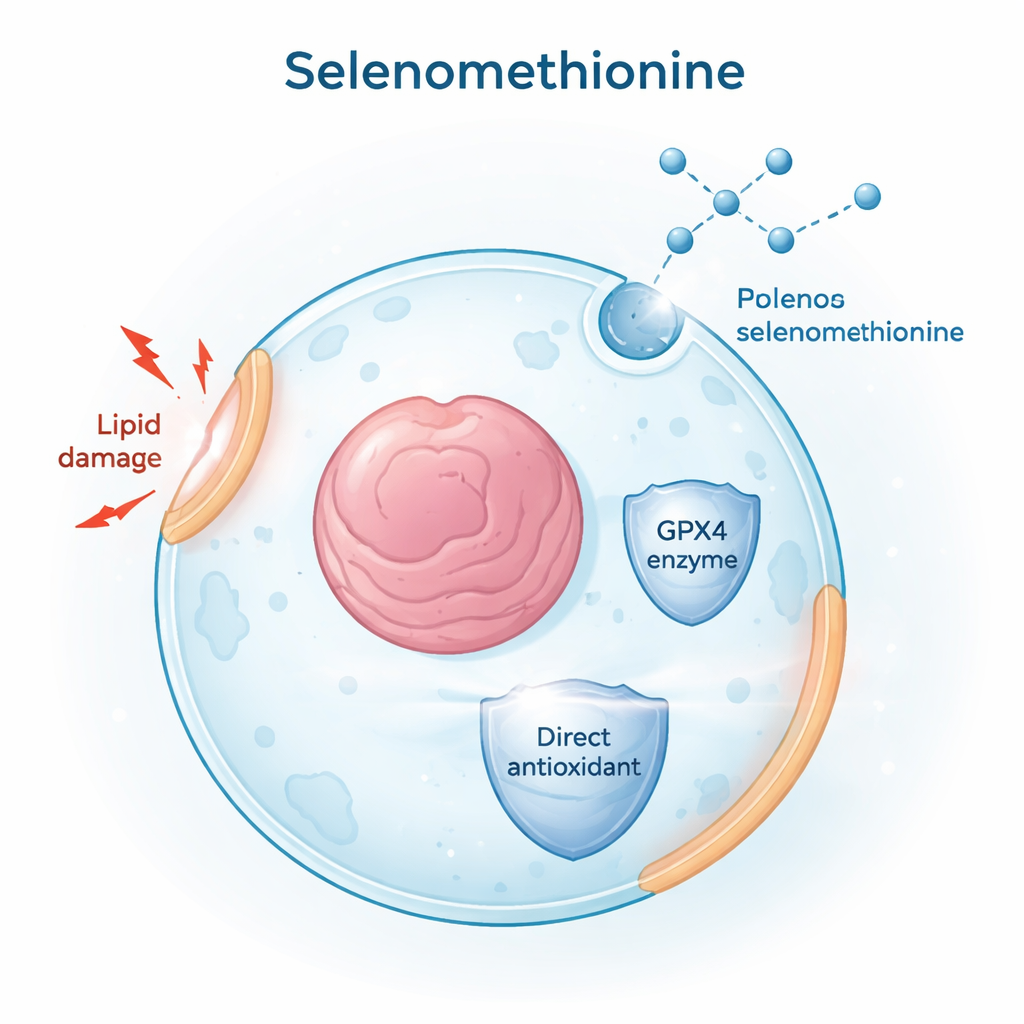
Suministro de selenio para una enzima protectora clave
Un pilar de la defensa anti‑ferroptosis en las células es una enzima llamada GPX4, que depende del selenio para funcionar. El equipo buscó determinar si la selenometionina simplemente alimenta esta vía o si hace algo más. Rastrearon cómo el selenio procedente de la selenometionina podía convertirse en formas aptas para la síntesis de GPX4, incluso cuando una ruta habitual, denominada vía de la transsulfuración, estaba deteriorada u obstruida. Usando silenciamiento genético y inhibidores químicos de enzimas en estas rutas de azufre‑selenio, encontraron que la selenometionina seguía elevando los niveles de GPX4 y protegiendo a las células. Esto demostró que las células pueden recurrir a múltiples rutas metabólicas para extraer selenio de la selenometionina y mantener la producción de GPX4, incluso en tejidos donde la vía clásica es débil.
Protección que no depende de la enzima habitual
Sorprendentemente, cuando los investigadores eliminaron por completo GPX4 de las células mediante edición genética CRISPR, la selenometionina siguió protegiendo frente a la ferroptosis. Continuó reduciendo el daño lipídico en las membranas y la muerte celular, lo que indica que GPX4 no explica todo el efecto. Experimentos adicionales sugirieron que parte de esta protección implica la incorporación de selenometionina en proteínas recién sintetizadas, pero que eso solo explica una fracción del efecto. Los autores se centraron entonces en la reactividad química de la propia selenometionina. Encontraron que puede neutralizar directamente especies reactivas de oxígeno (ROS), incluido el peróxido de hidrógeno, y que se convierte en una forma oxidada, el “sulfoxido”. La espectrometría de masas confirmó este producto, y administrar a las células la versión sulfoxida también redujo la ferroptosis, lo que implica que las células pueden reciclarla de vuelta a la selenometionina activa en un ciclo redox.
De cultivo celular a la protección renal en animales vivos
Para evaluar si estos mecanismos importan en un organismo entero, el equipo recurrió a un modelo de ratón de lesión renal aguda causada por el fármaco anticancerígeno cisplatino, una condición conocida por implicar ferroptosis. Los ratones tratados con cisplatino mostraron pérdida de peso, riñones inflamados, función renal deteriorada y niveles elevados de marcadores de ferroptosis. Cuando los animales recibieron selenometionina, muchas de estas alteraciones mejoraron: se recuperó el peso corporal, disminuyó la inflamación renal, se normalizaron las medidas sanguíneas de la función renal, cayeron las señales inflamatorias y se redujeron los marcadores químicos de daño lipídico. El tejido renal también mostró niveles más altos de GPX4 y menos lesiones estructurales. Estos beneficios fueron comparables a los observados con ferrostatina‑1, un conocido inhibidor experimental de la ferroptosis. 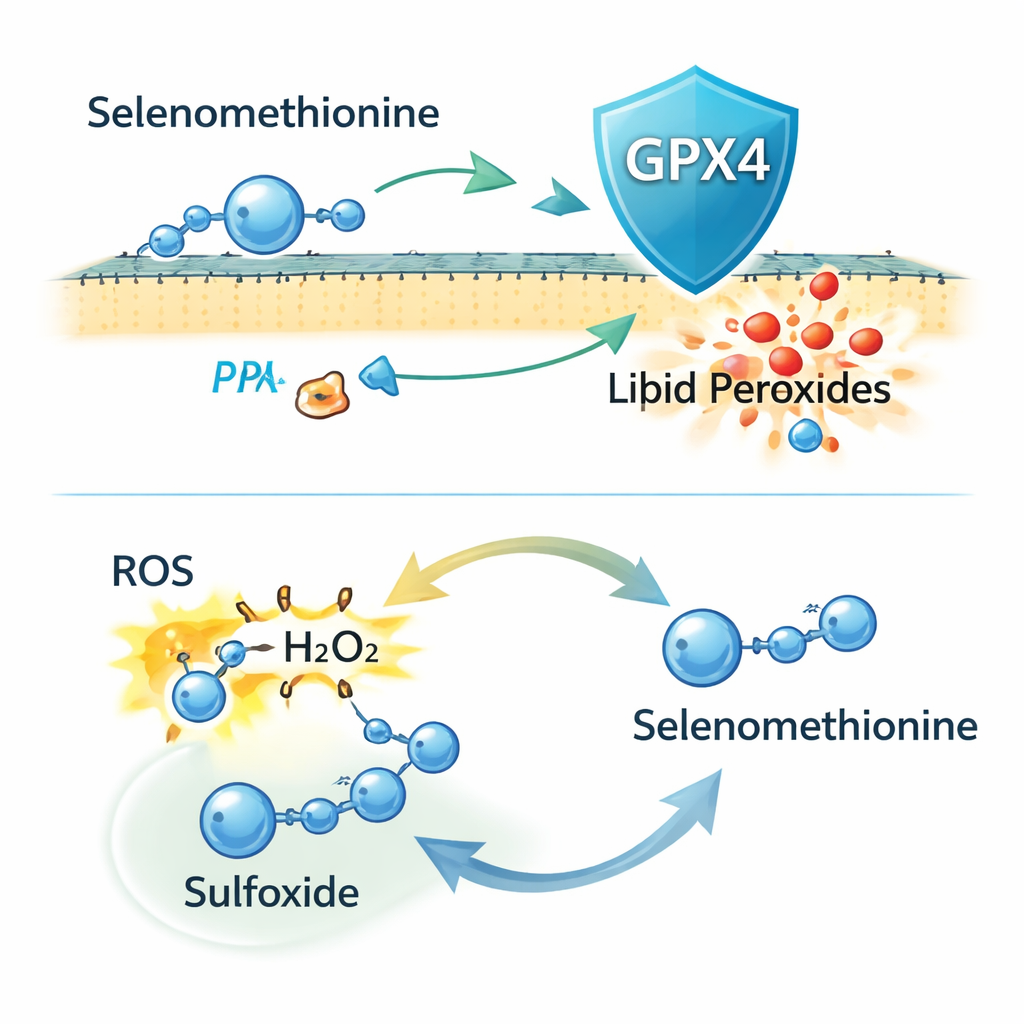
Qué implica esto para futuras terapias
En términos cotidianos, este trabajo sugiere que la selenometionina actúa como un extintor de incendios de doble propósito contra un “oxidado” impulsado por hierro de las membranas celulares. Por un lado, suministra selenio para que las células sinteticen más de la enzima GPX4, que actúa como un equipo de limpieza interno para los lípidos dañados. Por otro lado, la selenometionina misma puede absorber oxidantes dañinos y reciclarse, ofreciendo una protección complementaria independiente de GPX4. En conjunto, estas características convierten a la selenometionina en una candidata prometedora para prevenir o tratar enfermedades en las que la ferroptosis desempeña un papel central, como el daño renal inducido por fármacos y, potencialmente, otras condiciones impulsadas por estrés oxidativo descontrolado.
Cita: Xia, C., Sun, X., Shao, J. et al. Selenomethionine as a dual-mechanism ferroptosis inhibitor: selenium-supply-driven GPX4 biosynthesis beyond transsulfuration and reductive-capacity-mediated ROS scavenging independent of GPX4 activity. Cell Death Dis 17, 224 (2026). https://doi.org/10.1038/s41419-026-08466-x
Palabras clave: ferroptosis, selenio, selenomethionina, estrés oxidativo, lesión renal aguda