Clear Sky Science · es
La chaperonina TRiC, componente Cct3, es necesaria para el transporte axonal, la mielinización y la refinación de la unión neuromuscular
Cuando el cableado nervioso falla
Nuestros cerebros y cuerpos dependen de largas fibras nerviosas parecidas a cables para transmitir señales de forma rápida y fiable. Para realizar ese trabajo, muchas fibras están envueltas en una vaina aislante, la mielina, y sus extremos deben formar contactos precisos con los músculos. Este artículo explora qué ocurre cuando falla un “ayudante” celular clave para el plegamiento de proteínas, llamado Cct3. Usando pez cebra y tejido humano, los autores muestran cómo este único componente de una gran máquina chaperona puede alterar la mielina, las conexiones nervio–músculo y el sistema de transporte interno que mantiene a las neuronas vivas y funcionales.
Un sastre celular para construir nervios
Dentro de cada célula, las proteínas recién sintetizadas deben plegarse en las formas correctas, igual que un sastre ajusta cuidadosamente un traje. El complejo TRiC, que incluye la subunidad Cct3, es uno de los principales “sastres”, ayudando a plegarse correctamente a cerca del 10% de las proteínas celulares, en especial las proteínas estructurales actina y tubulina. Estos bloques constructores forman el andamiaje interno de la célula y las vías por las que se mueven cargas vitales. En pacientes con versiones defectuosas de CCT3 y genes relacionados, las exploraciones cerebrales muestran una reducción de la materia blanca (el cableado rico en mielina del cerebro) y problemas en los nervios periféricos y los músculos. Los autores se propusieron entender cómo la pérdida de Cct3 descarrila el desarrollo y la función nerviosa.
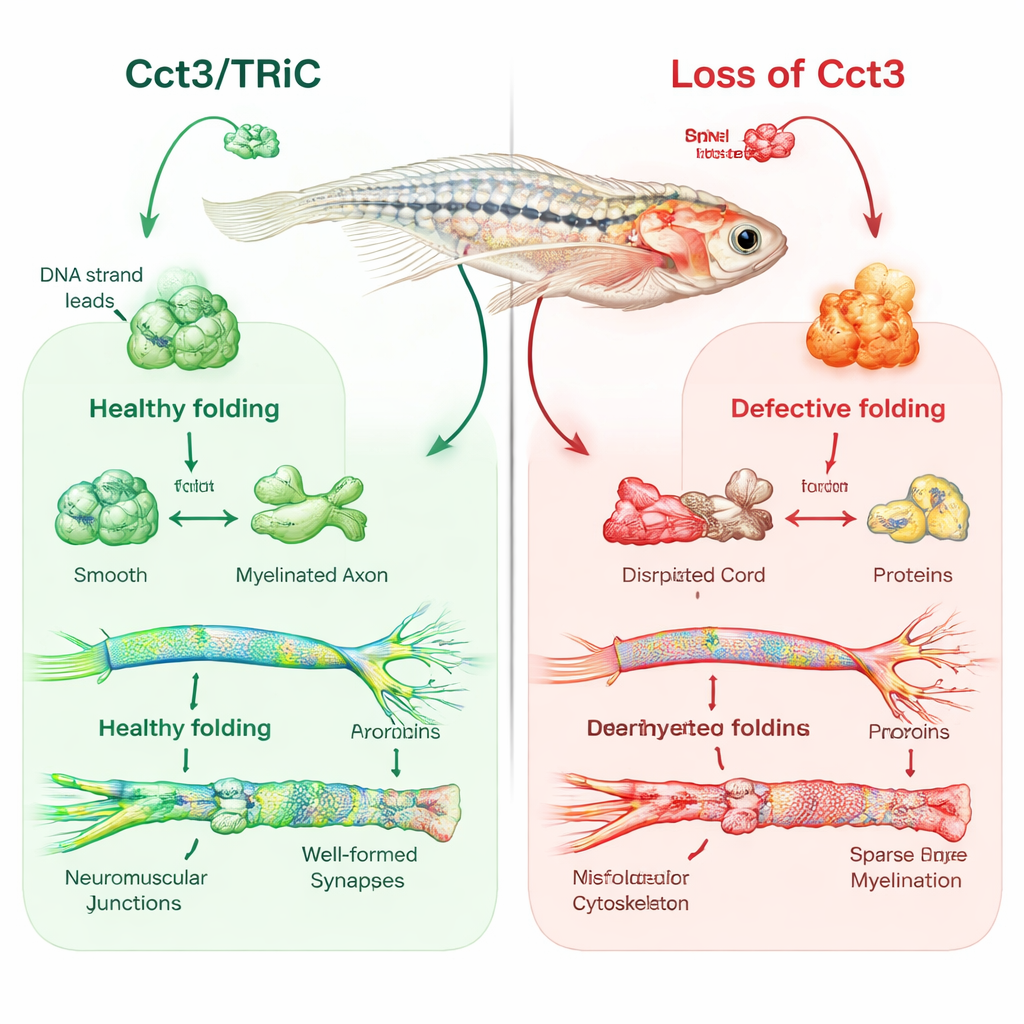
El pez cebra como ventana a la aislación nerviosa
El equipo usó edición génica CRISPR/Cas9 para crear pez cebra que carecían de cct3 funcional. Estos pequeños peces mostraron cerebros y ojos más pequeños, acumulación de líquido alrededor del corazón, respuestas débiles al tacto y murieron a los pocos días. Cuando los investigadores restablecieron cct3 normal inyectando su ARN mensajero, muchas de estas alteraciones mejoraron, confirmando que la pérdida de Cct3 era la causa principal. Centrándose en la mielina, usaron marcadores fluorescentes y microscopía electrónica para visualizar las capas aislantes alrededor de los nervios. En peces normales, las células formadoras de mielina en el cerebro y los nervios periféricos envolvían los axones con vainas ordenadas y estratificadas para el día cuatro del desarrollo. En contraste, los mutantes de cct3 tenían muchas menos células mielinizantes y prácticamente no presentaban mielina adecuada alrededor de muchos axones, pese a que esos axones parecían tener forma normal en la superficie.
Células de soporte frágiles y enlaces nervio–músculo tensionados
Para averiguar por qué faltaba la mielina, los autores examinaron las células de Schwann y las células de la cresta neural relacionadas —las células de soporte que envuelven los nervios periféricos. En peces normales, estas células extendían procesos largos y delgados y luego refinaban su forma al formar segmentos de mielina. En los mutantes, se redondeaban, acortaban sus procesos y se fragmentaban. Sus núcleos se desintegraban siguiendo un patrón típico de muerte celular programada, y apareció un marcador clave de muerte (Caspasa 3 activada), mostrando que muchas de estas células morían prematuramente. Entretanto, en las uniones neuromusculares donde el nervio contacta el músculo, el patrón de “puntos calientes” de receptores en el músculo no se refinó. En lugar de muchos cúmulos pequeños y precisos, los mutantes presentaban menos parches de receptores, pero más grandes, eco de los pliegues sinoviales simplificados observados en un paciente humano con una mutación en CCT3.
Pistas internas rotas y tráfico de cargas ralentizado
Puesto que TRiC ayuda a plegar actina y tubulina, los autores inspeccionaron de cerca el andamiaje interno de los axones motores. Encontraron que los niveles totales de tubulina estaban marcadamente reducidos en los mutantes, y el número de microtúbulos normales —los tubos huecos que actúan como vías para el transporte— descendió dramáticamente tanto en los nervios centrales como en los periféricos. Las “señales” químicas en la tubulina que son importantes para microtúbulos estables y aptos para el transporte también se alteraron severamente. Usando imágenes en vivo de mitocondrias y endosomas fluorescentes en axones motores, observaron cómo se movían estas cargas. En peces sanos, los orgánulos viajaban con rapidez y en dirección a lo largo del axón. En los mutantes, muchos orgánulos se detenían o simplemente oscilaban de un lado a otro, coherente con pistas dañadas y transporte interrumpido.
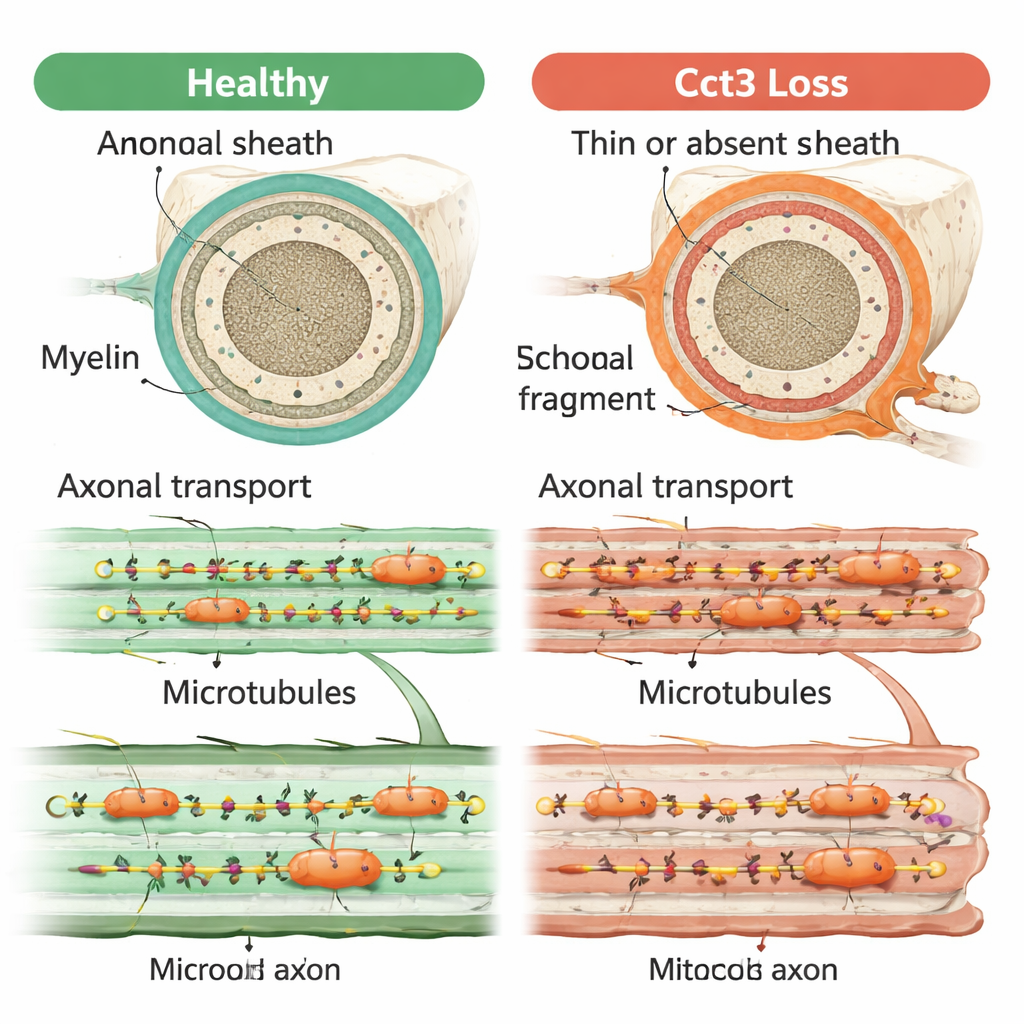
Un problema central tras muchos síntomas
En conjunto, los hallazgos muestran que Cct3 es esencial para varios aspectos interconectados de la salud nerviosa: sostiene la supervivencia de las células de soporte que forman la mielina, posibilita el envolvimiento adecuado de la mielina y permite que las uniones neuromusculares en maduración se afinen correctamente. Todos estos papeles pueden rastrearse hasta su función en plegar y mantener las proteínas que construyen el citoesqueleto y las vías de microtúbulos usadas para el transporte axonal. Cuando esas vías fallan, señales y materiales clave no pueden alcanzar los lugares correctos a lo largo del nervio, lo que probablemente socava tanto la comunicación con las células formadoras de mielina como la modelación de los contactos nervio–músculo. Este trabajo sugiere que el transporte axonal alterado puede ser el hilo común que vincula los diversos problemas cerebrales y nerviosos observados en los trastornos relacionados con TRiC.
Cita: Zhang, X., Zajt, K.K., Palaz, T. et al. The chaperonin TRiC component Cct3 is required for axonal transport, myelination, and neuromuscular junction refinement. Cell Death Dis 17, 221 (2026). https://doi.org/10.1038/s41419-026-08465-y
Palabras clave: mielinización, transporte axonal, unión neuromuscular, chaperonas moleculares, modelo de pez cebra