Clear Sky Science · es
Transporte y señalización BDNF‑TrkB alterados en neuronas del prosencéfalo basal en el síndrome de Down
Por qué importa este estudio cerebral
Las personas con síndrome de Down viven más que nunca, pero también afrontan un riesgo muy alto de desarrollar demencia similar a la del Alzheimer en la mediana edad. Este estudio examina a fondo células cerebrales individuales para entender por qué ciertas neuronas son tan vulnerables. Al rastrear cómo estas células mueven y responden a una molécula clave, un “fertilizante” cerebral, los investigadores descubren un atasco de tráfico dentro de las neuronas que podría ayudar a explicar la pérdida de memoria y apuntar a nuevas estrategias terapéuticas.
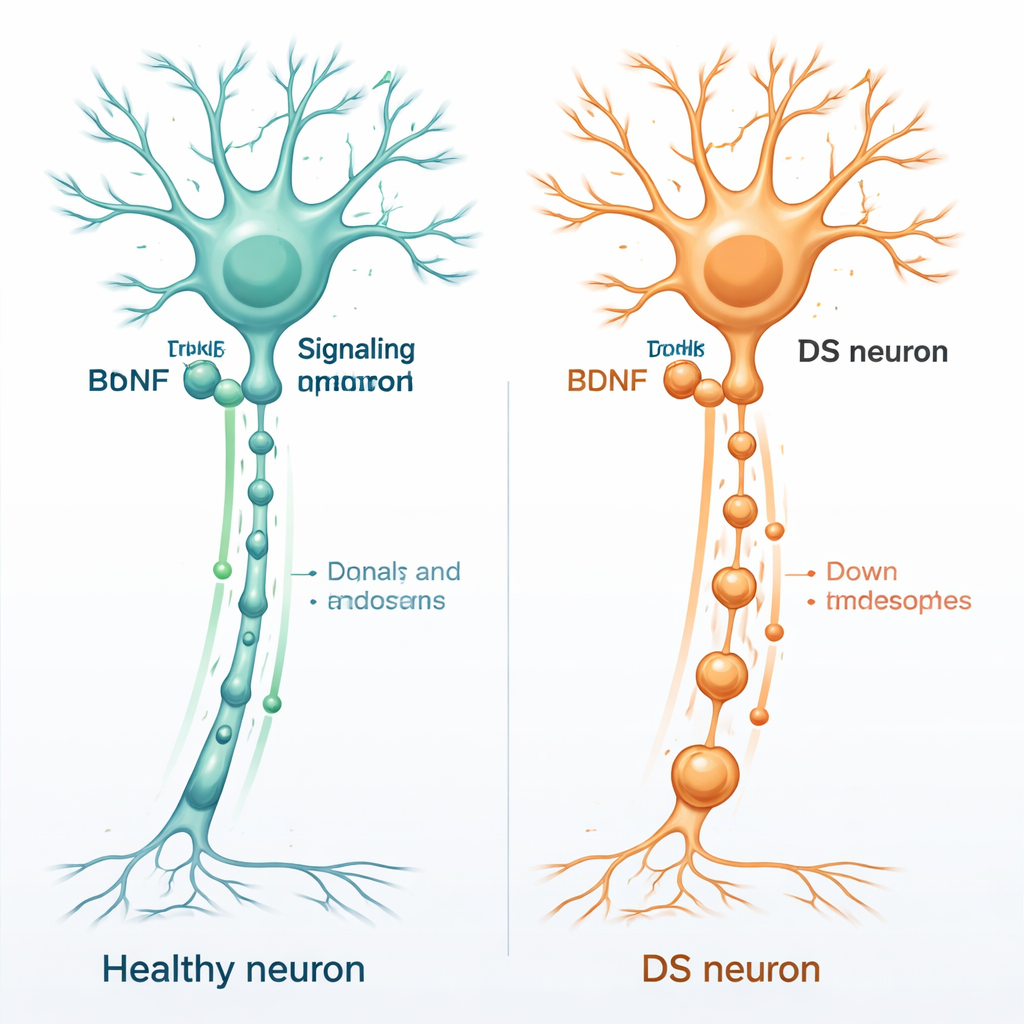
Fertilizante cerebral y salud de las neuronas
Las neuronas sanas dependen de un conjunto de moléculas de apoyo llamadas neurotrofinas, que actúan como fertilizantes para las células nerviosas. Una de las más importantes es el factor neurotrófico derivado del cerebro, o BDNF. El BDNF se une a una proteína receptora en las neuronas llamada TrkB, habitualmente en los extremos distales de las fibras nerviosas. Una vez que el BDNF se acopla, todo el complejo BDNF–TrkB se introduce en pequeñas burbujas membranosas y se transporta de vuelta a lo largo de la fibra nerviosa hasta el cuerpo celular. Estas burbujas móviles, conocidas como endosomas de señalización, indican al núcleo qué genes activar para mantener la neurona viva, conectada y adaptable.
Cuando los contenedores celulares de transporte crecen demasiado
El equipo se centró en las neuronas del prosencéfalo basal, un grupo de células que sostiene fuertemente la memoria y la atención y que es una de las primeras en degenerarse tanto en el síndrome de Down como en la enfermedad de Alzheimer. Usando un modelo de ratón del síndrome de Down llamado Dp1Tyb, tiñeron neuronas con un marcador de endosoma temprano y las compararon con neuronas normales. Las neuronas del síndrome de Down contenían muchos más endosomas tempranos que eran más de un 50 % más grandes de lo habitual. Estas estructuras están reguladas por Rab5, un interruptor molecular que ayuda a formar y clasificar estos “contenedores de envío” internos. Los investigadores hallaron que Rab5 estaba bloqueado en un estado sobreactivado en las neuronas del síndrome de Down, incluso antes de la estimulación con BDNF, lo que sugiere que el sistema endosomal ya estaba acelerado.
Atascos de tráfico a lo largo del axón
A continuación, los científicos se preguntaron si este paisaje interno distorsionado interfería con el movimiento de las señales del BDNF. Cultivaron neuronas en dispositivos microfluídicos que separan los cuerpos celulares de sus terminales axónicas, lo que les permitió estimular solo las puntas axónicas. Siguiendo trazadores fluorescentes inocuos que comparten la misma ruta de transporte que los complejos BDNF–TrkB, midieron la velocidad a la que los endosomas de señalización viajaban de regreso hacia los cuerpos celulares. En las neuronas normales, la adición de BDNF hizo que los endosomas se movieran aproximadamente un 30 % más rápido y se detuvieran con menor frecuencia, reflejando una respuesta sólida a las señales de crecimiento. En las neuronas del síndrome de Down, sin embargo, el BDNF no aceleró el transporte ni redujo las pausas. Un experimento separado que rastreó receptores TrkB reales confirmó que menos de ellos llegaban con éxito al cuerpo celular en las células del síndrome de Down.
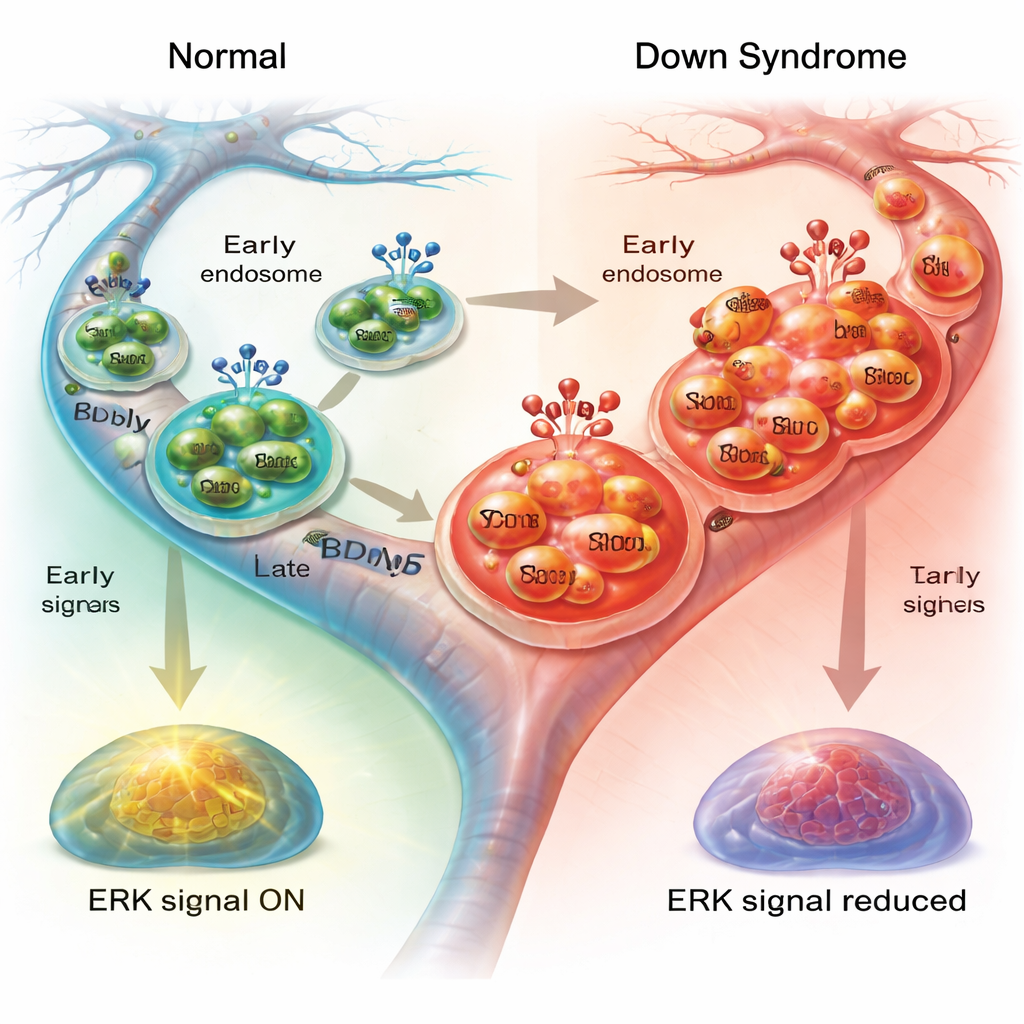
Señales posteriores dentro de la célula atenuadas
Para que estas burbujas en tránsito sostengan la salud neuronal, deben activar vías de señalización internas una vez que alcanzan su destino. Una ruta clave implica ERK1/2, un par de enzimas que transmiten el mensaje del BDNF al núcleo y ayudan a regular el esqueleto celular y la maquinaria de transporte. Cuando los investigadores midieron ERK1/2 activado tras el tratamiento con BDNF, observaron un aumento claro en las neuronas normales pero una respuesta mucho más débil en las neuronas del síndrome de Down, especialmente en los axones. Bloquear ERK1/2 en neuronas sanas reprodujo en parte el transporte lento observado en las células del síndrome de Down, frenando los endosomas y aumentando sus pausas. En cambio, el bloqueo de ERK1/2 tuvo poco efecto adicional en las neuronas del síndrome de Down, coherente con una señalización ya atenuada.
Qué implica esto para el envejecimiento cerebral en el síndrome de Down
En conjunto, los hallazgos sugieren un problema autorreforzante en neuronas vulnerables: Rab5 está sobreactivado, los endosomas tempranos se hinchan y los complejos BDNF–TrkB quedan atrapados en compartimentos que no se mueven eficientemente. Como resultado, menos señales de crecimiento alcanzan el cuerpo celular, la señalización por ERK1/2 se debilita y la maquinaria que impulsa el transporte a larga distancia queda todavía más comprometida. Con el tiempo, este sistema de comunicación defectuoso puede contribuir a la pérdida temprana y severa de neuronas del prosencéfalo basal observada en la enfermedad tipo Alzheimer asociada al síndrome de Down. Al destacar este vínculo entre el “control de tráfico” endosomal y la señalización por factores de crecimiento, el estudio apunta a nuevas ideas terapéuticas que buscan normalizar la actividad de Rab5, restaurar la función endosomal y reforzar las respuestas al BDNF para ayudar a proteger estas neuronas críticas.
Cita: Blackburn, E., Birsa, N., Lopes, A.T. et al. Impaired BDNF-TrkB trafficking and signalling in Down syndrome basal forebrain neurons. Cell Death Dis 17, 214 (2026). https://doi.org/10.1038/s41419-026-08464-z
Palabras clave: Síndrome de Down, Enfermedad de Alzheimer, BDNF, transporte axonal, endosomas