Clear Sky Science · es
La señalización por acetilación de PDHA1 suprime la cuproptosis para atenuar el efecto antiandrogénico en el cáncer de próstata
Por qué importa esta investigación
El cáncer de próstata es uno de los cánceres más comunes en hombres, y muchos casos avanzados se tratan con fármacos que bloquean las señales hormonales masculinas. Un fármaco clave, enzalutamida, suele funcionar al principio pero luego deja de ser efectivo cuando los tumores desarrollan resistencia. Este estudio revela una razón sorprendente por la que algunos cánceres de próstata escapan a los efectos de la enzalutamida y muestra cómo bloquear una única vía metabólica podría volver a sensibilizar a los tumores, abriendo la puerta a tratamientos más duraderos.
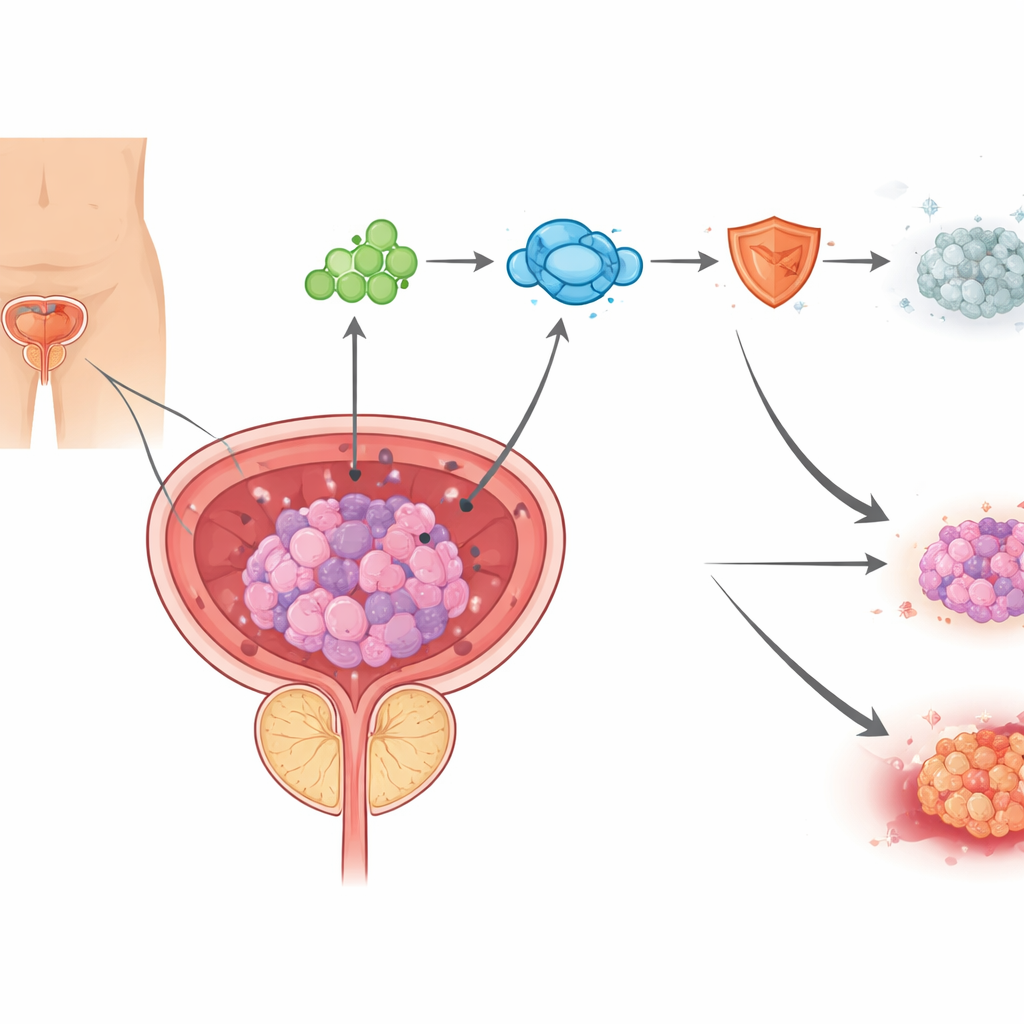
Un nuevo tipo de muerte celular impulsado por el cobre
Las células pueden morir de muchas maneras distintas, y la investigación oncológica moderna intenta cada vez más reactivar estos programas naturales de muerte en las células tumorales. Los autores se centran en una forma de muerte celular descrita recientemente llamada cuproptosis, que se desencadena cuando el cobre se acumula dentro de las mitocondrias, las centrales energéticas de la célula. En muestras de cáncer de próstata de pacientes tratados con fármacos bloqueadores de andrógenos, el equipo encontró señales de acumulación de cobre y daño mitocondrial, junto con cambios en proteínas que son señales distintivas de la cuproptosis. En cultivos celulares, la enzalutamida aumentó los niveles de cobre y dañó las mitocondrias, y un compuesto que une cobre pudo rescatar en gran medida a las células, lo que demuestra que la enzalutamida puede matar células de cáncer de próstata en parte al empujarlas hacia una muerte impulsada por cobre.
Cómo los tumores amortiguan el golpe tóxico del cobre
Sin embargo, no todas las células cancerosas sucumben. Al analizar varios conjuntos de datos de tumores de próstata resistentes a la enzalutamida y centrarse en genes relacionados con la cuproptosis, los investigadores identificaron una proteína destacada: PDHA1, una pieza central del mecanismo que convierte el combustible derivado de la glucosa en acetil‑CoA, un bloque constructivo clave de la célula. Los niveles de PDHA1 eran más altos en tumores resistentes, se asociaban con peor supervivencia y enfermedad más agresiva, y aumentaban por la misma enzalutamida. En experimentos de laboratorio, reducir PDHA1 hizo que las células cancerosas fueran mucho más sensibles tanto a la enzalutamida como a un fármaco que induce directamente la cuproptosis, mientras que aumentar PDHA1 las hacía más difíciles de eliminar. En ratones, los tumores con PDHA1 reducido se encogieron mucho más bajo tratamiento con enzalutamida, confirmando que esta enzima ayuda a los tumores a resistir la terapia en organismos vivos.
Un escudo metabólico y epigenético frente al tratamiento
El equipo desentrañó entonces cómo PDHA1 construye este escudo. Dado que PDHA1 alimenta la producción de acetil‑CoA, probaron si podría cambiar la forma en que se empaqueta y lee el ADN. Cuando PDHA1 era alto, aumentaban los niveles de acetil‑CoA y las marcas químicas de “acetilo” en las histonas, especialmente en una marca asociada a genes activos. Uno de los beneficiarios clave fue SLC7A11, un transportador que introduce cisteína en las células para fabricar glutatión, un antioxidante principal. Con más PDHA1, las células producían más glutatión; con menos PDHA1, la cisteína y el glutatión disminuían. El glutatión, a su vez, se unía y neutralizaba el cobre, reduciendo el estrés que desencadena la cuproptosis. Restaurar glutatión o SLC7A11 pudo deshacer el aumento del estrés por cobre observado cuando PDHA1 estaba bloqueada, demostrando que la cadena PDHA1–acetil‑CoA–histona–SLC7A11–glutatión permite a las células cancerosas limpiar el cobre y evitar la muerte.
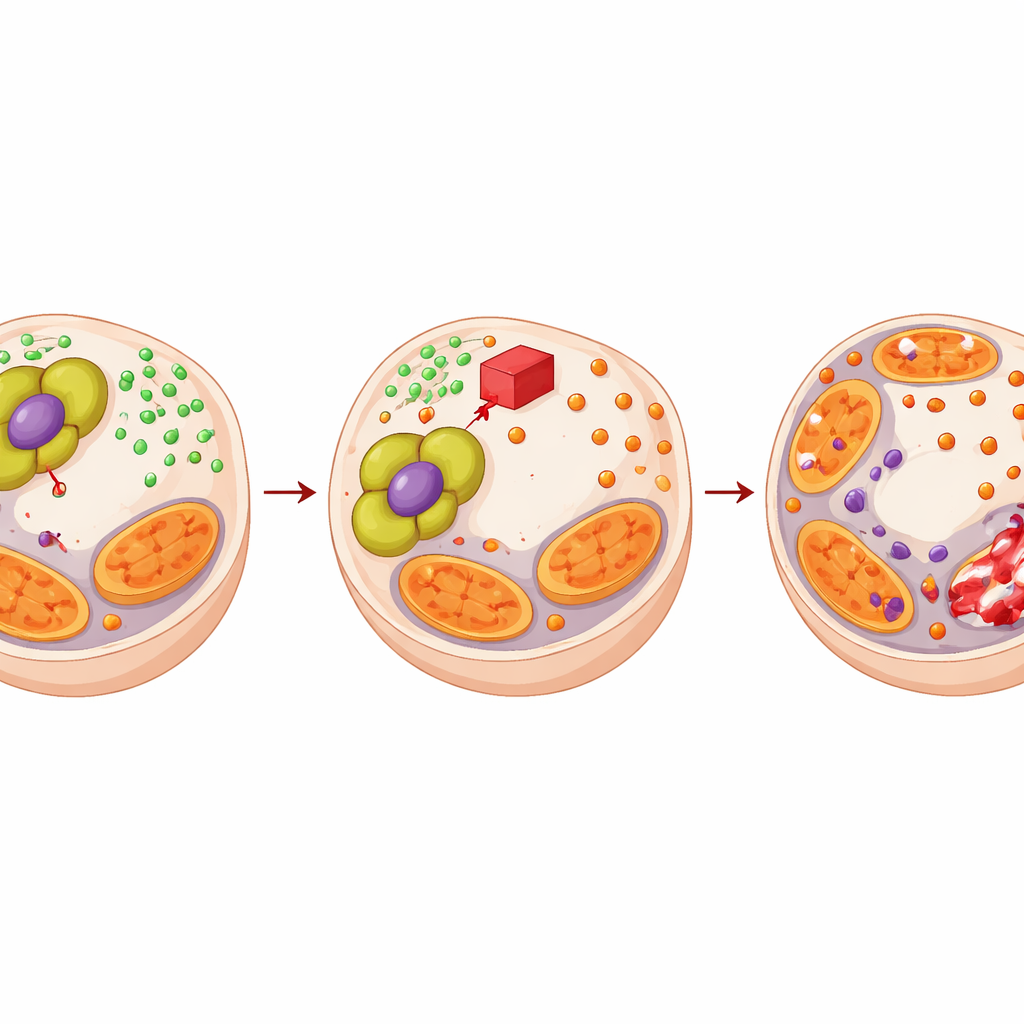
Convertir una vulnerabilidad en una estrategia terapéutica
Dado que PDHA1 ayuda a los tumores a resistir la enzalutamida al reforzar este sistema tampón de cobre, los autores se preguntaron si un fármaco dirigido a PDHA1 podría cambiar la situación. Usaron CPI‑613, un compuesto que altera el mismo complejo metabólico. CPI‑613 por sí solo aumentó el estrés por cobre y dañó proteínas mitocondriales en células de cáncer de próstata, pero preservó las células prostáticas normales. Cuando se combinó con enzalutamida, CPI‑613 redujo el crecimiento de células cancerosas mucho más que cualquiera de los tratamientos por separado, con análisis matemáticos que confirmaron una sinergia real. En modelos tumorales en ratones e implantes tumorales derivados de pacientes, la pareja de fármacos produjo tumores más pequeños, más tejido necrótico, menos células en división y firmas más intensas de muerte celular impulsada por cobre.
Qué significa esto para los pacientes
En conjunto, estos hallazgos muestran que algunos cánceres de próstata escapan a la enzalutamida al recablear su metabolismo para generar más acetil‑CoA, reescribir la actividad génica y aumentar el glutatión, que absorbe el cobre tóxico y bloquea la cuproptosis. Al inhibir PDHA1, este circuito protector puede desmantelarse, permitiendo que avance la muerte celular impulsada por cobre y restaurando el efecto de la terapia bloqueadora de hormonas. Aunque aún hacen falta ensayos clínicos, el trabajo apunta a una estrategia concreta y comprobable: combinar enzalutamida con fármacos dirigidos a PDHA1 como CPI‑613 para superar la resistencia en hombres con cáncer de próstata avanzado y de difícil tratamiento.
Cita: Zhuang, R., Zhou, Q., Cheng, B. et al. PDHA1–acetylation signaling suppresses cuproptosis to attenuate anti-androgen effect in prostate cancer. Cell Death Dis 17, 243 (2026). https://doi.org/10.1038/s41419-026-08462-1
Palabras clave: cáncer de próstata, resistencia a fármacos, muerte celular inducida por cobre, metabolismo del cáncer, regulación epigenética