Clear Sky Science · es
La señalización IRE1 endotelial mantiene la integridad de la barrera hematoencefálica y limita la neuroinflamación tras una lesión cerebral traumática
Por qué importa proteger la pared interior del cerebro
Tras un golpe en la cabeza, el daño inmediato es solo una parte de la historia. En las horas y días siguientes, el cerebro desencadena una potente respuesta de estrés e inmune que puede ampliar silenciosamente la lesión. Este estudio explora cómo un diminuto sistema sensor de estrés dentro de las células que recubren los vasos sanguíneos cerebrales ayuda a mantener sellada y tranquila la pared interior del cerebro—la barrera hematoencefálica—después de una lesión cerebral traumática. Comprender esta defensa oculta podría señalar nuevos tratamientos que limiten la discapacidad persistente tras un traumatismo craneoencefálico.
Los guardianes del cerebro bajo estrés
El cerebro depende de una barrera especializada formada por células endoteliales, que recubren el interior de los vasos sanguíneos y controlan estrictamente qué puede pasar de la sangre al tejido cerebral. La lesión cerebral traumática (LCT) puede alterar esta barrera hematoencefálica, permitiendo que moléculas inflamatorias y células inmunitarias entren y empeoren el daño. Dentro de estas células endoteliales existe un sistema de control de calidad llamado respuesta ante proteínas desplegadas, que ayuda a las células a afrontar el estrés en una estructura denominada retículo endoplásmico. Uno de sus componentes clave, conocido como IRE1, actúa como sensor y regulador cuando las células están bajo presión. Los investigadores se preguntaron: ¿este sensor de estrés endotelial ayuda a defender la barrera tras una LCT, o empeora la situación?
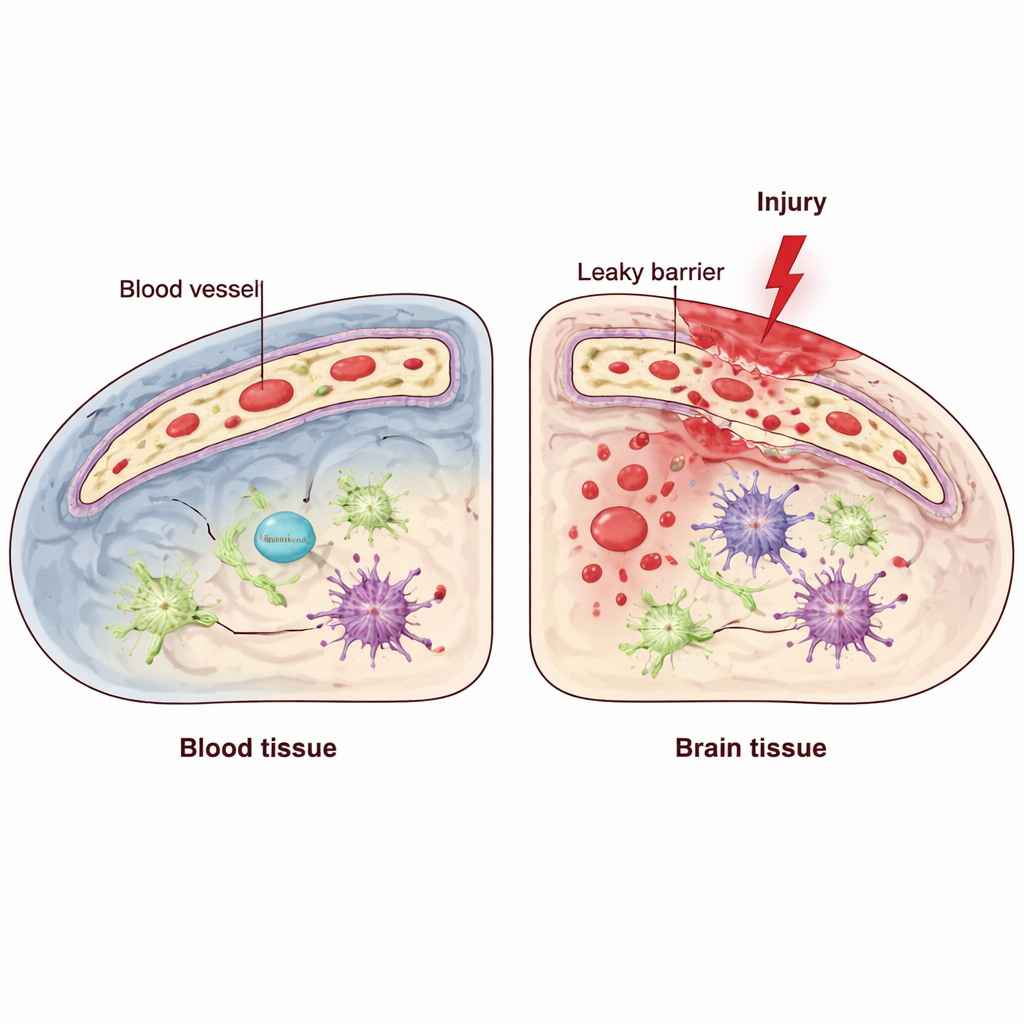
Apagar un sensor celular en las células vasculares
Para averiguarlo, el equipo utilizó ratones modificados genéticamente en los que IRE1 podía desactivarse selectivamente solo en las células endoteliales. Luego indujeron una lesión controlada en el área motora de la corteza, imitando aspectos de la LCT humana, y compararon estos ratones con sus compañeros normales. Evaluaron el movimiento con pruebas que miden el equilibrio y la colocación precisa de las patas, y examinaron el tejido cerebral con microscopía de alta resolución y técnicas moleculares. En ratones normales, la actividad de IRE1 aumentó en las células de los vasos sanguíneos cerca de la lesión poco después del trauma, lo que sugiere que las células endoteliales detectan y responden rápidamente al estrés. Cuando IRE1 faltaba específicamente en estas células, los animales rindieron peor en las pruebas motoras, lo que indica una recuperación funcional más pobre.
Vasos permeables, más células inmunitarias y neuronas moribundas
Los investigadores examinaron a continuación cómo se mantenía la barrera hematoencefálica. Normalmente, proteínas sanguíneas grandes como los anticuerpos permanecen dentro de los vasos. Tras una LCT, se espera cierta filtración cerca de la lesión, pero los ratones sin IRE1 endotelial mostraron una infiltración mucho más generalizada de estas proteínas en el cerebro. La microscopía reveló que una molécula de unión clave, VE-cadherina, que ayuda a sellar las células endoteliales entre sí, se redujo en el área lesionada cuando IRE1 estaba ausente, aunque el número total de vasos parecía similar. Esta permeabilidad fue acompañada por una oleada de células inmunitarias que entraron en el cerebro alrededor de la lesión y por niveles más altos de señales inflamatorias. En esas mismas regiones, las neuronas mostraron más signos de degeneración y muerte celular programada, y la zona de tejido dañado que rodea el núcleo de la lesión resultó visiblemente más amplia.
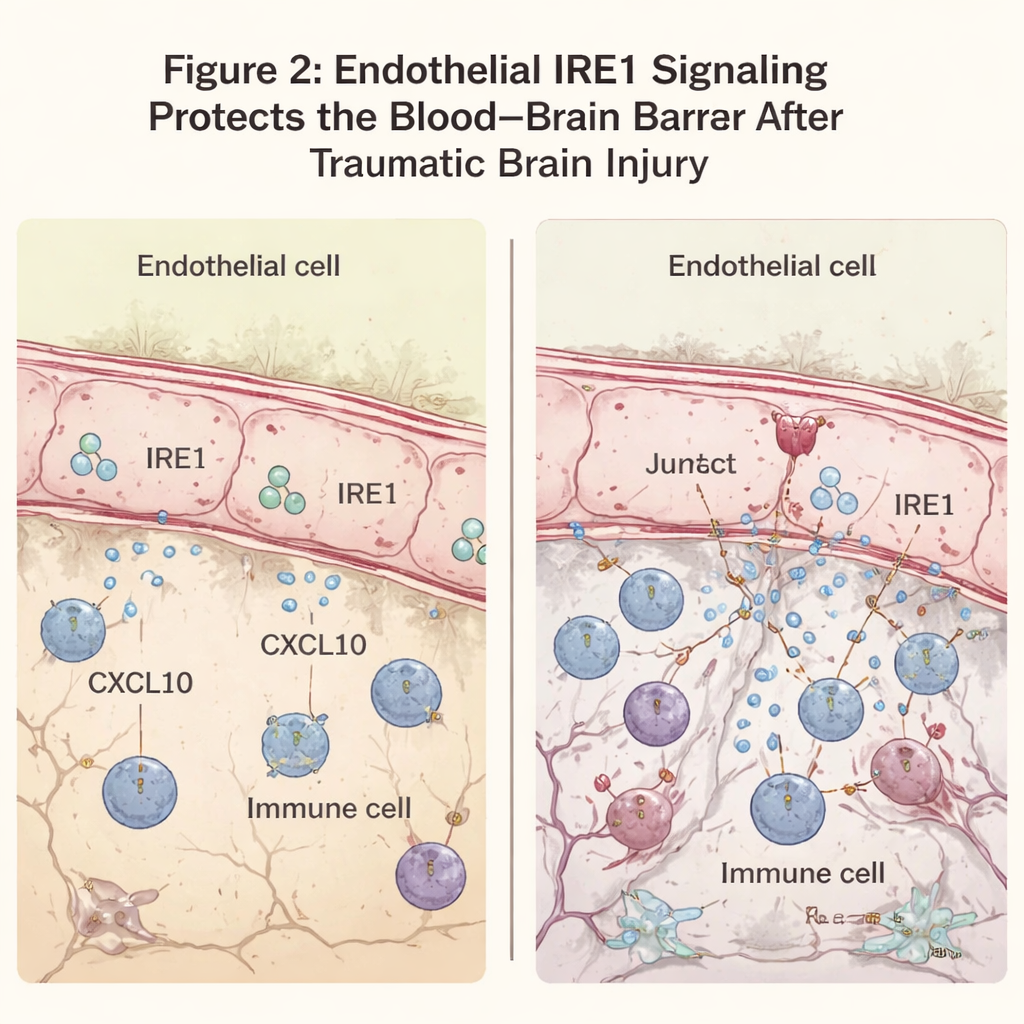
Un fármaco contra el estrés calma la tormenta de señales
Para entender los fundamentos moleculares, el equipo analizó qué genes se activaban tras la lesión. En ratones sin IRE1 endotelial, los genes implicados en respuestas antivirales e inflamatorias aumentaron con fuerza. Entre ellos destacó CXCL10, una quimiocina—una especie de señal molecular—que atrae células inmunitarias y puede debilitar aún más la barrera. CXCL10 se elevó de forma particular en las células endoteliales cerca de la lesión cuando IRE1 faltaba. En células endoteliales cerebrales cultivadas expuestas a un desencadenante inflamatorio, reducir el estrés del retículo endoplásmico con un fármaco llamado TUDCA disminuyó tanto la actividad de IRE1 como la producción de CXCL10. Administrado a ratones lesionados, TUDCA redujo CXCL10 y marcadores de células inmunitarias en la corteza dañada y mejoró el rendimiento motor, lo que sugiere que atenuar esta vía de estrés puede aliviar la lesión secundaria.
Qué significa esto para las personas con traumatismos craneales
En términos sencillos, este trabajo sugiere que el sensor de estrés IRE1 en las células que recubren los vasos sanguíneos cerebrales actúa como un guardián tras una lesión cerebral traumática. Cuando está presente y funciona, ayuda a mantener la barrera hematoencefálica hermética, reduce la liberación de señales químicas que atraen células inmunitarias y limita la propagación de la inflamación y la pérdida neuronal alrededor de la lesión. Cuando está desactivado, la barrera se vuelve más permeable, las células inmunitarias invaden y más tejido cerebral resulta dañado. Dado que las células vasculares son relativamente accesibles a fármacos que circulan por el torrente sanguíneo, dirigir sus respuestas al estrés—con compuestos como TUDCA o terapias futuras más precisas—podría convertirse en una estrategia práctica para reducir el daño a largo plazo tras un traumatismo craneoencefálico.
Cita: Fan, Q., Takarada-Iemata, M., Tanaka, T. et al. Endothelial IRE1 signaling maintains blood–brain barrier integrity and limits neuroinflammation after traumatic brain injury. Cell Death Dis 17, 210 (2026). https://doi.org/10.1038/s41419-026-08461-2
Palabras clave: lesión cerebral traumática, barrera hematoencefálica, células endoteliales, neuroinflamación, estrés celular