Clear Sky Science · es
CD36 aumenta la sensibilidad de las células de cáncer de mama triple negativo a la ferroptosis inducida por palmitato
Por qué la grasa alrededor de los tumores puede ser tanto aliada como enemiga
Los tumores de mama crecen en un tejido que es de forma natural rico en grasa, y se sabe que las células cancerosas “se alimentan” de los ácidos grasos cercanos. Este estudio explora un giro sorprendente: en las condiciones adecuadas, una de las grasas más comunes del organismo, el ácido palmítico, puede en realidad ayudar a matar una forma especialmente agresiva de cáncer de mama al desencadenar un tipo específico de muerte celular. Comprender cómo ocurre esto podría señalar nuevas opciones terapéuticas para pacientes que actualmente tienen pocas alternativas.
Un cáncer de mama difícil de tratar bajo el microscopio
El cáncer de mama triple negativo (TNBC) carece de los receptores hormonales y de factores de crecimiento que apuntan muchos fármacos modernos, lo que lo convierte en uno de los tipos de cáncer de mama más difíciles de tratar. Estos tumores viven en estrecho contacto con adipocitos, que liberan grandes cantidades de ácidos grasos, incluido el ácido palmítico saturado. Los investigadores quisieron saber si el ácido palmítico simplemente alimenta el crecimiento tumoral o si también podría crear una vulnerabilidad que permitiera eliminar las células cancerosas.
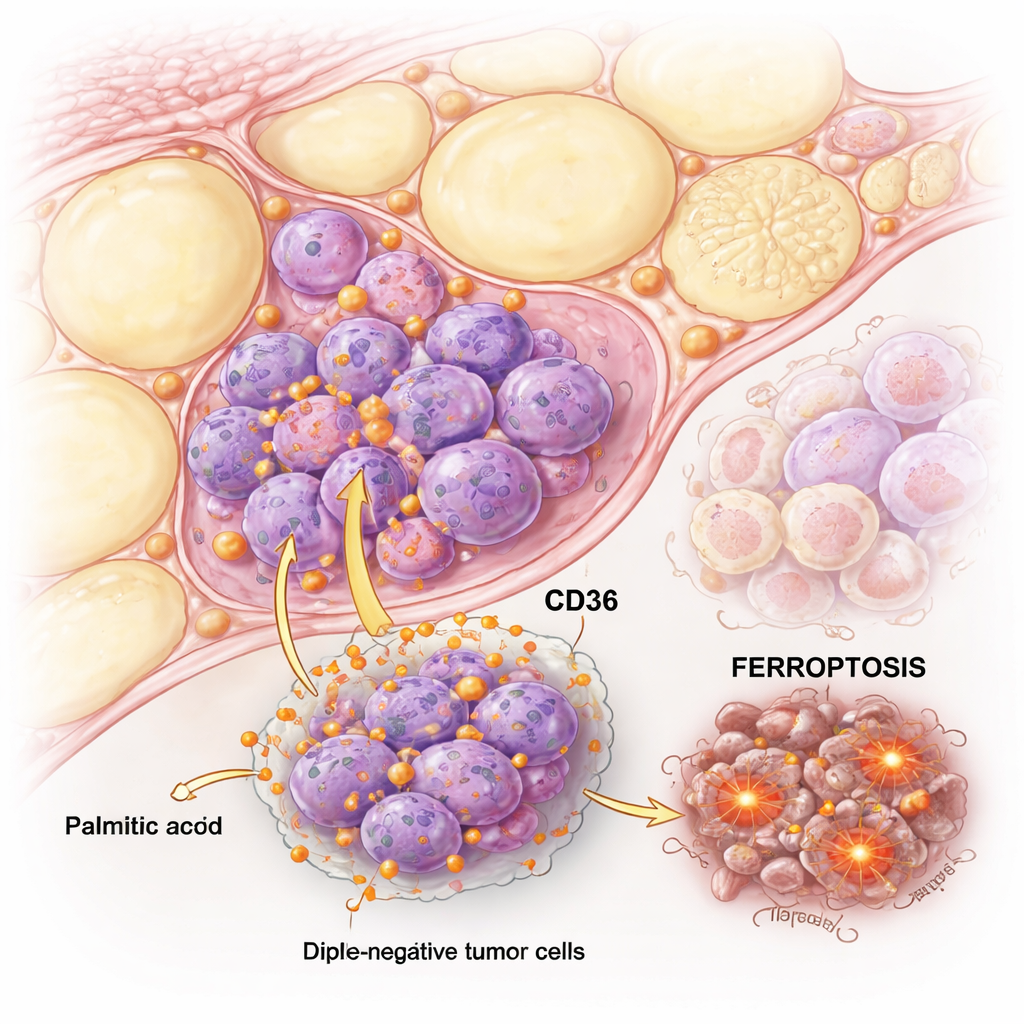
Cuando el ácido palmítico empuja a las células cancerosas al límite
El equipo comparó células de TNBC con células de cáncer de mama “luminal” sensibles a hormonas y las expuso a cantidades crecientes de ácido palmítico. Ambos tipos de células podían dañarse con dosis altas, pero las células TNBC fueron mucho más sensibles. Pruebas detalladas mostraron que en las células luminales el ácido palmítico desencadenaba principalmente apoptosis clásica, una forma ordenada de muerte celular. Sin embargo, en las células TNBC, el ácido palmítico provocó tanto apoptosis como otra vía, menos familiar, llamada ferroptosis, que depende del hierro y de la destrucción de los lípidos de la membrana celular.
Una puerta para ácidos grasos llamada CD36
Para entender por qué las células TNBC reaccionaban de forma tan diferente, los investigadores se centraron en CD36, una proteína en la superficie celular que actúa como una puerta para los ácidos grasos de cadena larga. Las células TNBC presentaban de forma natural mucho más CD36 que las células luminales, y la exposición al ácido palmítico aumentó aún más los niveles de CD36. Esto hizo que las células TNBC absorbieran más ácido palmítico, acumularan más lípidos dañados, produjeran más especies reactivas de oxígeno en sus mitocondrias y acumulasen más hierro libre dentro de la célula: todas señales clave de ferroptosis. Cuando CD36 fue bloqueado con un fármaco, o reducido con herramientas genéticas, la ferroptosis inducida por ácido palmítico disminuyó drásticamente.
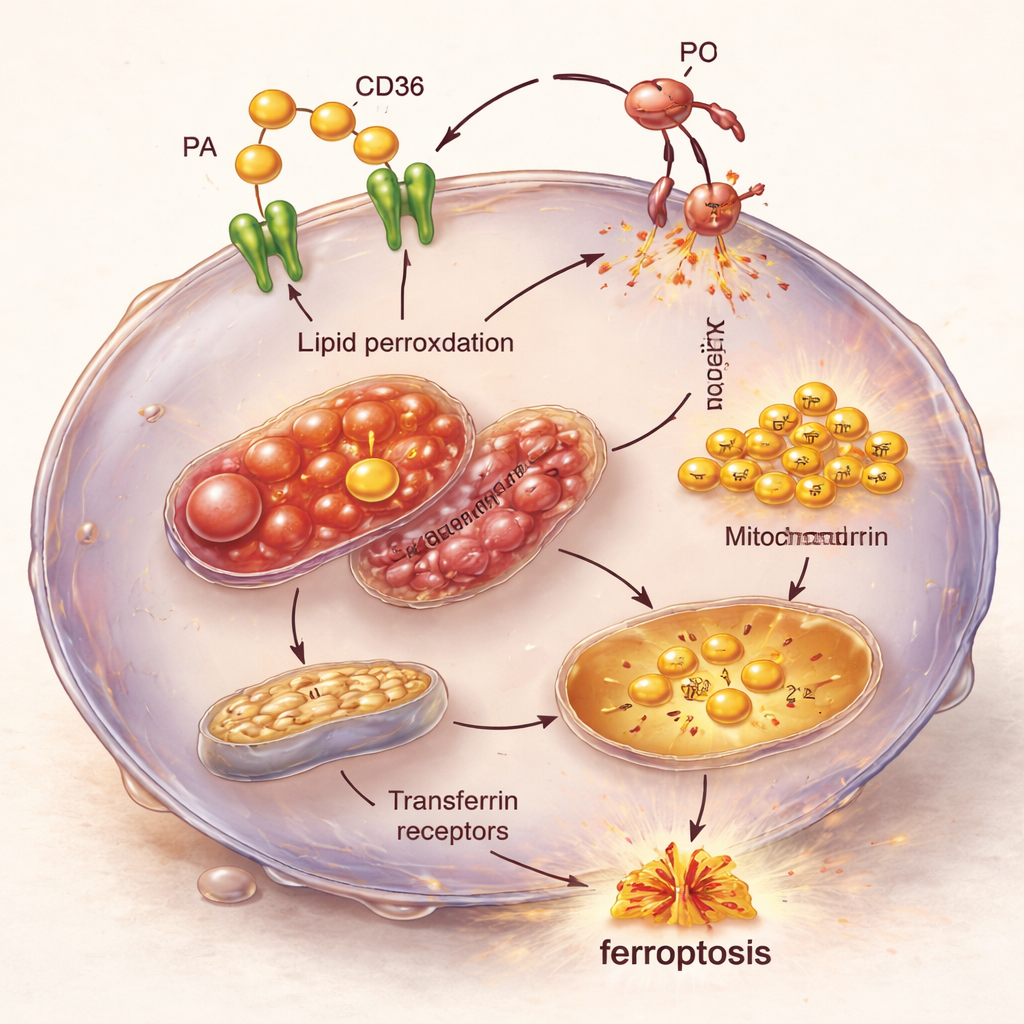
Acercándose a la reacción en cadena dentro de la célula
La microscopía y los análisis de actividad génica revelaron la reacción en cadena interna detrás de esta vulnerabilidad. Las células TNBC sobrecargadas con ácido palmítico y CD36 mostraron mitocondrias hinchadas y estructuralmente dañadas y niveles crecientes de hierro introducido a través de los receptores de transferrina. Al mismo tiempo, se activaron genes que favorecen la ferroptosis, mientras que se redujo la expresión de genes que normalmente protegen contra esta forma de muerte celular. El resultado es una tormenta perfecta: exceso de grasa entrando, más hierro disponible para impulsar reacciones químicas y defensas debilitadas contra el daño lipídico, que en conjunto empujan a las células TNBC hacia la ferroptosis.
¿Qué pacientes podrían beneficiarse más?
El cáncer no es uniforme, ni siquiera dentro del TNBC. Utilizando muestras tumorales cultivadas en ratones y grandes bases de datos de pacientes, los autores encontraron que CD36 era especialmente alto en un subtipo particular de TNBC llamado receptor androgénico luminal (LAR), que ya había sido señalado como más sensible a la ferroptosis. Otros subtipos de TNBC con alta captación de hierro también tendían a mostrar niveles más elevados de CD36. Este patrón sugiere que CD36 podría servir como marcador para identificar a los pacientes cuyos tumores están naturalmente preparados para terapias basadas en la ferroptosis.
Convertir una grasa común en una aliada terapéutica
En términos sencillos, este trabajo muestra que una grasa abundante en la dieta y en el organismo, el ácido palmítico, puede ayudar a matar ciertas células de cáncer de mama triple negativo cuando expresan altos niveles del transportador de grasas CD36. Al provocar sobrecarga lipídica, acumulación de hierro y daño a las membranas celulares, CD36 hace que estas células cancerosas sean más propensas a sufrir ferroptosis, un destino destructivo del que no pueden escapar. Si futuros tratamientos pueden impulsar con seguridad esta vía, o combinarla con fármacos que debiliten aún más las defensas celulares, los clínicos podrían convertir una debilidad metabólica en una forma nueva y más precisa de atacar algunos de los tumores de mama más agresivos.
Cita: Closset, L., Foy, JP., Louadj, L. et al. CD36 enhances sensitivity of triple negative breast cancer cells to palmitate-induced ferroptosis. Cell Death Dis 17, 219 (2026). https://doi.org/10.1038/s41419-026-08460-3
Palabras clave: cáncer de mama triple negativo, ferroptosis, CD36, ácido palmítico, metabolismo tumoral