Clear Sky Science · es
Desubiquitinación mediada por USP30 de la hexocinasa 2 controla el destino metabólico de la glucosa y la progresión tumoral
Cómo las células cancerosas reconfiguran su uso del azúcar
Las células cancerosas son famosas por su “deseo de azúcar”: consumen glucosa de formas inusuales para alimentar un crecimiento rápido. Este estudio descubre un nuevo interruptor, una proteína llamada USP30, que ayuda a las células tumorales a decidir cómo usar la glucosa. Al ajustar otra proteína, la hexocinasa 2 (HK2), USP30 puede empujar a las células cancerosas a quemar más azúcar y crecer más rápido, lo que apunta a un objetivo novedoso para futuros fármacos anticancerígenos. 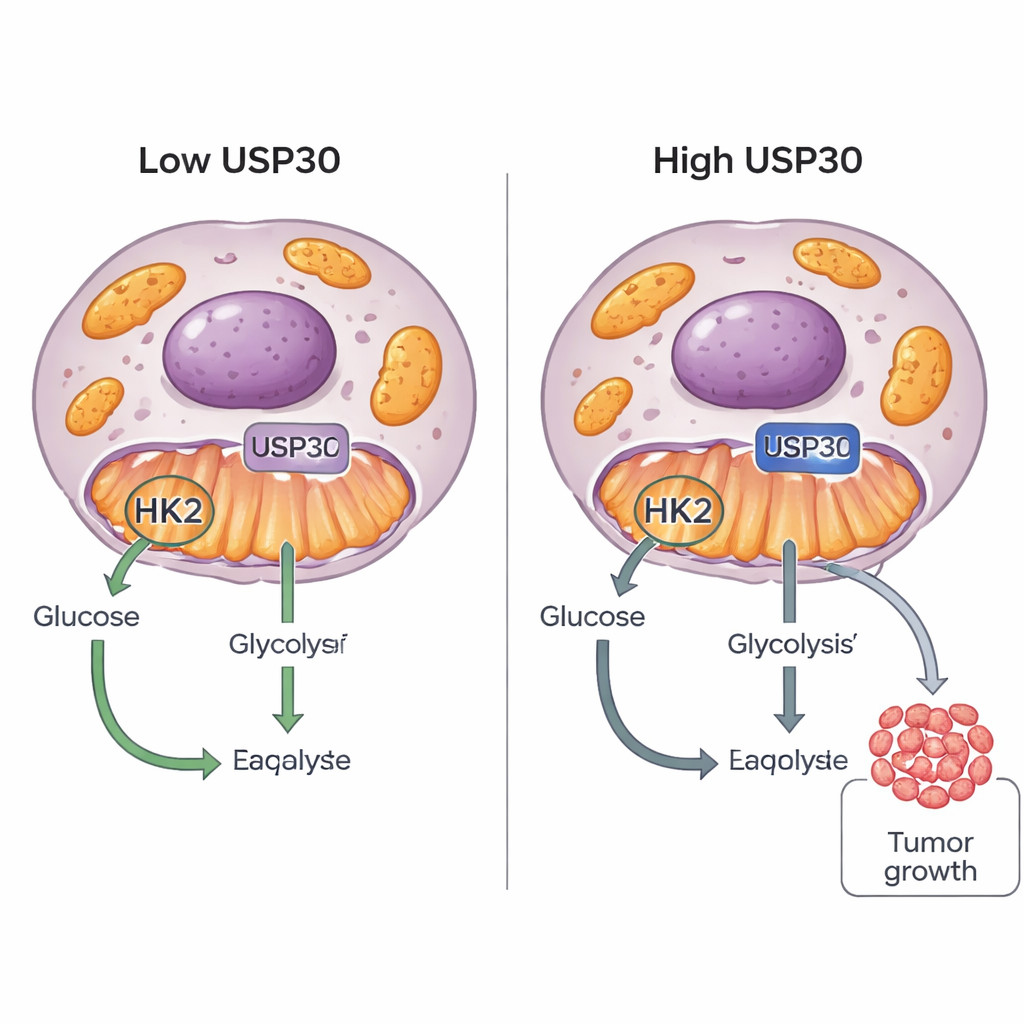
Un estilo de vida hambriento de azúcar dentro de los tumores
La mayoría de las células sanas extraen energía de los nutrientes de forma eficiente, pero muchas células cancerosas favorecen una vía rápida y menos eficiente llamada glucólisis aeróbica, también conocida como efecto Warburg. Captan grandes cantidades de glucosa y la convierten rápidamente en lactato, incluso cuando el oxígeno es abundante. Esta estrategia hace más que producir energía: suministra bloques de construcción para ADN, lípidos y proteínas, ayuda a los tumores a sobrevivir al estrés y puede incluso debilitar las respuestas inmunitarias. En la puerta de entrada a esta vía se encuentra la hexocinasa, una enzima que marca la glucosa entrante con un grupo fosfato, comprometiéndola a una degradación posterior y a la química que sostiene el crecimiento.
Una enzima mitocondrial pasa al primer plano
USP30 es una enzima situada en la superficie externa de las mitocondrias, las centrales energéticas de la célula. Pertenece a una familia de “desubiquitinantes” que eliminan pequeñas etiquetas proteicas llamadas ubiquitinas de otras proteínas, cambiando a menudo su estabilidad, localización o actividad. USP30 ya se conocía por sus funciones en células cerebrales y en el control de la calidad mitocondrial, pero su impacto en el cáncer no quedaba claro. Al sondear grandes bases de datos genéticos de tumores, los investigadores observaron que los tumores con niveles más altos de USP30 tendían a mostrar firmas más intensas de consumo de glucosa y firmas más débiles de oxidación de grasas, lo que sugiere que USP30 podría ayudar a los cánceres a desplazarse hacia un estilo de vida alimentado por azúcar.
Conectando USP30 con los guardianes del azúcar de la célula
Para explorar este vínculo, el equipo redujo o eliminó USP30 en varias líneas celulares cancerosas y midió cómo procesaban la energía. Usando instrumentos que rastrean la producción de ácido y el consumo de oxígeno en tiempo real, encontraron que la pérdida de USP30 redujo drásticamente tanto la glucólisis como la respiración mitocondrial. La producción de lactato y el consumo de glucosa disminuyeron, mostrando que el motor de quema de azúcar de las células se había ralentizado. Una batería de experimentos de espectrometría de masas reveló entonces que USP30 interactúa físicamente con varias enzimas vinculadas al metabolismo de la glucosa, en especial las hexocinas HK1 y HK2. Pruebas posteriores mostraron que esta interacción depende de la actividad catalítica de USP30 y ocurre de forma directa, no solo a través de socios indirectos.
Un potente control molecular sobre la hexocinasa 2
Ahondando más, los investigadores hallaron que USP30 elimina tipos específicos de cadenas de ubiquitina —los llamados enlaces atípicos— de HK1 y HK2. En HK2, esta edición ocurre en un único aminoácido crucial, la lisina 144 (K144). Cuando K144 se muta de modo que ya no puede llevar ubiquitina, HK2 se vuelve más estable, se une con más fuerza a una proteína de canal llamada VDAC1 en las mitocondrias y muestra mayor actividad enzimática. Células diseñadas para portar esta mutación K144 enviaron más HK2 a las mitocondrias, quemaron más glucosa, liberaron más lactato y mostraron un crecimiento y movilidad más rápidos en placas de laboratorio. En ratones, los tumores derivados de células con la HK2 mutante K144 crecieron más grandes y rápido que los que tenían HK2 normal, subrayando la potencia de este diminuto interruptor molecular. 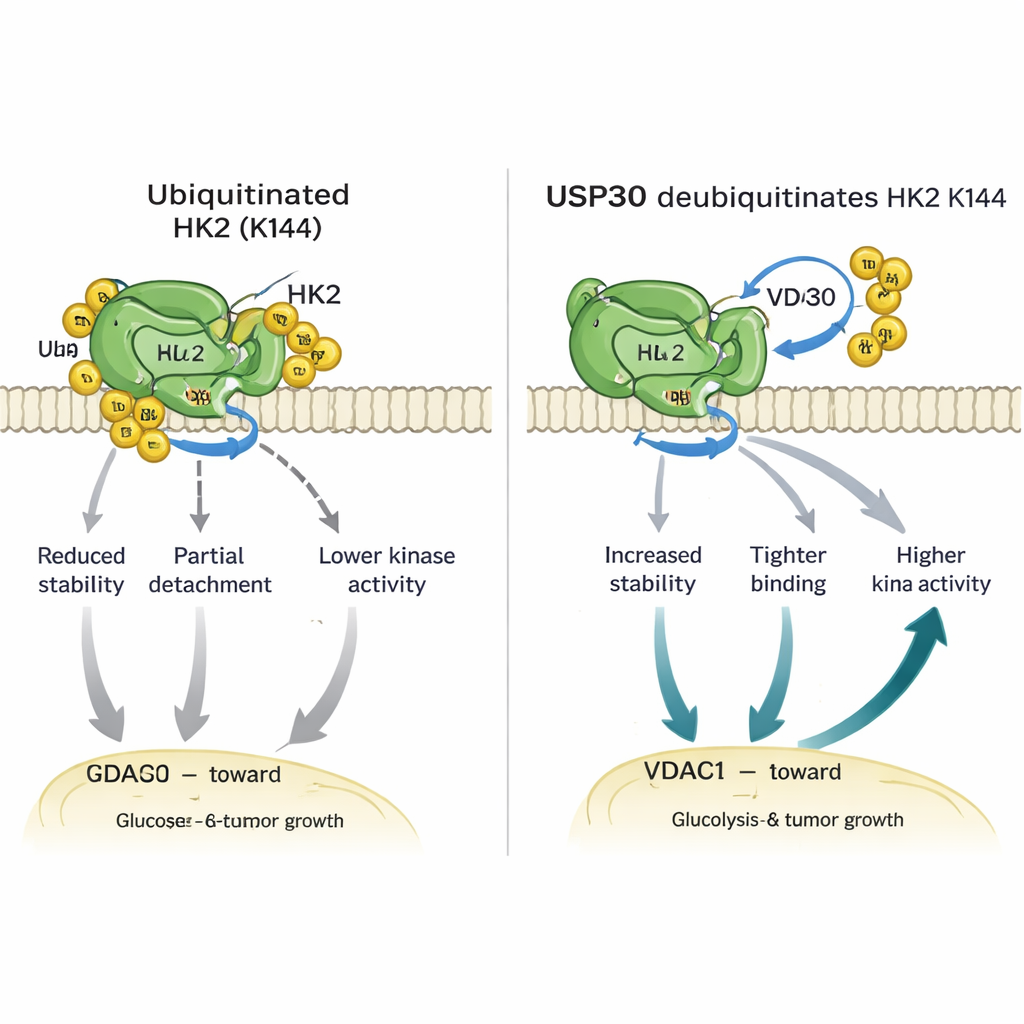
Convertir un interruptor metabólico en una ventaja de crecimiento
Estos resultados trazan una cadena clara de eventos: USP30 se une a HK2, elimina las etiquetas de ubiquitina en K144 y, al hacerlo, mantiene HK2 activo y anclado en las mitocondrias. Esto potencia la glucólisis, alimenta la división y la migración de las células tumorales y, en última instancia, acelera el crecimiento tumoral. Cuando USP30 falta o está inactivo, HK2 se vuelve menos estable y menos efectiva, y las células cancerosas pierden parte de su ventaja metabólica. En términos no técnicos, USP30 actúa como un mecánico que mantiene el motor de azúcar de la célula cancerosa afinado y bien sujeto: quita al mecánico y el motor falla.
Qué significa esto para futuros tratamientos contra el cáncer
Para un público general, la idea clave es que las células cancerosas dependen de controles finamente ajustados sobre cómo consumen azúcar, y USP30 es un mando recién descubierto en ese panel de control. Al estabilizar HK2 en un sitio específico, USP30 ayuda a los tumores a mantener su metabolismo hambriento de glucosa y a crecer con más agresividad. Fármacos que bloqueen USP30, o que interrumpan su unión a HK2 en la lisina 144, podrían debilitar los tumores al dejar sin combustible su motor de azúcar sin dañar necesariamente en la misma medida a las células normales. Este trabajo, por tanto, añade una pieza importante al rompecabezas de cómo el cáncer reconfigura el metabolismo y sugiere un ángulo prometedor para terapias dirigidas.
Cita: Haowei, Z., Li, X., Liao, W. et al. USP30-mediated Deubiquitination of Hexokinase 2 controls the metabolic fate of glucose and tumor progression. Cell Death Dis 17, 225 (2026). https://doi.org/10.1038/s41419-026-08459-w
Palabras clave: metabolismo del cáncer, glucólisis, hexocinasa 2, USP30, efecto Warburg