Clear Sky Science · es
Eliminar selectivamente subunidades de eIF2 en ovocitos provoca apoptosis de ovocitos de ratón en folículos en crecimiento temprano mediante disfunciones mitocondriales y daño en el ADN
Por qué importa la vida de los ovocitos
Las mujeres nacen con todos los ovocitos que tendrán en la vida, almacenados dentro de unas pequeñas estructuras del ovario llamadas folículos. Cuando esos folículos se pierden demasiado rápido, las mujeres pueden desarrollar insuficiencia ovárica prematura (IOP), una condición que conduce a infertilidad temprana y con frecuencia a síntomas similares a la menopausia a una edad temprana. Este estudio en ratones plantea una pregunta básica pero crucial: ¿qué sucede dentro de los ovocitos cuando falla un paso clave en la producción de nuevas proteínas, y cómo puede eso llevar a la pérdida precoz de la fertilidad?
El interruptor que inicia la producción de proteínas
Para mantenerse saludables, los ovocitos deben fabricar constantemente las proteínas correctas en el momento adecuado. Una parte central de este proceso es una máquina molecular formada por tres componentes llamada eIF2, que ayuda a iniciar la producción de proteínas a partir de los mensajes genéticos. Los investigadores desactivaron selectivamente dos subunidades de eIF2, llamadas eIF2α y eIF2β, solo en ovocitos de ratón en las primeras etapas de crecimiento folicular. Cuando faltaba cualquiera de las subunidades, las hembras quedaron completamente infértiles. Sus ovarios eran más pequeños y la progresión normal desde folículos tempranos a folículos maduros y liberadores de ovocitos se detuvo en gran medida, con muchos menos folículos en cada etapa posterior. Con el tiempo, prácticamente todos los folículos se agotaron, imitándose una condición grave de inicio temprano similar a la IOP.
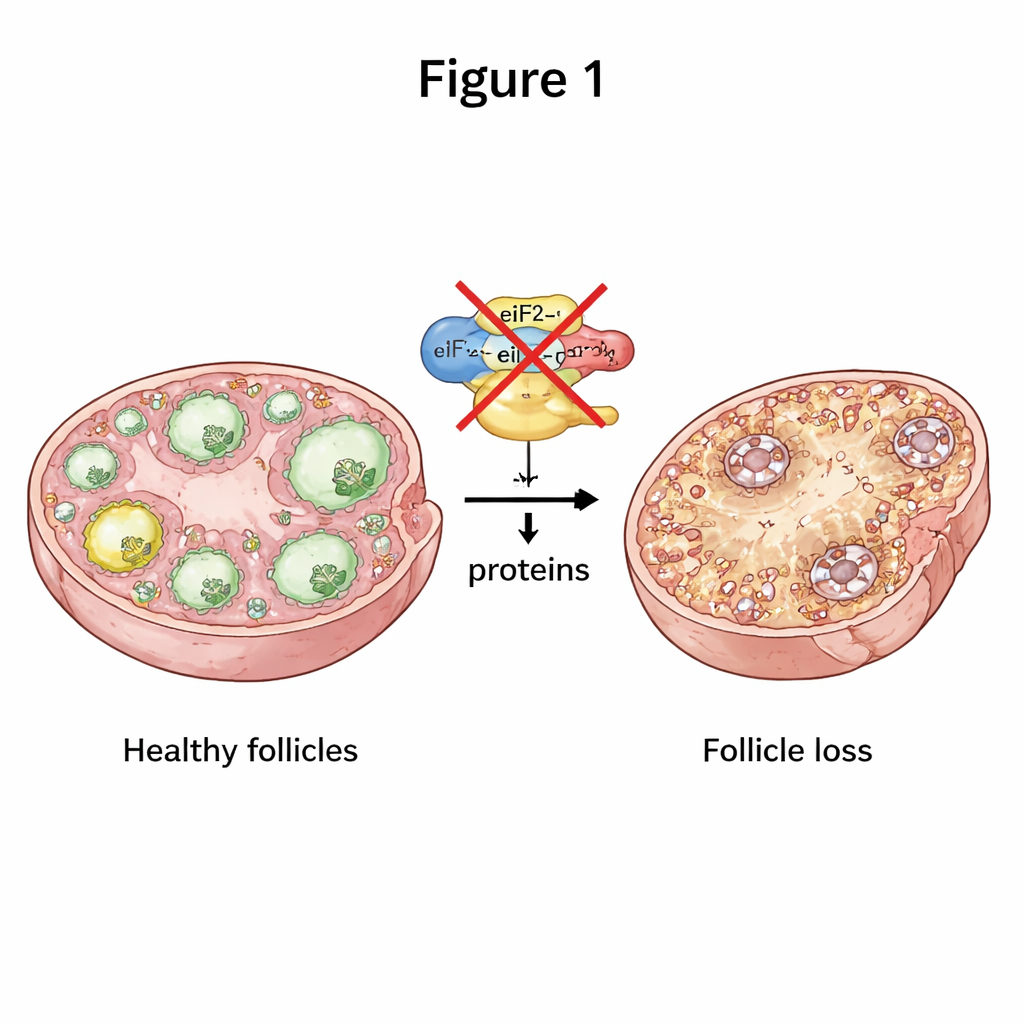
Cuando se rompe la comunicación en el ovario
Los folículos no son solo ovocitos flotando solos; son asociaciones estrechas entre un ovocito y las células “auxiliares” que lo rodean, llamadas células de la granulosa. El equipo encontró que sin eIF2β, los ovocitos producían mucho menos de varias proteínas de señalización cruciales que normalmente apoyan el crecimiento de las células de la granulosa y el suministro de nutrientes. Los puentes físicos entre ovocito y células de la granulosa estaban desorganizados y acortados, y las microvellosidades en la superficie del ovocito parecían atrofiadas y dañadas al observarlas con microscopía electrónica. Las células de la granulosa en esos folículos se dividían menos y morían con más frecuencia. Esta ruptura en la comunicación bidireccional implicó que los folículos no podían crecer correctamente, empujando al ovario hacia la pérdida folicular.
Fallo de energía en las “baterías” del ovocito
Las mitocondrias, a menudo llamadas centrales energéticas de la célula, son especialmente importantes en los ovocitos porque suministran la energía necesaria para el crecimiento y el posterior desarrollo embrionario. En los ovocitos deficientes en eIF2β, la tasa global de nueva síntesis proteica disminuyó y muchas proteínas relacionadas con las mitocondrias se redujeron. Las mitocondrias se volvieron anormalmente largas, se agruparon cerca de la superficie celular y mostraron una menor potencial de membrana, niveles de energía (ATP) más bajos y menos copias de ADN mitocondrial. Al mismo tiempo, las células acumularon altos niveles de especies reactivas de oxígeno (ROS), moléculas oxigenadas agresivas que pueden dañar componentes celulares. En conjunto, estos cambios revelaron un colapso profundo de la dinámica y la función mitocondrial.
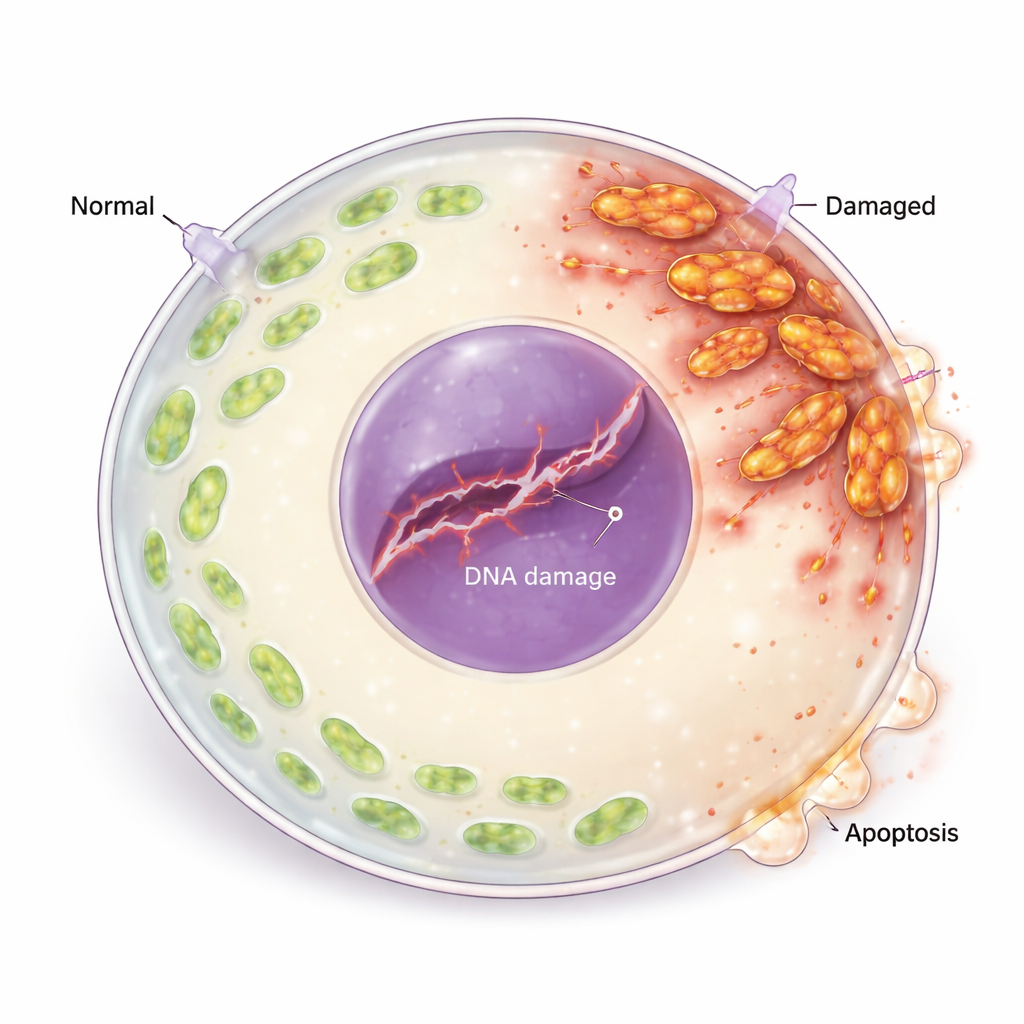
Del estrés oxidativo al daño del ADN y la muerte celular
El exceso de ROS no solo dañó las mitocondrias; también lesionó el material genético del ovocito. Los investigadores observaron marcadores aumentados de rotura de hebras de ADN y activación de la maquinaria de respuesta al daño del ADN de la célula, incluyendo proteínas que detectan y señalan lesiones genéticas. Una proteína clave de reparación estaba reducida, lo que sugiere que el daño no se reparaba de forma eficiente. Aguas abajo, el equilibrio de reguladores de vida y muerte se desplazó: las proteínas pro-muerte aumentaron mientras que las proteínas protectoras anti-muerte disminuyeron, y los ovocitos mostraron signos claros de muerte celular programada (apoptosis). Cuando el equipo trató los ovocitos con un antioxidante (N-acetilcisteína), los niveles de ROS cayeron, los marcadores de daño en el ADN y de apoptosis disminuyeron, y la maduración ovocitaria mejoró, vinculando directamente el estrés oxidativo con la pérdida de ovocitos.
Qué implica para la falla ovárica temprana
Al seguir los eventos desde un único complejo molecular (eIF2) hasta la producción defectuosa de proteínas, el colapso mitocondrial, el estrés oxidativo, el daño en el ADN y, finalmente, la muerte de los ovocitos, este trabajo traza una cadena detallada de acontecimientos que puede destruir la reserva ovárica. El estudio refuerza la idea de que mutaciones en factores que inician la traducción, ya observadas en algunas mujeres con IOP, pueden dañar directamente a los ovocitos a través de esta vía. También apunta a posibles estrategias de ayuda: antioxidantes, moduladores de la respuesta al estrés o tratamientos que protejan los folículos tempranos (como la hormona anti-Mülleriana, que preservó parcialmente folículos dormidos en estos ratones) podrían algún día apoyar la fertilidad en pacientes cuyos ovarios son vulnerables a estreses similares.
Cita: Liu, H., Wang, W., Li, B. et al. Oocyte-specific knockout of eIF2 subunits causes apoptosis of mouse oocytes within the early growing follicles via mitochondrial dysfunctions and DNA damage. Cell Death Dis 17, 196 (2026). https://doi.org/10.1038/s41419-026-08449-y
Palabras clave: insuficiencia ovárica prematura, apoptosis de ovocitos, disfunción mitocondrial, traducción de proteínas, especies reactivas de oxígeno