Clear Sky Science · es
Los hepatocitos diploides resisten la lesión hepática inducida por acetaminofén gracias a la supresión de la señalización JNK
Por qué algunos hígados resisten mejor las sobredosis
El acetaminofén (paracetamol) está presente en incontables botiquines, pero tomar demasiado es una causa principal de insuficiencia hepática aguda. Este estudio plantea una pregunta aparentemente simple con grandes implicaciones: ¿responden todas las células hepáticas de la misma manera ante una sobredosis? Los investigadores muestran que un tipo particular de célula hepática, los hepatocitos diploides, es sorprendentemente buena para sobrevivir y reparar el daño tras una sobredosis de acetaminofén, gracias a la atenuación de una vía interna de estrés.
Dos tipos de células hepáticas, dos destinos distintos
El hígado es inusual porque la mayoría de sus células funcionales (hepatocitos) poseen juegos adicionales de cromosomas, lo que las convierte en poliploides. Una fracción menor permanece diploide, con sólo dos juegos de cromosomas como la mayoría de las células del cuerpo. Los científicos sabían que estos grupos difieren en cómo se dividen y regeneran, pero su papel en la lesión por fármacos no estaba claro. Los autores emplearon ratones criados para que sus hígados estén llenos de células diploides pero funcione normalmente en otros aspectos, y los compararon con ratones típicos cuyos hígados son mayoritariamente poliploides. Ambos grupos recibieron dosis bajas y altas de acetaminofén para observar cómo respondían sus hígados con el tiempo.
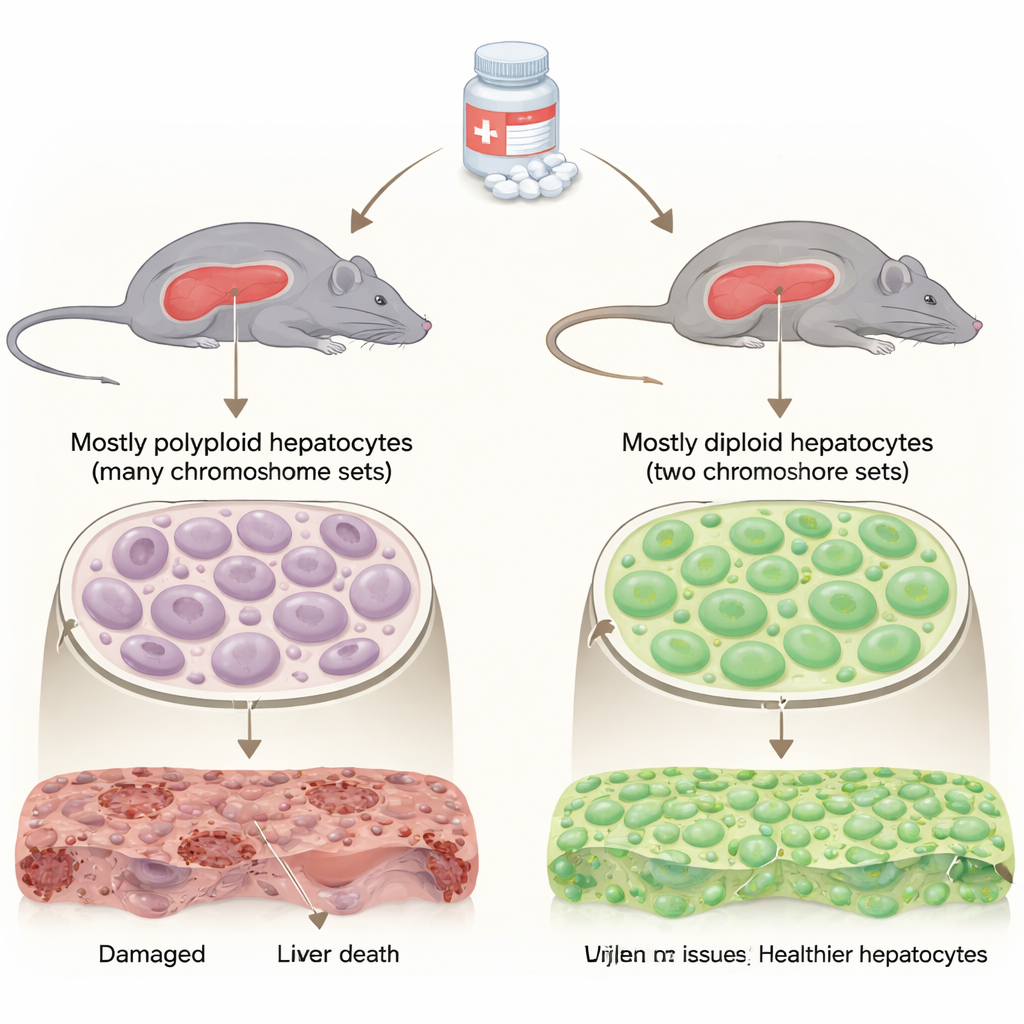
Hígados ricos en diploides sobreviven a las sobredosis y se recuperan más rápido
Cuando los ratones recibieron una sobredosis “regenerativa” de acetaminofén, ambos grupos mostraron daño hepático, pero los ratones ricos en diploides lo soportaron mucho mejor. Presentaron mayor supervivencia, niveles más bajos de enzimas hepáticas en sangre (indicativo de menos daño) y áreas más pequeñas de tejido muerto y ADN fragmentado bajo el microscopio. Incluso con una dosis más severa, “no regenerativa”—que normalmente provoca lesión persistente y muerte—más de la mitad de los ratones ricos en diploides sobrevivieron, frente a menos de uno de cada diez en los controles. A pesar de esta protección, los hígados con predominio de diploides no permanecieron inactivos: activaron proteínas de división celular antes, lo que sugiere que tanto resisten el daño como comienzan la reconstrucción más pronto.
No es el fármaco en sí, sino el cableado del estrés
Una posibilidad obvia era que los hígados ricos en diploides simplemente metabolizaran el acetaminofén de forma diferente. El equipo midió enzimas clave que convierten el fármaco en su subproducto tóxico, los niveles de la molécula protectora glutatión y la cantidad de fármaco ligado a proteínas hepáticas. Todos fueron similares entre los dos tipos de ratones, lo que significa que ambos produjeron y manejaron la misma cantidad de toxina. La diferencia crucial surgió más tarde, en cómo las células respondieron a esa toxina. En los hígados típicos, con predominio de poliploidia, los genes y proteínas implicados en estrés celular, daño del ADN y lesión mitocondrial se activaron fuertemente. En los hígados ricos en diploides, estas respuestas estuvieron atenuadas y se resolvieron antes, mientras que los genes vinculados a la regeneración se encendieron más pronto.
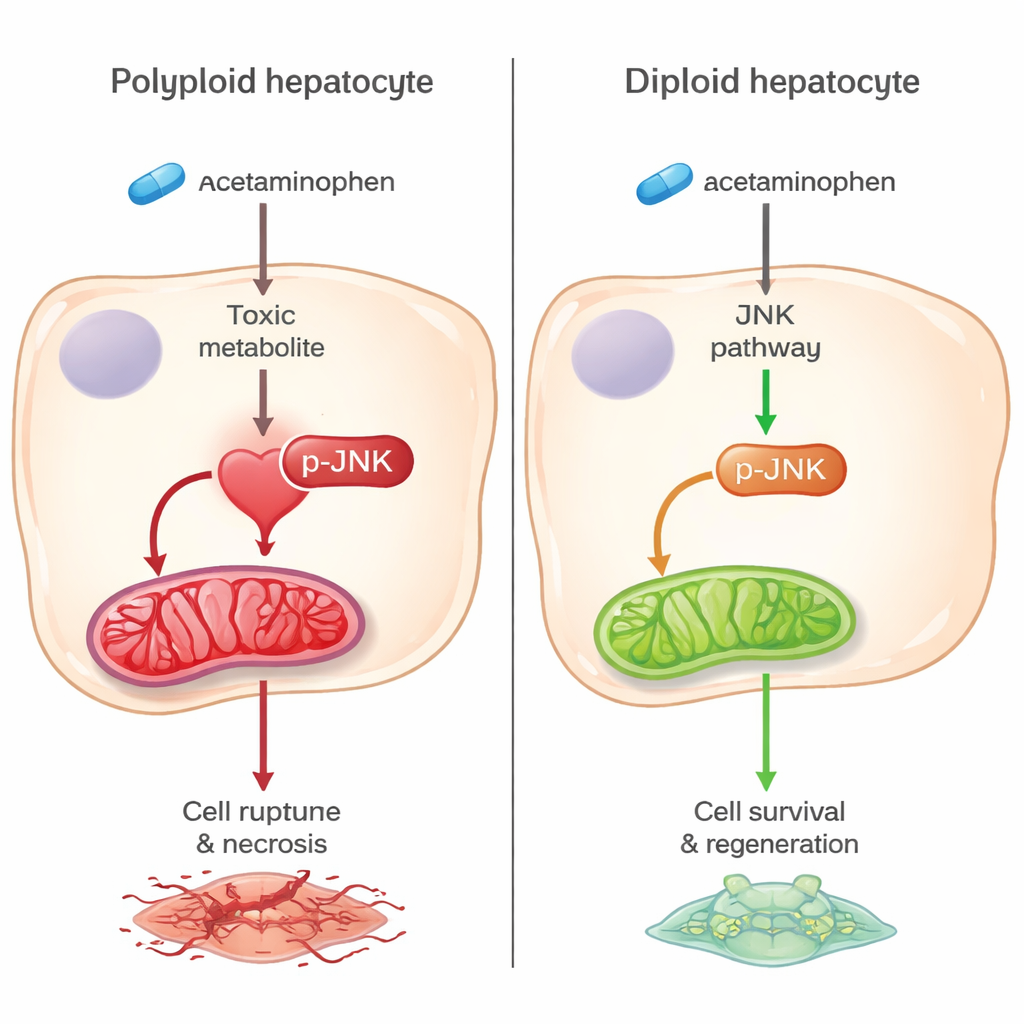
Una vía de muerte más silenciosa protege a las células diploides
El actor central en esta diferencia es una vía de señalización del estrés conocida como vía JNK. En hígados estándar, el subproducto tóxico del acetaminofén activa enzimas ascendentes que ponen en marcha JNK, que luego se desplaza a las mitocondrias —las centrales energéticas de la célula— provocando daño oxidativo y muerte celular. En los hígados ricos en diploides, la activación de estas enzimas ascendentes y de JNK mismo estuvo marcadamente reducida, y mucho menos JNK alcanzó las mitocondrias. Los marcadores de estrés oxidativo y de desintegración mitocondrial también fueron menores, lo que indica que estas centrales se mantuvieron más intactas. Es importante señalar que, cuando los mismos genes fueron eliminados sólo en hígados adultos sin cambiar la ploidía celular, no hubo protección, lo que apunta a la abundancia de células diploides —no a la manipulación genética en sí— como el factor clave.
Por qué el tipo celular importa en la lesión hepática humana
Para ver si este patrón se mantiene de forma más general, los investigadores expusieron a acetaminofén células hepáticas normales de ratón cultivadas en placa. Las células con muchos juegos de cromosomas (altamente poliploides) murieron más fácilmente, mientras que las células diploides y de baja ploidía tuvieron más probabilidades de sobrevivir. En conjunto, los hallazgos respaldan un modelo en el que los hepatocitos diploides son los “primeros intervinientes” del hígado ante una lesión tóxica súbita: moderan una vía principal de muerte, preservan sus mitocondrias e inician la regeneración con rapidez. Las células poliploides aún pueden ser beneficiosas en otros contextos, como la protección frente al cáncer o la adaptación al daño crónico a largo plazo. Pero ante una sobredosis puntual, tener más hepatocitos diploides podría marcar la diferencia entre la recuperación y la insuficiencia hepática.
Cita: Wilson, S.R., Delgado, E.R., Alencastro, F. et al. Diploid hepatocytes resist acetaminophen-induced liver injury through suppressed JNK signaling. Cell Death Dis 17, 203 (2026). https://doi.org/10.1038/s41419-026-08448-z
Palabras clave: sobredosis de acetaminofén, lesión hepática, ploidía de hepatocitos, señalización JNK, regeneración hepática