Clear Sky Science · es
La transglutaminasa 2 agrava la supervivencia del cáncer de ovario al inactivar directamente a GSK3β
Por qué esta investigación importa para la salud de la mujer
El cáncer de ovario es uno de los más mortales en mujeres porque suele detectarse tarde y con frecuencia reaparece incluso tras quimioterapias intensas. Este estudio revela cómo una proteína poco conocida, la transglutaminasa 2 (TGase 2), ayuda a las células de cáncer de ovario a sobrevivir al tratamiento y a diseminarse por el organismo. Al sacar a la luz a este colaborador oculto del cáncer, el trabajo apunta a nuevas formas de hacer más eficaces los fármacos existentes y de frenar o detener la metástasis letal.
Un motor oculto dentro de tumores agresivos
Los médicos han observado durante mucho tiempo que muchos cánceres de ovario desarrollan resistencia a la quimioterapia y se diseminan ampliamente en el abdomen. Un culpable principal es un proceso llamado transición epitelio‑mesénquima (EMT), en el que las células cancerosas aflojan sus conexiones, se vuelven más móviles y actúan más como “viajeras” invasivas que como células de tejido organizado. Los autores muestran que la TGase 2, que se encuentra en niveles muy bajos en el ovario normal pero mucho más alta en tumores ováricos, está fuertemente ligada a este cambio. En un amplio panel de muestras humanas, los niveles de TGase 2 aumentaron de forma sostenida desde tumores en estadio temprano hasta enfermedad avanzada y metastásica, y su abundancia se correspondió estrechamente con la actividad de muchos genes relacionados con la EMT que controlan el movimiento celular, el crecimiento y la formación de vasos sanguíneos. 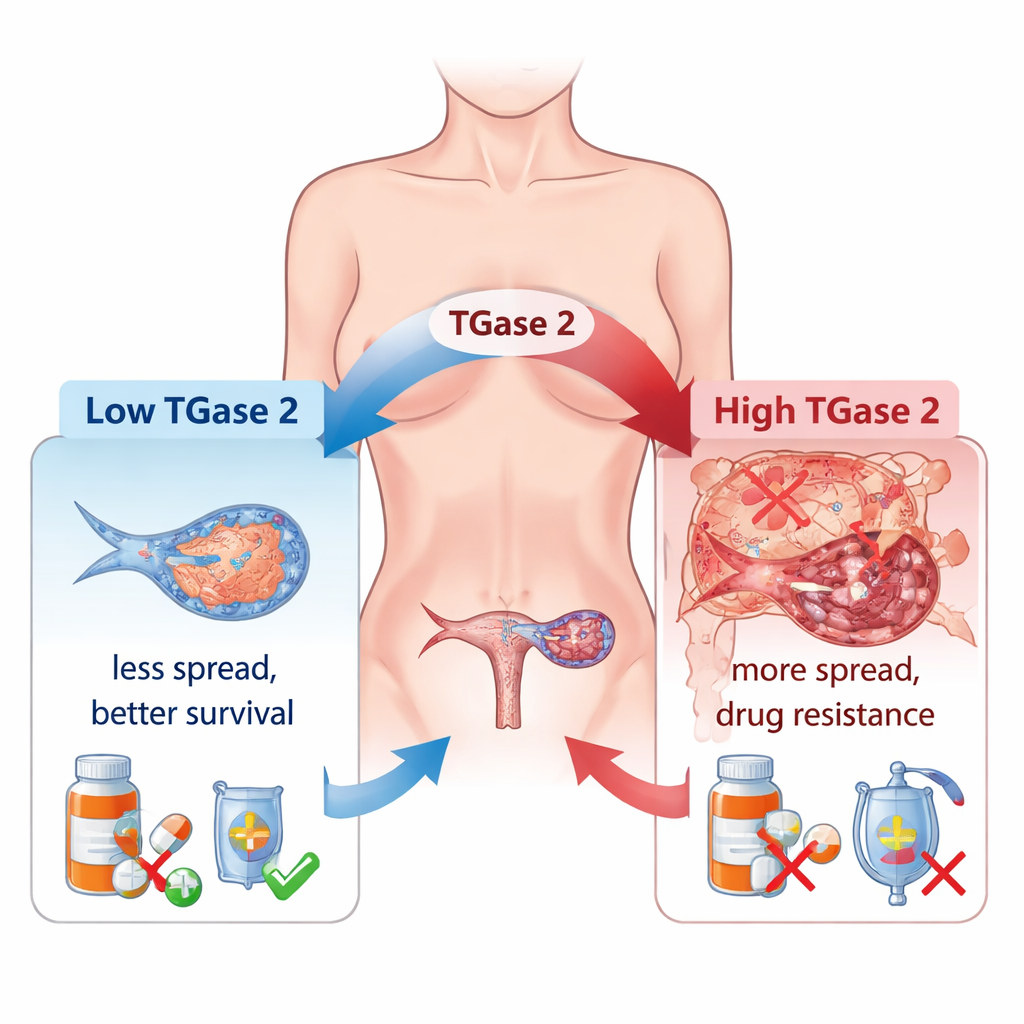
Cómo TGase 2 desactiva un interruptor de seguridad clave
Para entender qué hace realmente la TGase 2 dentro de las células cancerosas, los investigadores se centraron en su relación con otra proteína, GSK3β. En condiciones sanas, GSK3β actúa como un freno a la invasión: mantiene bajos los niveles de una molécula de señalización llamada β‑catenina, lo que a su vez restringe los genes que impulsan la EMT. El equipo descubrió que la TGase 2 se une físicamente a GSK3β y tanto debilita su actividad como facilita su envío a destrucción a través del sistema de reciclaje celular, una vía llamada autofagia. Cuando la TGase 2 era abundante, las células de cáncer de ovario migraban con mayor facilidad y mostraban niveles más altos de marcadores clásicos de EMT como la fibronectina, la vimentina y la β‑catenina. Al reducir la TGase 2 mediante herramientas genéticas, estas características invasivas disminuyeron y la señalización de β‑catenina se atenuó, lo que demuestra que la TGase 2 desactiva un interruptor de seguridad crucial contra la metástasis.
De las células cancerosas a animales vivos
El equipo preguntó luego si bloquear la TGase 2 podría realmente frenar el cáncer en animales. Diseñaron células de cáncer de ovario carentes del gen TGase 2 y las implantaron en ratones. En comparación con los ratones que recibieron células cancerosas normales, los animales con células deficientes en TGase 2 desarrollaron menores cargas tumorales y vivieron más tiempo. En un modelo separado que imita la diseminación del cáncer por el torrente sanguíneo, los ratones inyectados con células deficientes en TGase 2 desarrollaron muchas menos y más pequeñas metástasis pulmonares. De forma importante, estos depósitos metastásicos mostraron niveles más altos de GSK3β, lo que encaja con la idea de que eliminar la TGase 2 restaura el freno natural a la invasión y ayuda a contener la enfermedad.
Convertir una pista de laboratorio en una estrategia farmacológica
Dado que eliminar un gen no es práctico en pacientes, los autores probaron una pequeña molécula llamada estreptonigrina, conocida previamente por unirse al mismo extremo de la TGase 2 que ésta usa para captar otras proteínas. Encontraron que la estreptonigrina podía interrumpir la interacción TGase 2–GSK3β en las células, reducir su colocalización y limitar la migración celular cancerosa. En modelos murinos de cáncer de ovario, el tratamiento oral con estreptonigrina ralentizó el crecimiento tumoral, redujo las lesiones metastásicas y prolongó la supervivencia. De forma más llamativa, cuando la estreptonigrina se combinó con quimioterapias estándar como cisplatino o paclitaxel, los ratones vivieron semanas más que con la quimioterapia sola. La quimioterapia por sí misma tendía a elevar los niveles de TGase 2 y a reducir GSK3β, empujando indirectamente a las células hacia la EMT, pero añadir el inhibidor de TGase 2 revirtió esta tendencia y limitó la nueva movilidad de las células. 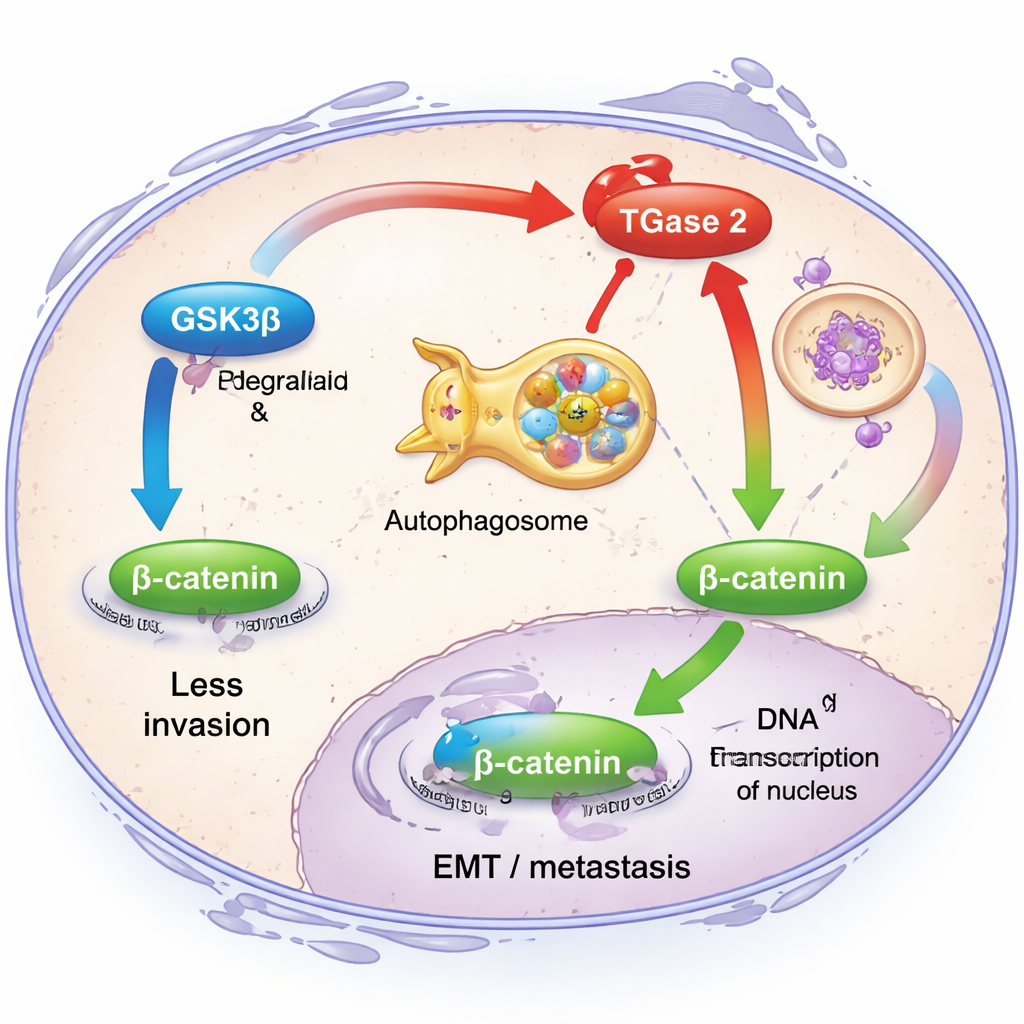
Qué podría significar esto para tratamientos futuros
Para un público no especializado, la idea principal es que las células de cáncer de ovario explotan la TGase 2 para apagar un freno antimetástasis incorporado y para capear la tormenta de la quimioterapia. Al inactivar directamente a GSK3β y estabilizar la β‑catenina, la TGase 2 ayuda a los tumores a volverse más invasivos y resistentes a los fármacos. Este trabajo sugiere que fármacos dirigidos a la región N‑terminal de la TGase 2 —como la estreptonigrina o compuestos futuros más seguros modelados a partir de ella— podrían mejorar la eficacia de las quimioterapias existentes, reducir la probabilidad de recaída y mejorar la supervivencia. En términos sencillos, dirigir la TGase 2 puede cerrar una “ruta de escape” del cáncer, manteniendo los tumores ováricos más sensibles al tratamiento y menos capaces de diseminarse.
Cita: Lee, H., Kang, J.H., Kim, H.J. et al. Transglutaminase 2 exacerbates ovarian cancer survival by directly inactivating GSK3β. Cell Death Dis 17, 199 (2026). https://doi.org/10.1038/s41419-026-08447-0
Palabras clave: cáncer de ovario, resistencia a fármacos, metástasis, transición epitelio‑mesénquima, terapia dirigida