Clear Sky Science · es
Inhibición de la internalización del receptor de células B (BCR) inducida por autoantígenos como estrategia terapéutica en el linfoma difuso de células B grandes (LDCBG)
Por qué esto importa para los pacientes
El linfoma difuso de células B grandes (LDCBG) es el cáncer hematológico de crecimiento rápido más frecuente en adultos, y muchos pacientes todavía recaen tras la quimio‑inmunoterapia estándar. Este estudio explora una debilidad sorprendente en un gran subconjunto de estos tumores: su dependencia de una “antena” en la superficie celular llamada receptor de células B (BCR). Al demostrar que bloquear la manera en que esta antena es internalizada puede mermar la supervivencia de las células cancerosas, el trabajo abre la puerta a reproponer fármacos antieméticos y antipsicóticos de larga trayectoria como agentes complementarios dirigidos contra el linfoma.
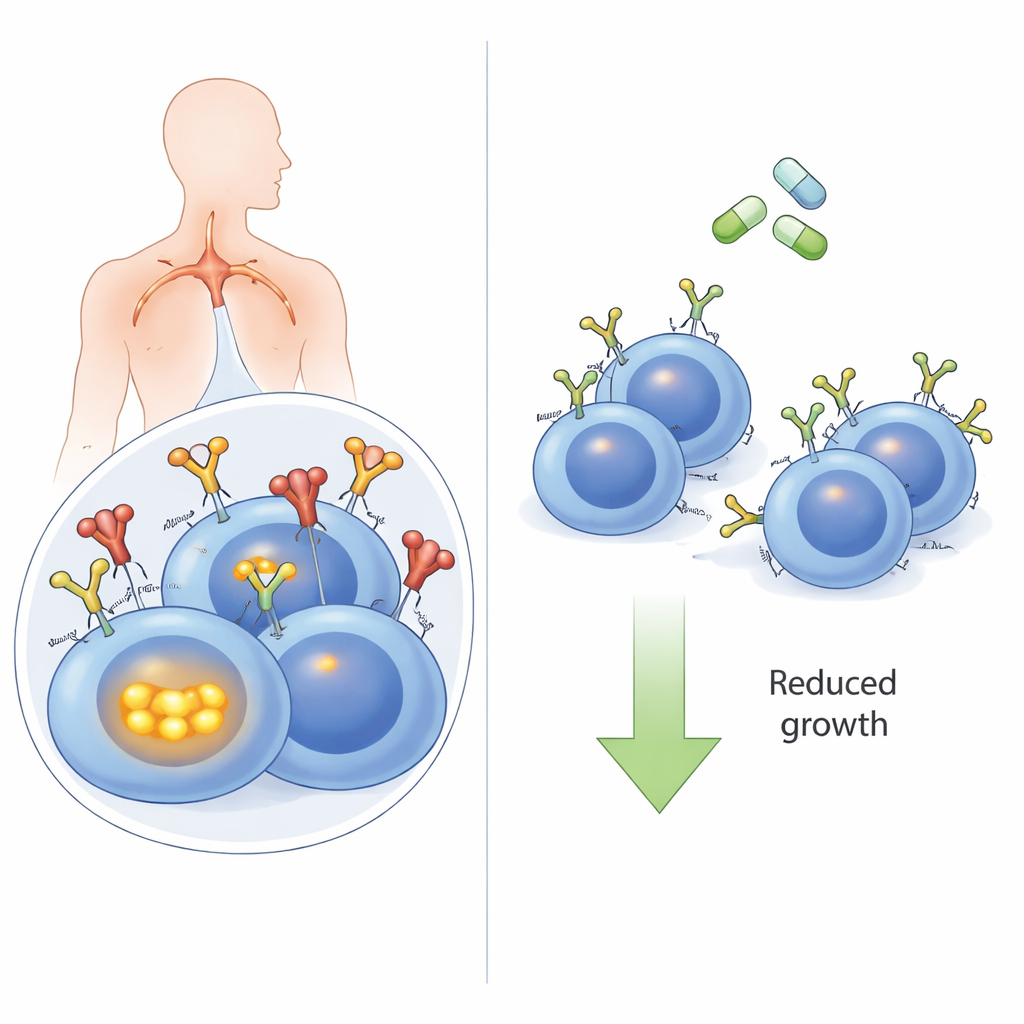
La antena de la célula cancerosa
Las células B, un tipo de glóbulo blanco, utilizan el receptor de células B en su superficie para reconocer amenazas. En muchos LDCBG, especialmente en el subtipo de alto riesgo “célula B activada” (ABC), ese mismo receptor es secuestrado para enviar mensajes constantes de “mantente vivo y crece”. A menudo, estos BCR reconocen moléculas propias del organismo (autoantígenos), que actúan como un timbre atascado. Cuando los autoantígenos se unen, el BCR hace más que señalizar en la superficie: es arrastrado hacia el interior y se integra en un complejo proteico interno con sensores llamados TLR9 y MYD88. Este supercomplejo activa NFκB, una potente vía de señalización que promueve el crecimiento. Hasta ahora no quedaba claro si este viaje hacia el interior del receptor era realmente necesario para las señales que impulsan el cáncer.
Reconfigurar la antena para probar sus límites
Para responder a esa pregunta, los investigadores usaron edición genética CRISPR para cambiar con precisión las “puntas” del BCR en líneas celulares de linfoma. Sustituyeron las regiones de reconocimiento natural autorreactivas por versiones que reconocen ovalbúmina, una proteína de huevo inocua usada como herramienta de laboratorio. Estos receptores modificados dejaron de captar sus autoantígenos habituales, pero todavía podían activarse de forma controlada con ovalbúmina añadida. En células de linfoma tipo ABC que normalmente dependen de la unión a autoantígenos, este cambio redujo drásticamente la actividad de muchas quinasa clave de señalización y atenuó los genes dependientes de NFκB. Las células crecieron más lentamente, a pesar de tener en realidad más BCR en su superficie, lo que demuestra que el compromiso continuo por autoantígenos y la consiguiente señalización interna son críticos para su supervivencia.
Internalización de receptores: un paso crucial
El equipo examinó luego directamente qué ocurre con el BCR después de encontrar su antígeno. En sus modelos ingenierizados, tanto los desencadenantes basados en anticuerpos como la ovalbúmina provocaron que el receptor desapareciera de la superficie celular en minutos, confirmando una rápida internalización. Esto sucedió no solo cuando el antígeno flotaba fuera de la célula, sino también cuando se exhibía de forma artificial en la membrana de la misma célula, imitando ciertas situaciones tumorales reales. Bloquear este tráfico hacia el interior de forma genética, usando una forma dominante negativa de una proteína llamada dinamina‑2, esencial para la endocitosis mediada por clatrina, mantuvo el BCR en la superficie, redujo los complejos internos BCR–TLR9–NFκB, disminuyó los genes diana de NFκB y ralentizó el crecimiento celular. Curiosamente, cuando se bloqueó la endocitosis, algunas señales de “fondo” del BCR en la superficie aumentaron, lo que sugiere que las células cancerosas pueden intentar compensar activando un modo de señalización tónica más débil.
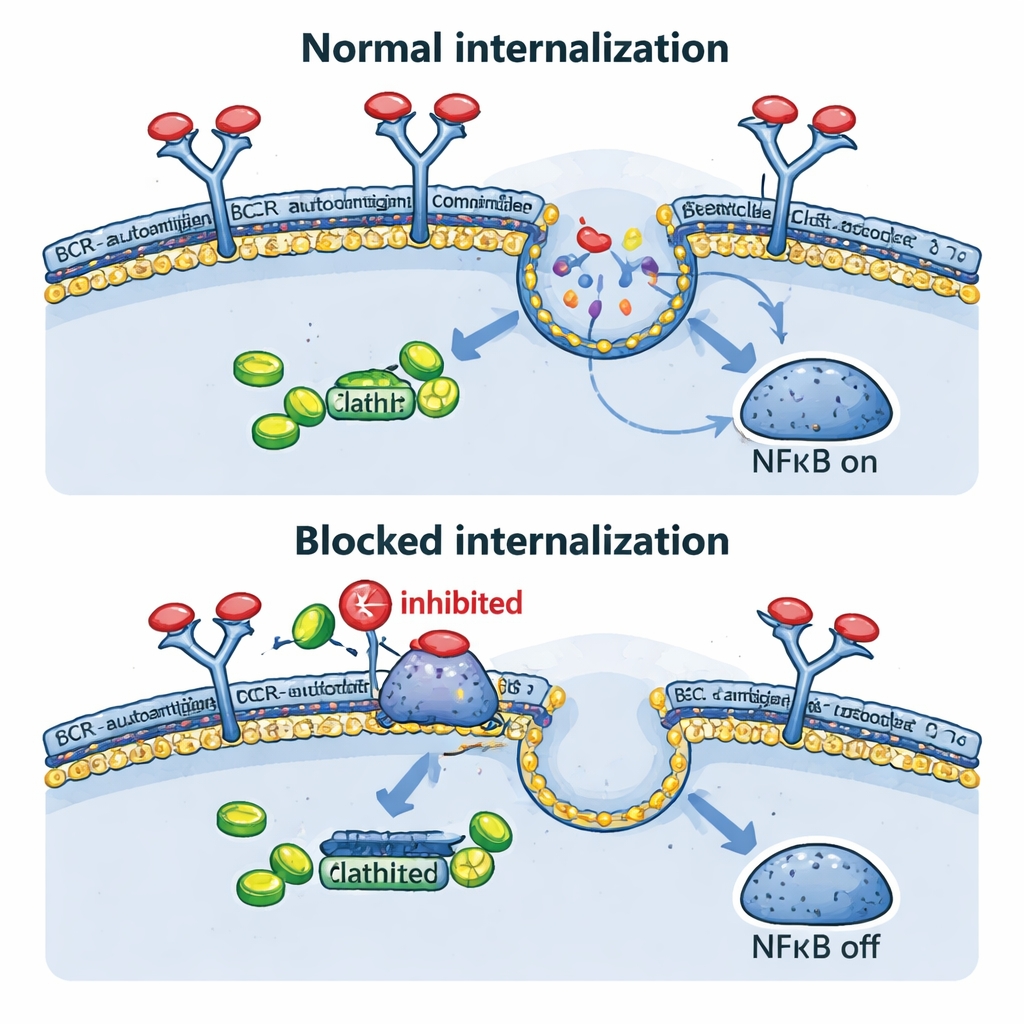
Fármacos antiguos, nuevas estrategias
Dado que desarrollar fármacos nuevos es lento y costoso, los autores preguntaron si medicinas existentes que bloquean la endocitosis podían imitar los experimentos genéticos. Las fenotiazinas, una familia de antipsicóticos y antieméticos, son conocidas por inhibir la dinamina‑2 y la captación dependiente de clatrina de receptores. En células de linfoma, compuestos como el proclorperazín y la clorpromazina aumentaron los niveles de BCR en la superficie y redujeron de forma marcada la internalización inducida por antígeno. Esto condujo a una menor actividad génica impulsada por NFκB y a una reducción de la viabilidad de las células LDCBG tipo ABC, particularmente en aquellas con componentes de BCR intactos. En ratones portadores de injertos de linfoma humano, el proclorperazín a dosis clínicamente alcanzables desaceleró significativamente el crecimiento tumoral. Además, la combinación de fenotiazinas con fármacos que bloquean otras enzimas enlazadas al BCR, como SYK y PI3Kδ, produjo efectos citotóxicos mayores que cualquiera de los tratamientos por separado.
Qué podría significar para el tratamiento
En conjunto, el estudio demuestra que, para un subgrupo significativo de LDCBG, las señales que impulsan el cáncer no provienen simplemente de receptores en la superficie celular; dependen de manera crítica de la internalización del complejo BCR–antígeno a través de una vía de endocitosis específica. Interrumpir este paso —ya sea mediante maniobras genéticas o con fármacos fenotiazínicos— debilita la señalización NFκB y perjudica la supervivencia de las células tumorales, al tiempo que potencialmente sensibiliza a las células frente a inhibidores ya existentes de la vía del BCR. Dado que las fenotiazinas ya tienen esquemas posológicos y perfiles de seguridad bien conocidos como antieméticos, este trabajo ofrece un plan realista para ensayos clínicos que las evalúen, solas o en combinación, en pacientes cuyos linfomas muestran actividad de BCR dependiente de autoantígeno.
Cita: Górniak, P., Polak, A., Rams, A. et al. Inhibition of autoantigen-induced B-cell receptor (BCR) internalization as a therapeutic strategy in diffuse large B cell lymphoma (DLBCL). Cell Death Dis 17, 216 (2026). https://doi.org/10.1038/s41419-026-08446-1
Palabras clave: linfoma difuso de células B grandes, receptor de células B, endocitosis, fenotiazinas, señalización NFkB