Clear Sky Science · es
La metilación reversible de arginina regula la actividad mitocondrial de IDH2: control coordinado por CARM1 y KDM3A/4A
Ajuste fino de las centrales energéticas de la célula
Las mitocondrias, a menudo llamadas las centrales energéticas de nuestras células, hacen mucho más que producir energía. Se ajustan constantemente en cómo metabolizan el combustible para satisfacer las necesidades del organismo, y cuando esto falla puede contribuir a enfermedades como la diabetes, la insuficiencia cardíaca y el cáncer. Este estudio descubre un “atenuador” oculto dentro de las mitocondrias: una pequeña etiqueta química en un único bloque de construcción de una enzima clave, IDH2, que contribuye a decidir si las mitocondrias funcionan a baja marcha o aumentan su producción energética.
Una etiqueta diminuta con grandes consecuencias
Las proteínas de nuestras células no son estáticas; con frecuencia se modifican con pequeños grupos químicos que alteran su comportamiento. Aunque muchas de estas modificaciones en el núcleo celular y el citosol están bien caracterizadas, las que ocurren dentro de las mitocondrias están menos exploradas. Los autores se centraron en un tipo particular de etiqueta denominada metilación de arginina y preguntaron si podría controlar cómo funcionan las enzimas mitocondriales. Se fijaron en una enzima llamada IDH2, una pieza clave del ciclo del ácido tricarboxílico (TCA), que ayuda a convertir nutrientes tanto en energía como en bloques metabólicos importantes. Con herramientas bioquímicas y espectrometría de masas, encontraron que IDH2 lleva una marca de metilo específica en un aminoácido, la arginina 188, y que dicha marca la coloca una enzima llamada CARM1 que, sorprendentemente, opera dentro de las mitocondrias.
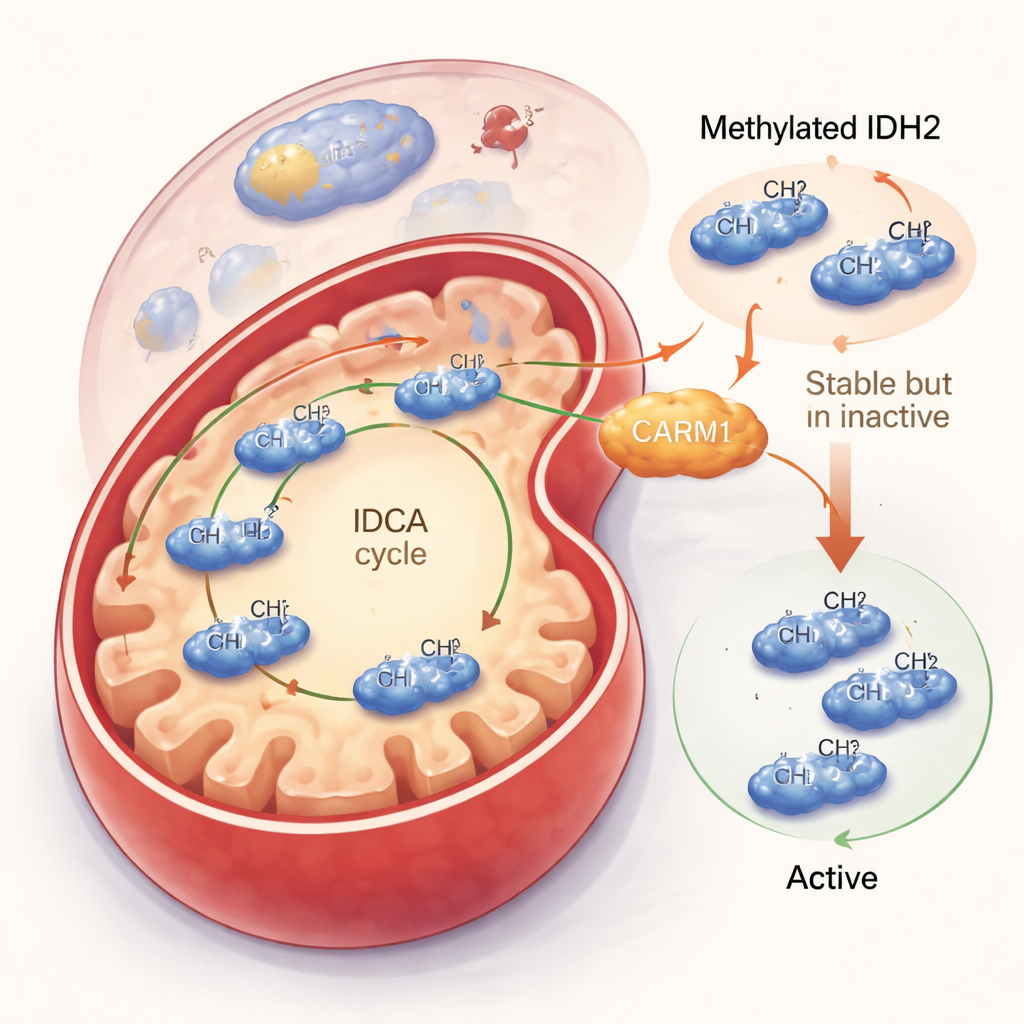
Reducir la actividad de IDH2 pero aumentar su durabilidad
El equipo se preguntó entonces qué hace realmente esta etiqueta de metilo. Cuando CARM1 estaba activo y podía metilar IDH2, la proteína IDH2 se volvía más estable y permanecía más tiempo en la célula. Pero esta ventaja aparente tenía un coste: la IDH2 metilada era menos activa. En experimentos celulares y con proteína purificada, la IDH2 metilada producía menos de su producto principal, alfa-cetoglutarato, y generaba menos de la molécula protectora NADPH. En contraste, una versión de IDH2 que no podía ser metilada en la arginina 188 formaba con mayor facilidad la estructura dimerizada activa, trabajaba más rápido y aumentaba tanto los niveles de alfa-cetoglutarato como de NADPH. Aunque había menos de esta IDH2 no metilada en total, cada molécula realizaba más trabajo, conduciendo a un incremento neto en la producción mitocondrial.
Un interruptor reversible con dos borradores
De forma crucial, esta marca de metilo no es permanente. Los investigadores mostraron que dos enzimas conocidas normalmente por eliminar otro tipo de etiqueta, las desmetilasas de lisina KDM3A y KDM4A, también pueden borrar la metilación de arginina en IDH2. Cuando estas desmetilasas estaban presentes, la arginina metilada en la posición 188 perdía sus grupos químicos adicionales, IDH2 se volvía menos estable pero más activa, y aumentaba su forma dimerizada. Las células con mayor actividad de KDM3A o KDM4A mostraron mayor potencial de membrana mitocondrial y consumieron más oxígeno, señales de que sus mitocondrias funcionaban a mayor intensidad en metabolismo oxidativo. Cuando estas enzimas se reducían, ocurría lo contrario: la actividad de IDH2 caía y el rendimiento mitocondrial se deterioraba, subrayando que se trata de un sistema de control reversible y no de un cambio unidireccional.
Vinculando metabolismo y enfermedad
Dado que IDH2 se ha relacionado con el cáncer y otros trastornos, los autores examinaron cómo podría importar este interruptor de metilación en contextos con rasgos de enfermedad. En varias líneas celulares normales y cancerosas, observaron que niveles más altos de proteína IDH2 a menudo iban acompañados de mayor metilación y, sorprendentemente, menor actividad enzimática, lo que sugiere que “más proteína” no siempre equivale a “más función”. En conjuntos de datos de cáncer de mama, los pacientes con mayores niveles de proteína IDH2 tendieron a presentar peor supervivencia, aunque la actividad del gen IDH2 no se correlacionó con el resultado. Los resultados apoyan un modelo en el que la metilación impulsada por CARM1 ralentiza el ciclo TCA y empuja a las células hacia vías alternativas de uso de nutrientes favorecidas por el cáncer, mientras que desmetilasas como KDM3A y KDM4A pueden reorientar a las células hacia una producción de energía más eficiente.
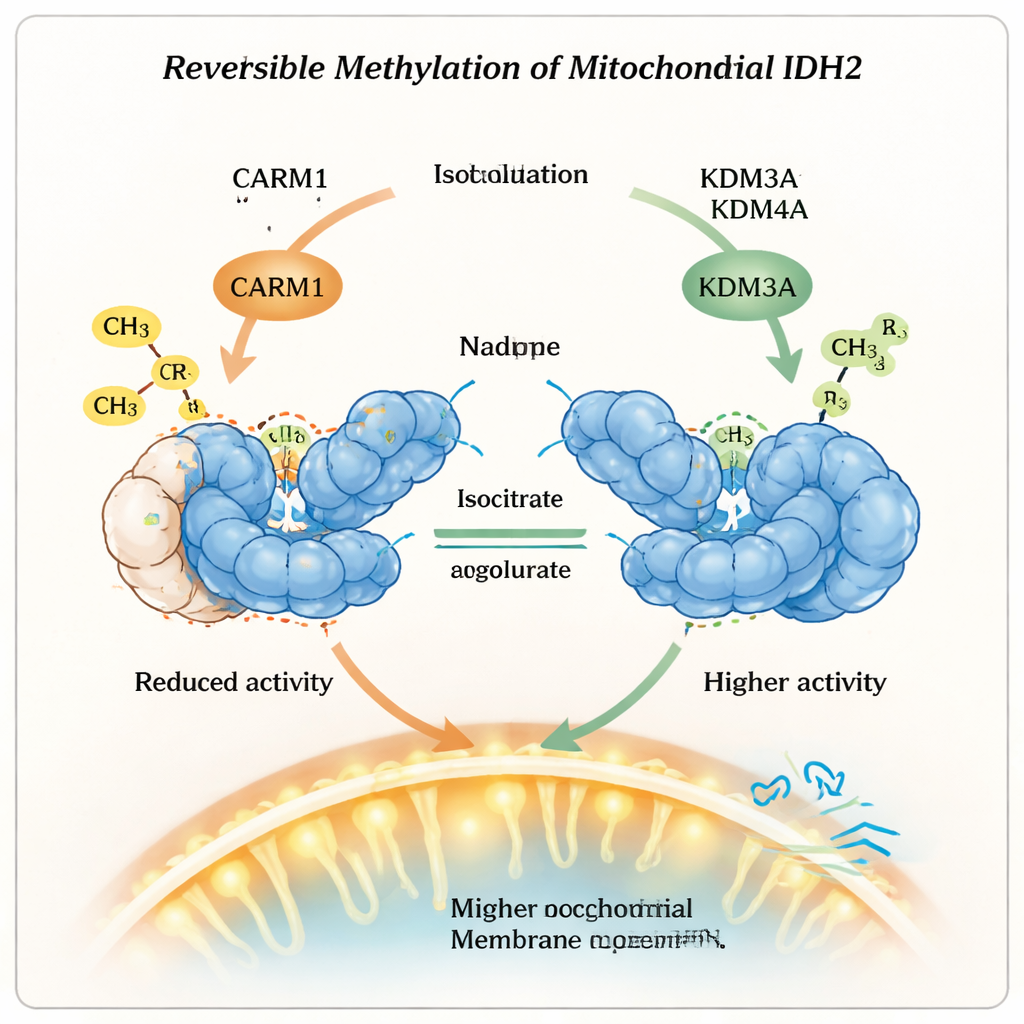
Implicaciones para la salud y la terapia
En términos cotidianos, este trabajo muestra que las mitocondrias no se limitan a encender o apagar enzimas, sino que usan etiquetas químicas reversibles como diales finamente ajustables. Al añadir un grupo metilo, CARM1 convierte a IDH2 en una forma de mayor vida media pero menos activa; al eliminar esa etiqueta, KDM3A y KDM4A sacrifican algo de estabilidad para ganar mayor potencia. Este equilibrio influye en cómo las células eligen entre una combustión rápida pero ineficiente de azúcares y una producción de energía más lenta y eficiente. Comprender este “atenuador” de metilación en IDH2 abre nuevas posibilidades terapéuticas para corregir el metabolismo mitocondrial alterado en condiciones como el cáncer y las enfermedades metabólicas, apuntando a las enzimas que escriben y borran estas marcas químicas pequeñas pero potentes.
Cita: Cho, Y., Winarto, J., Song, DG. et al. Reversible arginine methylation regulates mitochondrial IDH2 activity: coordinated control by CARM1 and KDM3A/4A. Cell Death Dis 17, 195 (2026). https://doi.org/10.1038/s41419-026-08444-3
Palabras clave: mitocondrias, IDH2, metilación de arginina, metabolismo celular, CARM1