Clear Sky Science · es
Un bucle inflamatorio MIF-p38-GSDMD en queratinocitos subyace al lupus cutáneo inducido por UVB
Por qué la luz solar puede ser un problema grave en el lupus
Para la mayoría de las personas, el sol simplemente produce bronceado o, en el peor de los casos, una quemadura. Pero para muchos pacientes con lupus, pocos minutos de luz ultravioleta B (UVB) pueden desencadenar erupciones dolorosas y prolongadas e incluso empeorar toda la enfermedad. Este estudio revela un “bucle de retroalimentación” oculto dentro de las células de la piel que ayuda a explicar por qué su piel es tan sensible a la luz, y apunta a posibles tratamientos muy locales que podrían calmar la reacción sin suprimir todo el sistema inmunitario.
Las células de la piel como problemáticas inesperadas
Los médicos sabían desde hace tiempo que el lupus eritematoso cutáneo (LEC) implica inflamación crónica y cicatrización de la piel, pero la atención a menudo se centraba en las células inmunitarias invasoras. Usando secuenciación de ARN de célula única, los autores en cambio se fijaron en las propias células estructurales de la piel: los queratinocitos de la capa externa y los fibroblastos de la capa subyacente. Encontraron que en pacientes con lupus hay subgrupos específicos de queratinocitos aumentados que muestran una fuerte “firma de interferón”, un patrón de genes de alarma antiviral permanentemente activados. Dentro de estos queratinocitos anómalos destacó una proteína mensajera: el factor inhibidor de la migración de macrófagos, o MIF, que se producía a niveles mucho más altos que moléculas inflamatorias más conocidas como TNF o IL‑6.
Un mensajero oculto liberado por la luz solar
Encontrar altos niveles de MIF dentro de los queratinocitos no explicaba todavía por qué la luz solar es tan peligrosa. Cuando el equipo expuso queratinocitos cultivados a UVB, descubrieron que la cantidad total de MIF en las células apenas cambiaba, pero la proteína se liberaba al fluido circundante de forma dependiente de la dosis. Cuanto más UVB, más MIF se filtraba, correlacionando estrechamente con un marcador de daño a la membrana. Cuando este fluido rico en MIF se aplicó a queratinocitos y fibroblastos frescos, provocó cambios típicos del LEC: más citocinas inflamatorias y enzimas que degradan y remodelan la matriz de sostén de la piel. Silenciar MIF con herramientas genéticas o bloquearlo con una pequeña molécula redujo drásticamente estas reacciones nocivas, mostrando que el MIF derivado de queratinocitos no es un mero espectador sino un amplificador clave del daño inducido por UVB. 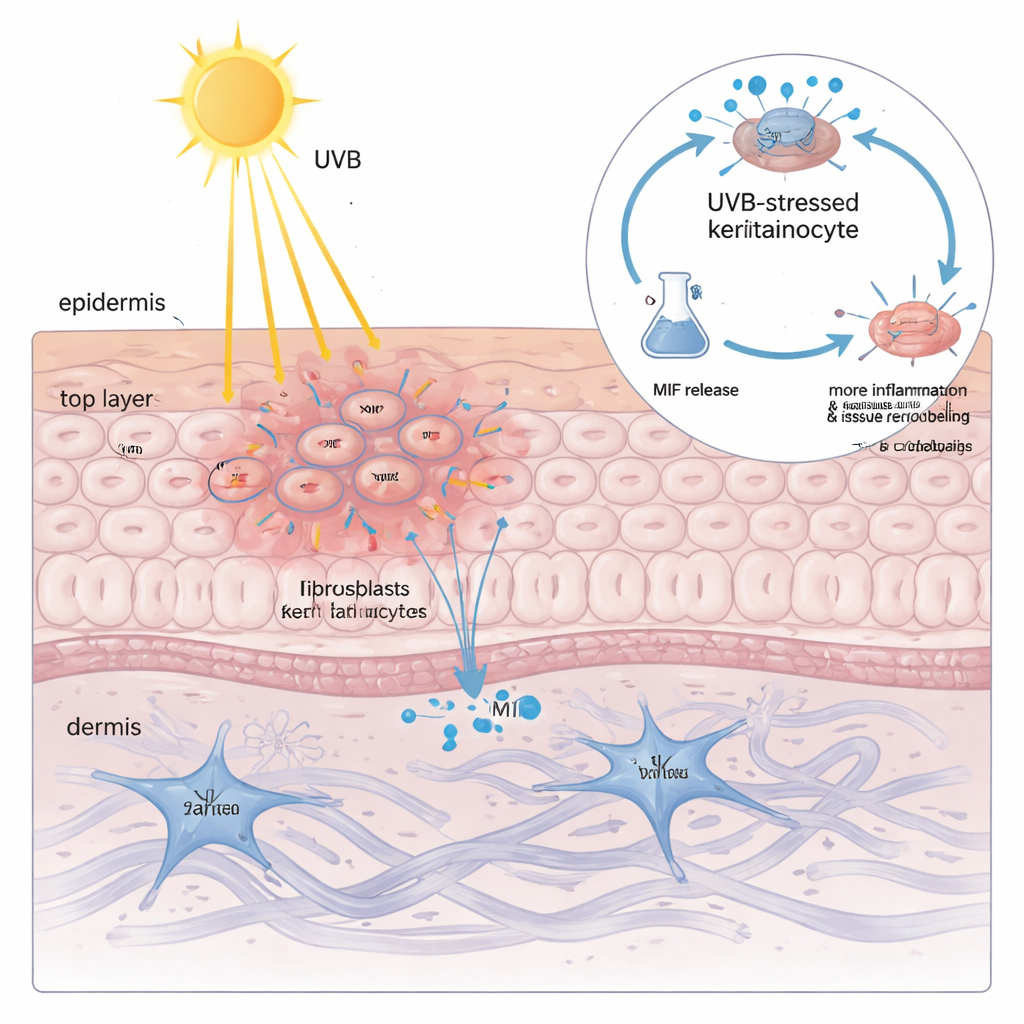
Un bucle inflamatorio autosostenido dentro de los queratinocitos
Para entender cómo el UVB fuerza a los queratinocitos a liberar MIF, los investigadores construyeron un modelo de queratinocitos “tipo lupus” cargando las células con su propio ADN y ARN, imitando los residuos genéticos mal gestionados que se observan en lupus. En este estado primado, el UVB activó una llamada respuesta de estrés ribotóxico: una señal de daño desde los ribosomas que encendió una quinasa llamada ZAKα y, a su vez, la enzima de estrés p38. Esta vía potenció otra proteína, el factor de transcripción C/EBPβ, que se unió a la región reguladora del gen NLRP3 y lo activó. NLRP3, a su vez, impulsó el corte de GSDMD, una proteína formadora de poros que perfora la membrana celular y provoca una forma inflamatoria de muerte celular conocida como piroptosis. De manera crucial, el MIF escapó principalmente a través de estos poros formados por GSDMD, no por vesículas secretoras normales. Una vez fuera, el MIF se unió a su receptor de superficie CD74 en los queratinocitos, reactivando p38, NLRP3 y GSDMD y cerrando así un círculo vicioso: UVB → p38 → NLRP3 → poros GSDMD → liberación de MIF → más activación de p38.
Del conocimiento molecular a nuevos tratamientos locales
Este bucle no fue solo una curiosidad de laboratorio. En una cepa de ratón propensa al lupus, la exposición a UVB produjo lesiones cutáneas severas con altos niveles de MIF, activación de p38, NLRP3 y GSDMD fragmentado en la epidermis. Cuando los investigadores utilizaron un virus de terapia génica para silenciar el gen Mif específicamente en la piel, las erupciones inducidas por UVB fueron mucho más leves y los marcadores de inflamación y remodelado de tejidos disminuyeron tanto en queratinocitos como en fibroblastos. Para evitar efectos secundarios sistémicos de fármacos, también diseñaron parches de microneedles solubles cargados con el inhibidor de MIF ISO‑1. Presionadas brevemente sobre la piel, estas diminutas agujas administraron el fármaco sin dolor en las capas superiores. Los ratones propensos al lupus tratados desarrollaron muchas menos y menos graves lesiones tras la UVB, y la firma molecular del bucle MIF‑p38‑GSDMD se atenuó notablemente. 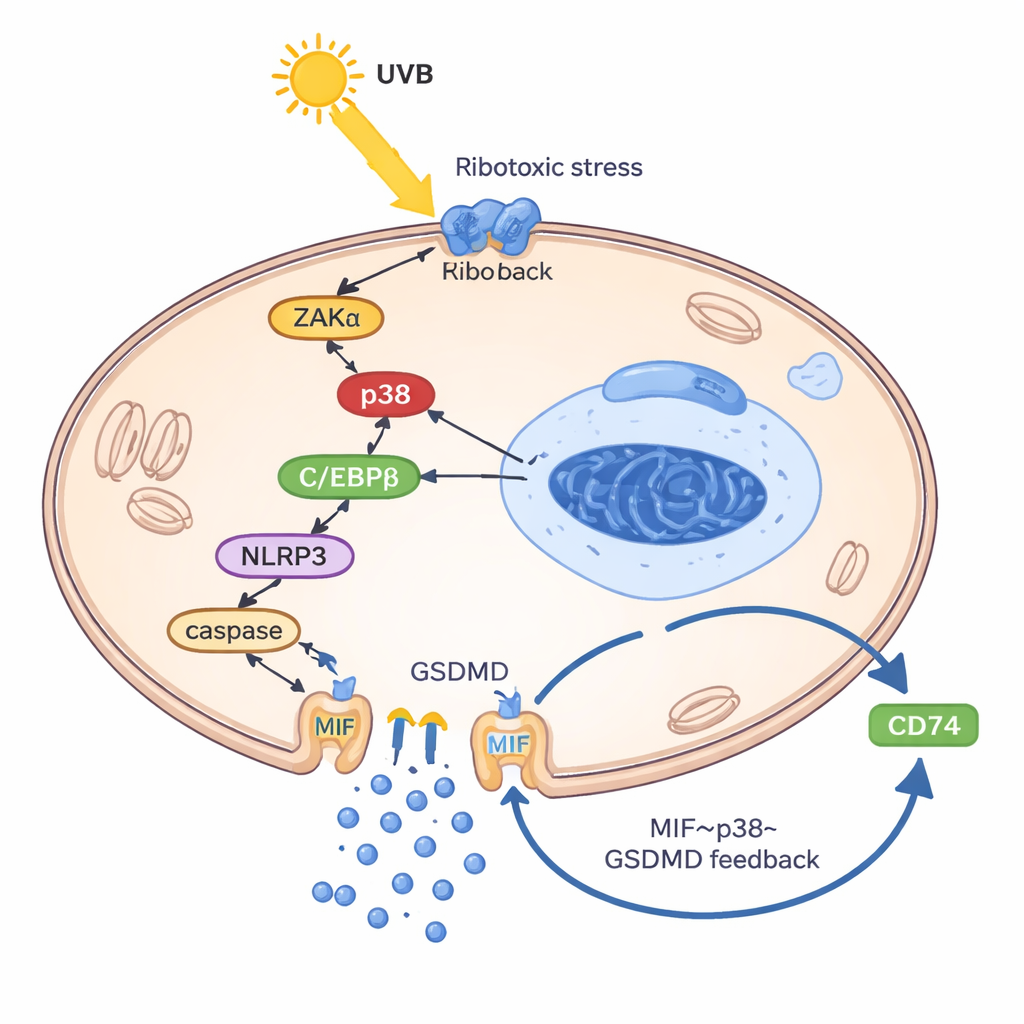
Qué significa esto para las personas con lupus
En términos sencillos, este trabajo muestra que en el lupus ciertas células de la piel están programadas para sobrerreaccionar al UVB liberando una potente molécula “amplificadora”, MIF, a través de poros que ellas mismas generan en la membrana. Ese refuerzo retroalimenta y mantiene la maquinaria inflamatoria activa, incluso después de que la exposición inicial a la luz haya terminado. Al mapear este bucle paso a paso, el estudio sugiere que bloquear MIF directamente en la piel —mediante silenciamiento génico o sistemas de administración inteligentes como parches de microneedles— podría romper el ciclo de los brotes fotosensibles sin apagar de forma generalizada el sistema inmunitario. Si estrategias similares resultan seguras y eficaces en humanos, podrían ofrecer a las personas con lupus nuevas formas de vivir con mayor comodidad a la luz.
Cita: Guo, C., Luo, S., Luo, J. et al. A MIF-p38-GSDMD inflammatory loop in keratinocytes underlies UVB-induced cutaneous lupus. Cell Death Dis 17, 198 (2026). https://doi.org/10.1038/s41419-026-08443-4
Palabras clave: lupus cutáneo, fotosensibilidad, queratinocitos, bucle inflamatorio, terapia con microneedles