Clear Sky Science · es
Neumonitis relacionada con inhibidores de puntos de control inmunitarios: avances actuales y el papel putativo de la terapia con células madre mesenquimales
Cuando el tratamiento contra el cáncer vuelve su contra las vías respiratorias
Los fármacos que liberan al sistema inmunitario contra el cáncer han transformado el tratamiento de enfermedades como el cáncer de pulmón y el melanoma. Sin embargo, este nuevo poder tiene un precio: en algunos pacientes, el mismo ataque inmunitario que elimina tumores también se vuelve contra los pulmones, provocando una afección llamada neumonitis relacionada con inhibidores de puntos de control inmunitarios (ICIP). Esta revisión explica qué es la ICIP, por qué ocurre, cómo la tratan hoy los médicos y por qué un tipo especial de células madre —las células madre mesenquimales (CMM)— podría algún día ofrecer una forma más segura y precisa de calmar la tormenta sin sacrificar el control del cáncer. 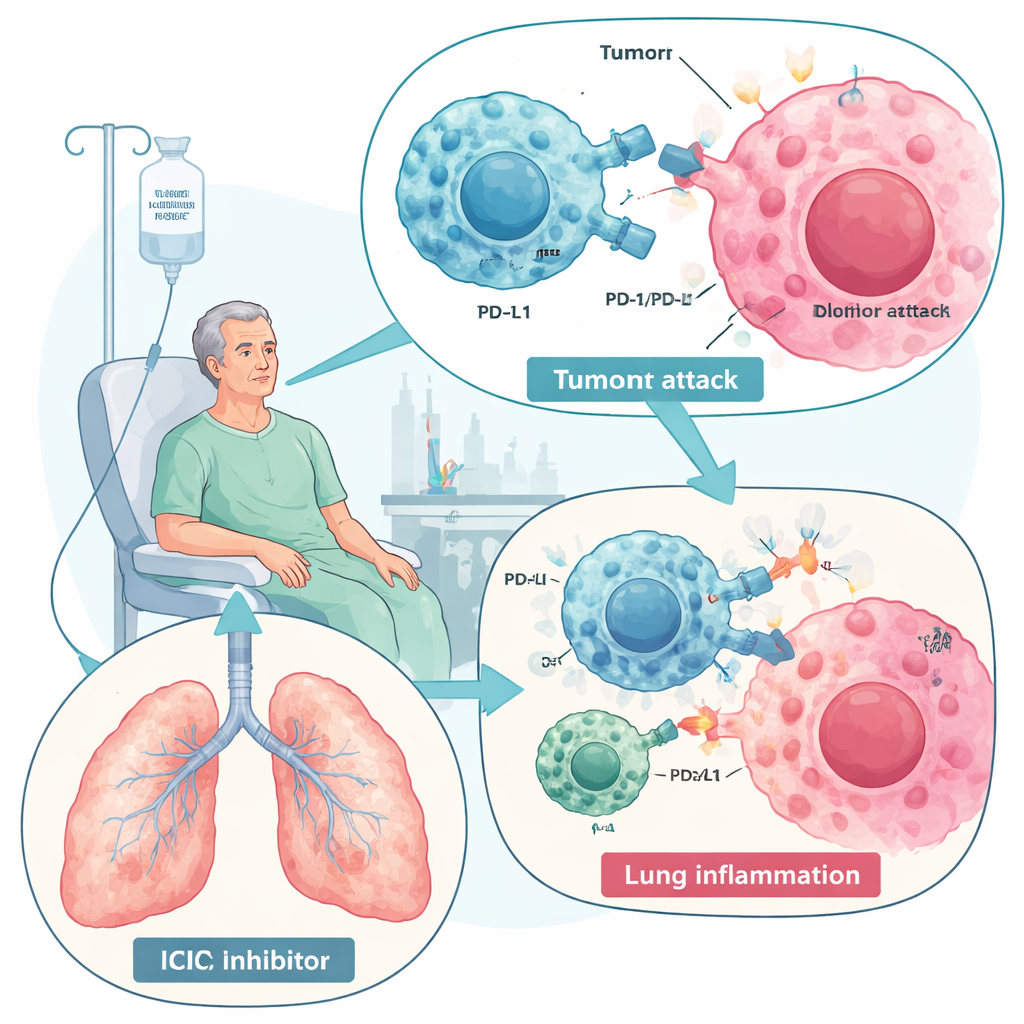
Fármacos oncológicos potentes con un riesgo oculto para los pulmones
Los inhibidores de puntos de control inmunitarios, especialmente los que bloquean PD-1 y PD-L1, actúan eliminando los “frenos” moleculares que normalmente mantienen las respuestas inmunitarias bajo control. Con los frenos quitados, las células T pueden reconocer y destruir mejor las células cancerosas, mejorando la supervivencia en muchos tipos de tumor. Pero este mismo impulso puede romper la tolerancia normal y desencadenar efectos adversos inmunitarios en múltiples órganos. La ICIP es la complicación pulmonar más grave de estos fármacos y una de las principales causas inmunomediadas de muerte relacionada con el tratamiento. Afecta desde unos pocos por ciento hasta casi un tercio de los pacientes en algunos estudios de la práctica clínica real, sobre todo en quienes tienen cáncer de pulmón o enfermedades pulmonares preexistentes como EPOC o enfermedad pulmonar intersticial. Los síntomas varían desde tos leve y dificultad para respirar hasta insuficiencia respiratoria potencialmente fatal.
Cómo el sistema inmunitario daña el pulmón
La revisión describe la ICIP como resultado de un equilibrio inmunitario perturbado dentro de los pulmones. Células “combatientes” hiperactivas —células T CD8, ciertos linfocitos T ayudadores, macrófagos inflamatorios, neutrófilos y células asesinas naturales— invaden el tejido pulmonar y liberan proteínas señalizadoras agresivas, incluidas interferón‑gamma, TNF‑alfa e interleucinas como IL‑6 e IL‑17. Al mismo tiempo, las células normalmente protectoras que amortiguan la inflamación, como las células T reguladoras y los macrófagos orientados a la reparación, están reducidas. Algunos pacientes también muestran niveles crecientes de anticuerpos autorreactivos antes o durante el tratamiento, lo que sugiere que la ICIP podría asemejarse en parte a una enfermedad autoinmune. En el líquido lavado de los pulmones, los médicos encuentran un patrón inflamatorio rico en células T y una mezcla de citocinas distinta de la infección o la progresión tumoral, lo que puede ayudar en el diagnóstico.
Visualizar, graduar y tratar el daño
En las tomografías computarizadas, la ICIP con mayor frecuencia aparece como áreas nebulosas en vidrio deslustrado o consolidaciones parcheadas dispersas por ambos pulmones, patrones que difieren del daño por radiación, que se mantiene confinado al campo irradiado. Los médicos diagnostican la ICIP combinando hallazgos radiológicos, síntomas y una cuidadosa exclusión de infección y otras causas. Las guías internacionales gradúan la gravedad de 1 (leve, a menudo solo radiológico) a 4 (insuficiencia respiratoria potencialmente mortal). El pilar del tratamiento actual son los glucocorticoides: potentes esteroides antiinflamatorios, a veces combinados con otros fármacos inmunomoduladores como tocilizumab (que bloquea IL‑6) o infliximab (que bloquea TNF‑alfa) en casos graves o resistentes a esteroides. Estos enfoques pueden salvar vidas, pero son herramientas toscas: los esteroides tienen muchos efectos secundarios, algunos pacientes no responden y la supresión inmune generalizada puede debilitar la propia respuesta antitumoral que estos fármacos pretendían potenciar.
Por qué las células madre entran en la conversación
Las células madre mesenquimales, que pueden obtenerse de médula ósea, tejido adiposo o cordón umbilical, han emergido como prometedores “moduladores inmunitarios” más que como simples constructores tisulares. Cuando se infunden en el torrente sanguíneo, muchas de estas células quedan temporalmente atrapadas en los pequeños vasos del pulmón —el llamado efecto de primer paso—, lo que es una desventaja para tratar órganos distantes pero una ventaja potencial para la enfermedad pulmonar. En modelos animales y en ensayos humanos iniciales de afecciones como neumonía grave, síndrome de distrés respiratorio agudo, enfermedad inflamatoria intestinal y enfermedad injerto contra huésped, las CMM atenúan respuestas inmunitarias sobreactivadas, desplazan las células inmunitarias hacia un estado más equilibrado y secretan factores de crecimiento que fomentan la reparación tisular limitando a la vez la cicatrización. Es importante destacar que sus beneficios a menudo surgen no por convertirse en células pulmonares, sino por la mezcla de moléculas señalizadoras y diminutas vesículas que liberan. 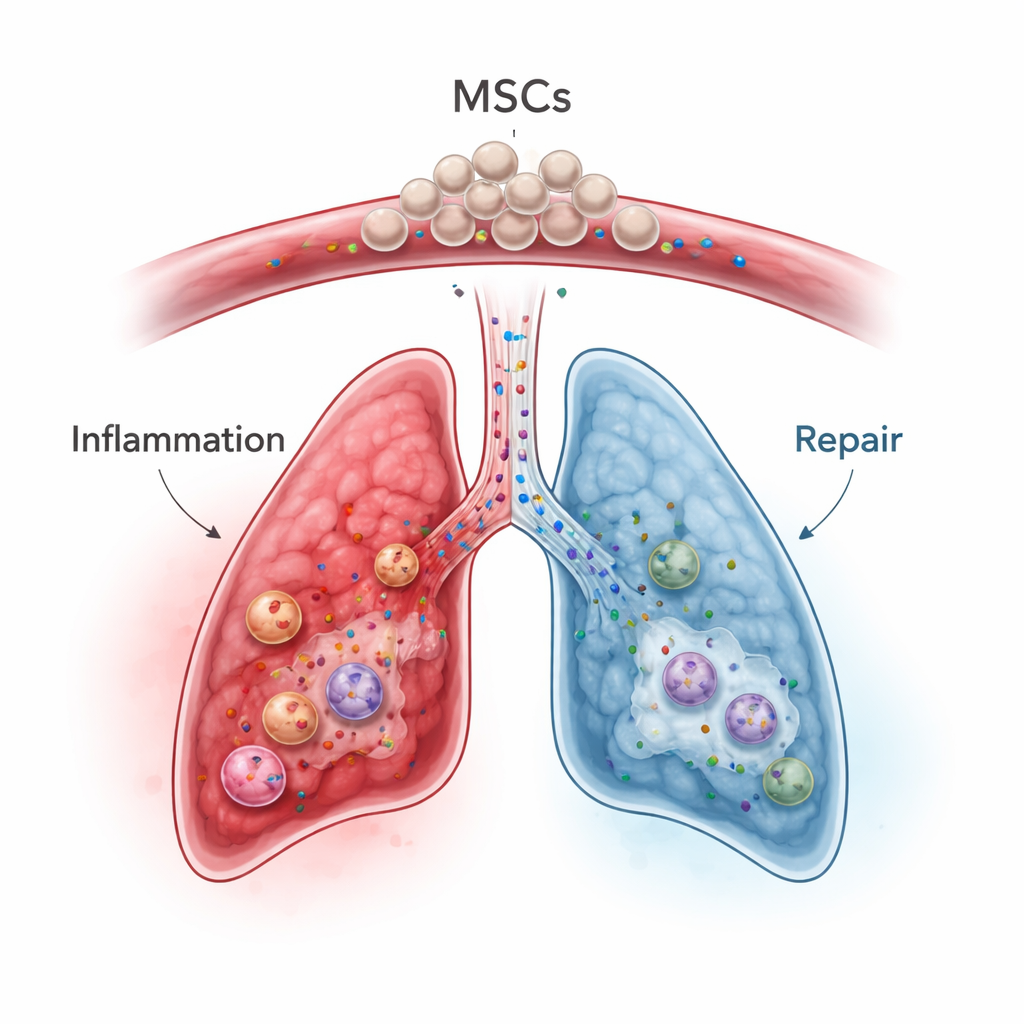
Cómo las CMM podrían calmar la ICIP sin anular la cura
En el contexto de la ICIP, las CMM podrían, en teoría, abordar varios problemas a la vez. Pueden frenar directamente a las células T activadas, promover el crecimiento y la función de las células T reguladoras y empujar a los macrófagos a alejarse de un modo agresivo y lesionante hacia uno reparador. También reducen mensajeros inflamatorios clave como IL‑6, IL‑1β y TNF‑alfa, y aumentan factores antiinflamatorios y proteínas protectoras como TSG‑6 que ayudan a limitar la lesión pulmonar y la fibrosis. Trabajos preclínicos sugieren que las CMM o exosomas derivados de CMM modificadas pueden reducir tormentas de citocinas y el daño orgánico inducido por inhibidores de puntos de control o radiación, mientras que en algunos escenarios preservan la actividad antitumoral mejor que los inmunosupresores estándar. Aun así, los autores advierten que las CMM también pueden interactuar con los tumores y la coagulación sanguínea de maneras complejas, y que sus efectos dependen en gran medida del entorno inflamatorio circundante e incluso de la fuente de las CMM (médula ósea, tejido adiposo o cordón umbilical).
Mirando hacia adelante: promesa con pruebas rigurosas
Para los pacientes cuyo tratamiento contra el cáncer se detiene o queda en riesgo por una toxicidad pulmonar grave, las terapias basadas en CMM podrían en el futuro proporcionar una forma más dirigida de enfriar la inflamación, reparar el tejido pulmonar y prevenir la cicatrización a largo plazo —idealmente sin deshacer los beneficios vitales de la inhibición de puntos de control inmunitarios. Sin embargo, aún no se han completado ensayos específicos de CMM para ICIP. Los autores sostienen que son urgentemente necesarios estudios animales bien diseñados y ensayos clínicos para definir qué tipo de producto de CMM o exosomas funciona mejor, cuánto administrar, cuándo hacerlo en relación con esteroides e inmunoterapia y cómo vigilar riesgos como el crecimiento tumoral o la trombosis. Hasta entonces, las CMM siguen siendo una opción prometedora pero todavía experimental en el horizonte para manejar este grave efecto secundario de la oncología moderna.
Cita: Li, Z., Zheng, X., Xia, H. et al. Immune checkpoint inhibitor-related pneumonitis: current advances and the putative role of mesenchymal stem cell therapy. Cell Death Dis 17, 200 (2026). https://doi.org/10.1038/s41419-026-08440-7
Palabras clave: efectos secundarios de la inmunoterapia, neumonitis, inhibidores de puntos de control, células madre mesenquimales, inflamación pulmonar