Clear Sky Science · es
c-Myc/GRPEL1 mantiene la síntesis de ácidos grasos vía FASN para apoyar la proliferación de células PDAC
Por qué importan las ansias de grasa de las células cancerosas
El cáncer de páncreas es uno de los más letales, en parte porque sus células son expertas en reprogramar su propio metabolismo para sobrevivir y crecer. Este estudio examina una parte sorprendente de esa historia: cómo las células tumorales pancreáticas aumentan sus “factorías de grasa” internas para alimentar un crecimiento incesante, y cómo bloquear este proceso podría abrir nuevas opciones terapéuticas para los pacientes.
Un cáncer difícil con una ventaja metabólica
La mayoría de los cánceres pancreáticos son de un tipo llamado adenocarcinoma ductal pancreático (PDAC), que suele detectarse tarde y responde mal a las terapias actuales. Las células de PDAC viven en un entorno hostil con poco oxígeno y nutrientes escasos, sin embargo prosperan al reconectar la forma en que usan azúcares, grasas y otros combustibles. Sus mitocondrias —pequeñas centrales energéticas dentro de las células— juegan un papel central en esta reconfiguración. Para mantener estas centrales en funcionamiento, las células supervisan y reparan constantemente miles de proteínas mitocondriales, un proceso conocido como control de calidad de proteínas mitocondriales. Hasta ahora no estaba claro cómo esta maquinaria de control de calidad se conecta con la forma en que los tumores pancreáticos se alimentan.
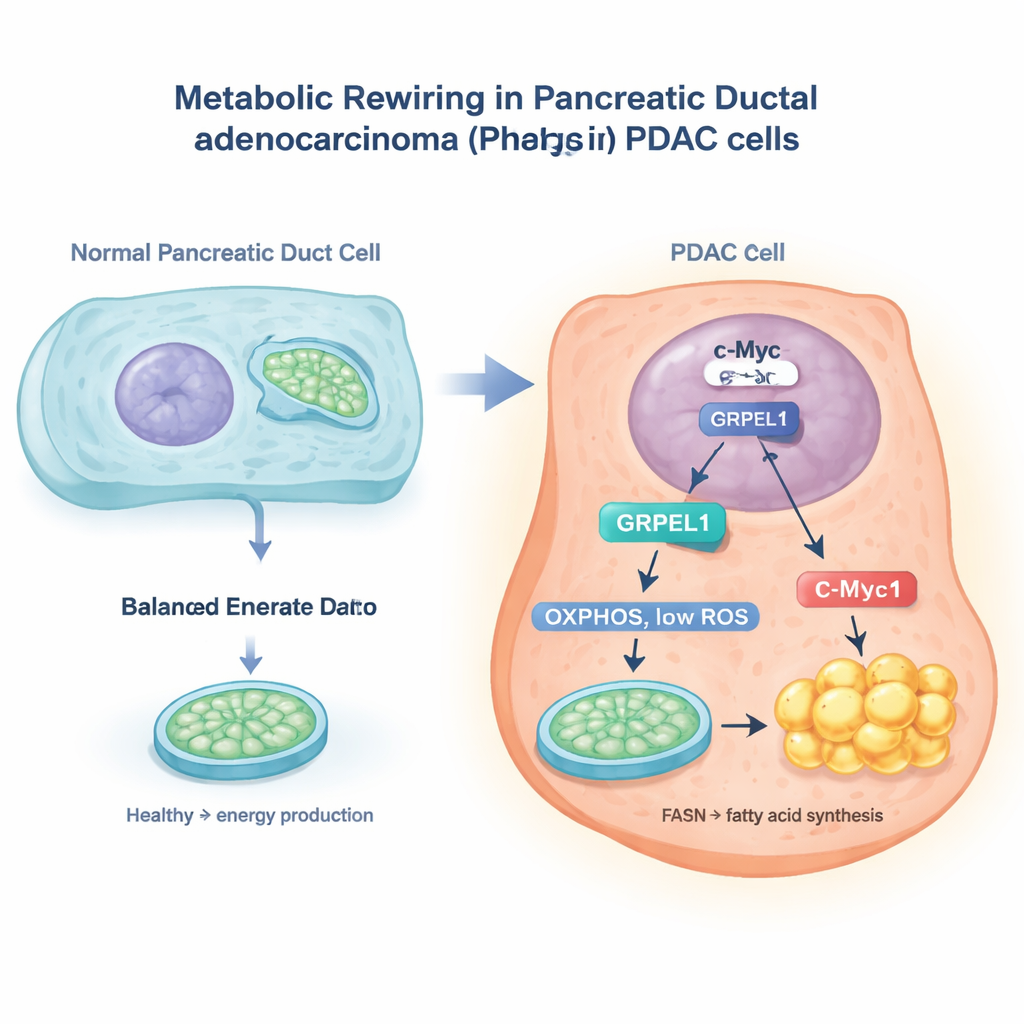
El interruptor c-Myc y un asistente mitocondrial
Los investigadores utilizaron grandes bases de datos de cáncer y experimentos en células de cáncer pancreático para centrarse en una proteína llamada GRPEL1, una ayudante implicada en el manejo de proteínas mitocondriales. Descubrieron que un gen cancerígeno bien conocido, c-Myc, actúa como un interruptor molecular en el núcleo celular que activa el gen GRPEL1. Cuando los niveles de c-Myc disminuyeron, los de GRPEL1 cayeron; cuando c-Myc se aumentó, GRPEL1 subió. Las muestras tumorales de pacientes también mostraron que c-Myc y GRPEL1 tienden a estar ambos elevados, y ambos se asociaron con peores resultados. En células PDAC cultivadas en el laboratorio, reducir GRPEL1 ralentizó la división celular y el crecimiento de colonias, mientras que añadir GRPEL1 extra ayudó a las células a proliferar más rápido, especialmente cuando c-Myc estaba bloqueado por otros medios.
De las mitocondrias a la producción de grasas
Indagando más, el equipo encontró que GRPEL1 hace más que mantener en orden las proteínas mitocondriales. Cuando se agotó GRPEL1, las mitocondrias en las células PDAC se volvieron menos eficaces en producir energía, perdieron su forma normal y liberaron más especies reactivas de oxígeno (ROS), subproductos químicamente reactivos a veces llamados “óxido” celular. Este aumento de ROS tuvo un efecto secundario: redujo los niveles de la sintasa de ácidos grasos (FASN), una enzima clave que construye nuevos ácidos grasos dentro de las células. Con FASN reducido, las células fabricaron menos grasas, almacenaron menos lípidos y su crecimiento se ralentizó. Cuando los investigadores eliminaron los ROS con un antioxidante, los niveles de FASN se recuperaron, lo que muestra que el vínculo GRPEL1–FASN está mediado por ROS. Curiosamente, c-Myc en sí no pareció activar directamente el gen FASN en este sistema, sino que influyó en FASN de forma indirecta a través de GRPEL1 y el estrés mitocondrial.
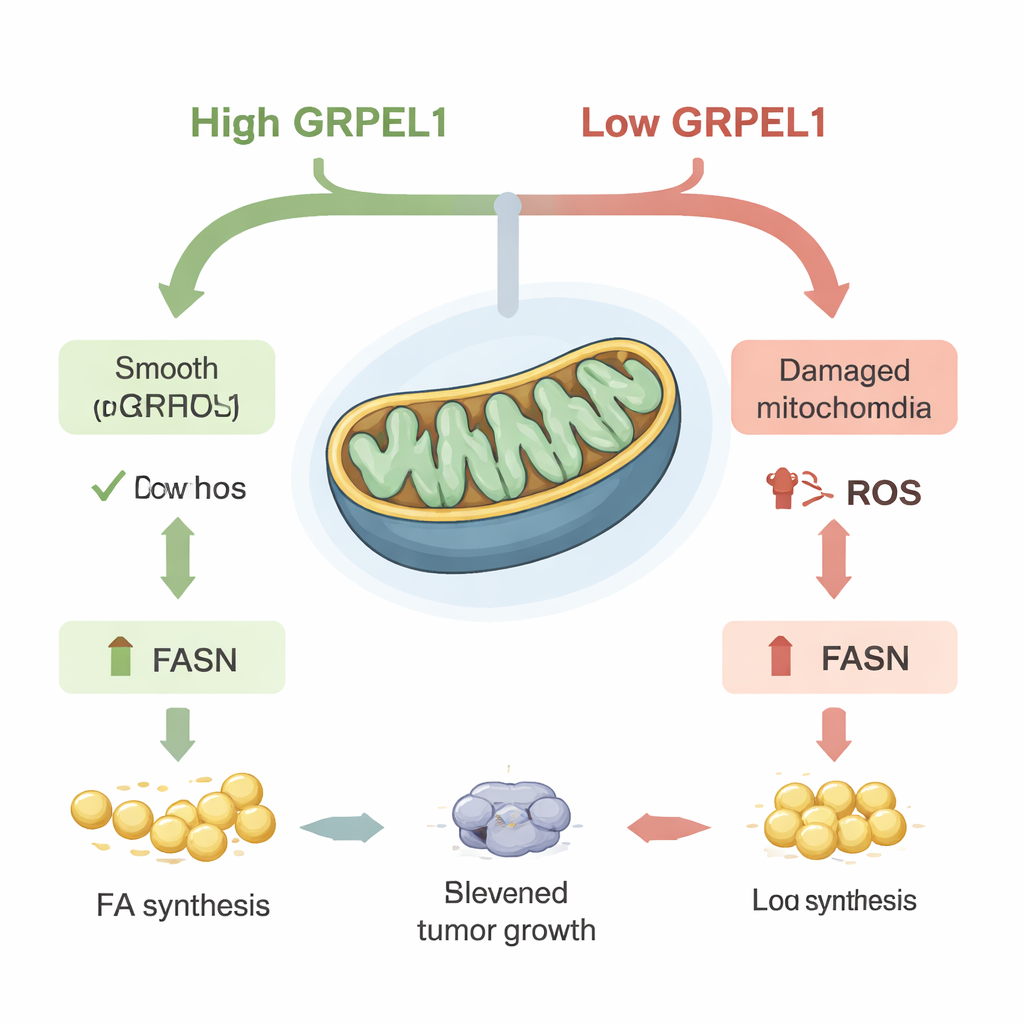
La grasa como combustible para el crecimiento tumoral
Dado que FASN está en el centro de la construcción de grasas, los científicos preguntaron si restaurarlo podría rescatar el crecimiento tumoral cuando GRPEL1 era bajo. En cultivos celulares, forzar a las células a producir más FASN revirtió en parte la desaceleración del crecimiento y la formación de colonias causada por la pérdida de GRPEL1. Lo mismo ocurrió en ratones: los tumores formados por células con GRPEL1 reducido crecieron más lentamente, pero reintroducir FASN revivió tanto el tamaño tumoral como el contenido graso. Análisis detallados de metabolitos y lípidos mostraron descensos generalizados en muchas moléculas relacionadas con las grasas cuando se redujeron GRPEL1 o c-Myc. Importante, suministrar ácidos grasos adicionales o una mezcla lipídica desde el exterior restauró parcialmente el crecimiento tanto en líneas celulares cancerosas como en organoides pancreáticos derivados de pacientes —mini-tumores cultivados en 3D—, lo que sugiere que el problema principal era la pérdida de grasas recién sintetizadas.
Convertir una vulnerabilidad en una terapia
En conjunto, el trabajo pinta un panorama claro: en el cáncer de páncreas, c-Myc eleva GRPEL1, que ayuda a que las mitocondrias funcionen sin problemas y mantiene los ROS bajo control. Este entorno mitocondrial tranquilo permite a las células mantener niveles altos de FASN, produciendo nuevos ácidos grasos que sirven como bloques para membranas, reservas energéticas y señales de crecimiento. Cuando se bloquea GRPEL1, las mitocondrias fallan, los ROS aumentan, FASN cae y las células cancerosas tienen dificultades para crecer —un efecto que puede sortearse parcialmente si se suministran grasas desde el exterior. Para el lector general, la conclusión es que los tumores pancreáticos dependen de un circuito interno de “fabricación de grasas”, impulsado por c-Myc, GRPEL1 y FASN. Fármacos que interrumpan este eje de producción de ácidos grasos, especialmente en los tumores donde está muy activo, podrían ofrecer una forma prometedora de privar de nutrientes a las células de cáncer de páncreas dejando a los tejidos normales menos afectados.
Cita: Wang, J., Zhang, L., Chen, K. et al. c-Myc/GRPEL1 maintains fatty acid synthesis via FASN to support PDAC cell proliferation. Cell Death Dis 17, 205 (2026). https://doi.org/10.1038/s41419-026-08439-0
Palabras clave: cáncer de páncreas, metabolismo tumoral, síntesis de ácidos grasos, mitocondrias, c-Myc