Clear Sky Science · es
KDM5B coopera con el complejo CRL4B para promover la tumorogénesis del cáncer de mama ER+ regulando el metabolismo del colesterol
Por qué esta investigación importa para la salud cotidiana
El cáncer de mama es el cáncer más frecuente en mujeres, y muchos tumores crecen en respuesta a la hormona estrógeno. Estos cánceres hacen más que dividirse rápidamente: también reprograman cómo usan grasas como el colesterol. Este estudio revela cómo una proteína reguladora de genes llamada KDM5B se asocia con otro complejo proteico, CRL4B, para aumentar el colesterol dentro de las células de cáncer de mama con receptor de estrógeno positivo (ER+). Al entender esta asociación oculta, los científicos esperan encontrar nuevas formas de frenar el crecimiento tumoral y mejorar tratamientos ya existentes, como la terapia hormonal y los fármacos reductores de colesterol.
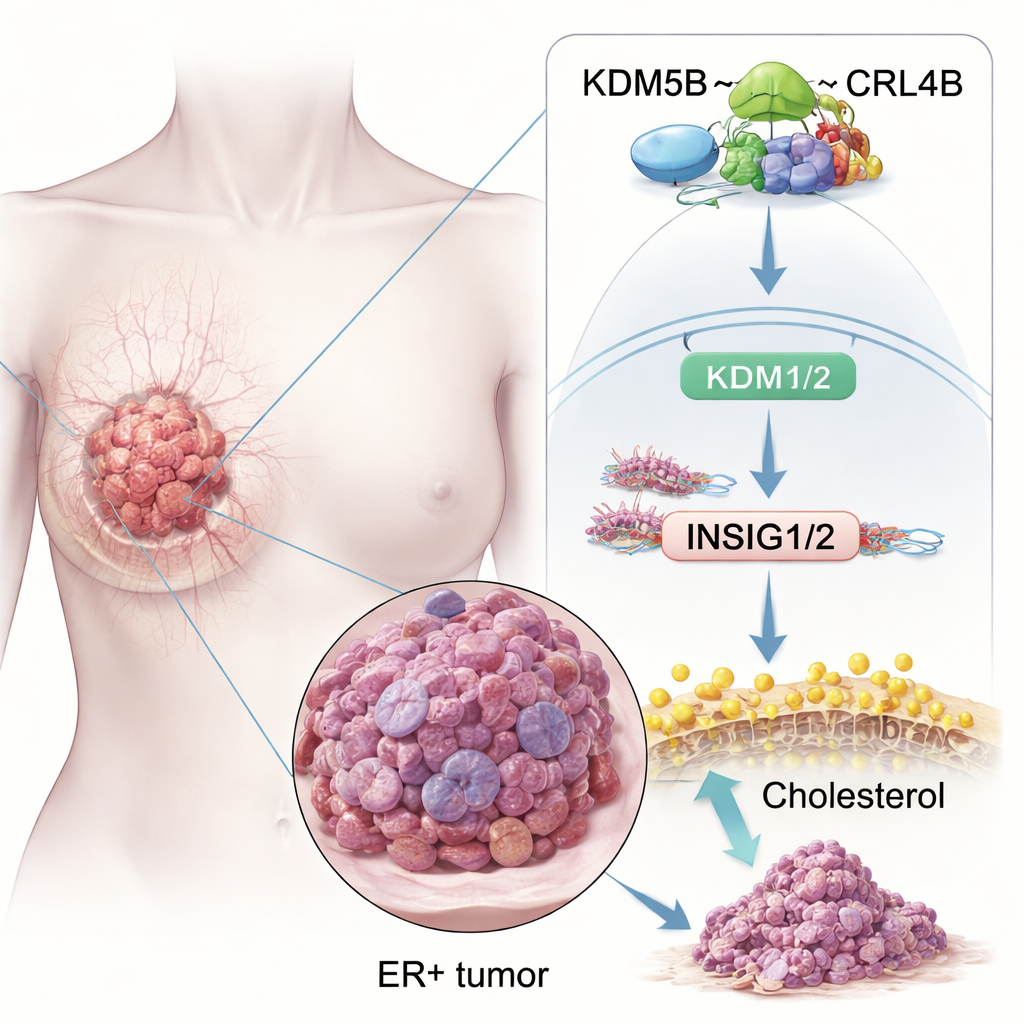
Una proteína que inclina la balanza hacia el cáncer
Los investigadores se preguntaron primero si KDM5B está simplemente presente en los cánceres ER+ o si realmente contribuye a impulsarlos. Al analizar grandes bases de datos y muestras de tejido, encontraron que los niveles de KDM5B son más altos en tumores de mama que en tejido mamario normal, y especialmente elevados en tumores ER+. Los pacientes cuyos tumores producen más KDM5B tienden a tener una supervivencia peor, incluso cuando reciben quimioterapia estándar o terapia hormonal. En experimentos en cultivo celular, aumentar KDM5B hizo que las células de cáncer de mama ER+ crecieran más rápido, invadieran con mayor facilidad los tejidos circundantes y formaran más agrupaciones tipo célula madre, que se cree que originan nuevos tumores. Reducir KDM5B produjo el efecto contrario, disminuyendo colonias en placas y tumores en ratones.
Una asociación poderosa dentro de las células tumorales
Para ver cómo KDM5B ejerce estos efectos, el equipo buscó sus socios proteicos. Descubrieron que KDM5B se une físicamente a partes de una máquina molecular llamada complejo CRL4B, un sistema enzimático que etiqueta proteínas y también modifica cómo se empaqueta el ADN. Pruebas bioquímicas detalladas mostraron que KDM5B interactúa directamente con dos componentes de CRL4B, CUL4B y DDB1, a través de regiones específicas de cada proteína. En células de cáncer de mama ER+, este complejo KDM5B–CRL4B actúa sobre muchos genes en sus interruptores de encendido/apagado. Mediante mapeo a escala genómica, los autores encontraron que KDM5B y CUL4B con frecuencia se localizan juntos en promotores génicos, donde alteran marcas químicas en histonas —los carretes alrededor de los cuales se enrolla el ADN— para silenciar genes.
Soltando los frenos del colesterol
Entre muchas vías afectadas, destacó el metabolismo del colesterol. Las células cancerosas necesitan colesterol extra para construir membranas y resistir el estrés, y los tumores ER+ también usan moléculas derivadas del colesterol para imitar el estrógeno. El estudio muestra que el complejo KDM5B–CRL4B se une directamente a las regiones de control de dos genes «freno» clave, INSIG1 e INSIG2. Estos genes normalmente ayudan a mantener bajo control a un regulador maestro del colesterol, SREBP2. KDM5B–CRL4B añade una marca represiva (H2AK119ub1) y elimina una marca activadora (H3K4me3) en las histonas en los promotores de INSIG1/2, reduciendo la expresión de estos genes. Con menos proteínas INSIG1/2, SREBP2 queda liberado para activar genes de síntesis de colesterol, elevando los niveles de colesterol dentro de las células de cáncer de mama ER+ y potenciando su comportamiento invasivo. Cuando los investigadores interrumpieron KDM5B o CRL4B, INSIG1/2 aumentaron, la actividad de SREBP2 disminuyó y el colesterol total en las células se redujo.
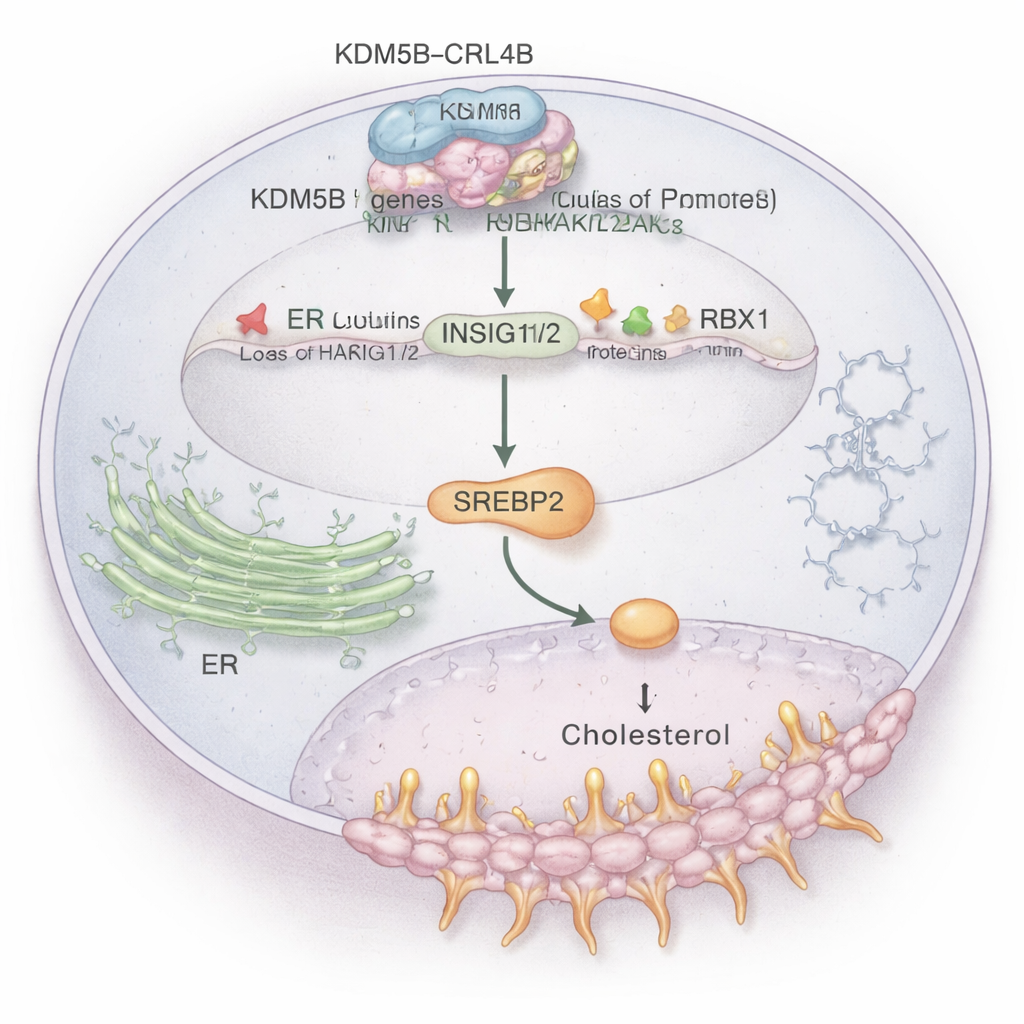
Intersección entre fármacos para el colesterol y señales cancerígenas
El trabajo también vincula esta vía con una señal derivada del colesterol llamada 27‑hidroxicolesterol (27‑HC), una molécula ya conocida por promover el cáncer de mama ER+. Tratar células ER+ con 27‑HC aumentó los niveles de KDM5B y suprimió aún más INSIG1/2, empujando a las células hacia mayor crecimiento e invasión. De manera importante, bloquear KDM5B o CRL4B atenuó estos efectos agresivos, lo que sugiere que 27‑HC actúa en parte al alimentar el eje KDM5B–CRL4B. Por separado, los investigadores mostraron que la simvastatina, una estatina de uso generalizado para reducir el colesterol, ralentizó el crecimiento de células de cáncer de mama, y cuando se combinó con un inhibidor de KDM5B, el efecto antitumoral fue mayor. Esto sugiere que combinar fármacos que atacan la producción de colesterol con fármacos que inhiben la actividad reguladora de KDM5B podría ser una estrategia terapéutica prometedora.
Qué significa esto para pacientes y futuros tratamientos
Este estudio revela una nueva cadena de eventos dentro de las células de cáncer de mama ER+: una señal relacionada con el colesterol (27‑HC) aumenta KDM5B; KDM5B se asocia con el complejo CRL4B para silenciar INSIG1 e INSIG2; esto libera a SREBP2, incrementa la producción de colesterol y ayuda a los tumores a crecer, invadir y mantener células con rasgos de célula madre. Dado que KDM5B también está elevado y asociado con peor supervivencia en varios otros cánceres, bloquear esta proteína —o restaurar los frenos INSIG1/2— podría ofrecer nuevas formas de controlar el crecimiento tumoral. Aunque se necesita más trabajo antes de que esto pueda traducirse en la práctica clínica rutinaria, los hallazgos subrayan hasta qué punto el comportamiento del cáncer está ligado a moléculas cotidianas como el colesterol y cómo fármacos existentes como las estatinas podrían, en el futuro, combinarse con terapias epigenéticas para mejorar los resultados.
Cita: Yang, Y., Gao, T., Yuan, B. et al. KDM5B cooperates with CRL4B complex to promote the tumorigenesis of ER+ breast cancer via regulating cholesterol metabolism. Cell Death Dis 17, 207 (2026). https://doi.org/10.1038/s41419-026-08438-1
Palabras clave: cáncer de mama ER-positiva, metabolismo del colesterol, KDM5B, INSIG1/INSIG2, terapia epigenética