Clear Sky Science · es
BCL-xL como diana terapéutica en el cáncer colorrectal refractario a cetuximab
Por qué esto importa para las personas con cáncer de colon
El cáncer colorrectal (de colon y recto) es uno de los cánceres más frecuentes en el mundo, y muchos pacientes con enfermedad avanzada reciben un anticuerpo dirigido llamado cetuximab. Este fármaco puede reducir los tumores al principio, pero en la mayoría de los pacientes el cáncer encuentra formas de escapar en pocos meses, dejando a los médicos con pocas opciones eficaces. Este estudio plantea una pregunta urgente: cuando los tumores de colon dejan de responder al cetuximab, ¿existe otro punto débil que nuevos medicamentos puedan explotar para inducir la muerte de las células tumorales?
Cuando un fármaco dirigido deja de funcionar
El cetuximab actúa bloqueando una antena en la superficie de las células tumorales llamada receptor del factor de crecimiento epidérmico (EGFR), que impulsa su crecimiento. El equipo creó un modelo de laboratorio de resistencia exponiendo una línea celular colorrectal sensible (LIM1215) a dosis crecientes de cetuximab durante seis meses. Surgieron dos poblaciones celulares resistentes obtenidas de forma independiente que siguieron proliferando incluso con niveles altos del fármaco, aunque parecían igual de sanas y de crecimiento rápido que las células originales cuando se retiraba el medicamento. Es importante que las células resistentes aún conservaban el blanco del fármaco en su superficie y el cetuximab todavía podía unirse a él, lo que sugiere que el cáncer no se había limitado a “ocultar” o alterar el receptor.
Las células resistentes redirigen sus señales de crecimiento
Para entender cómo las células eludían el cetuximab, los investigadores examinaron las vías clave de crecimiento dentro de la célula. En las células parentales, el cetuximab normalmente atenuaba la vía MAPK, un motor principal de la división celular. En las células resistentes, la actividad de MAPK se mantenía alta incluso cuando se bloqueaba EGFR, mostrando que la señal de crecimiento se había desvinculado del receptor original. La secuenciación del ARN celular reveló nuevas mutaciones activadoras en otro gen RAS, HRAS, en subpoblaciones de las células resistentes, pero no en otros sospechosos habituales como KRAS, NRAS o BRAF. Los intentos de cerrar esta señalización redirigida con un inhibidor de MEK (que actúa aguas abajo de RAS) redujeron el crecimiento solo de forma modesta. Esto subrayó que, en lugar de perseguir cada nueva mutación, podría ser más efectivo atacar la maquinaria celular de vida o muerte compartida por distintos clones resistentes. 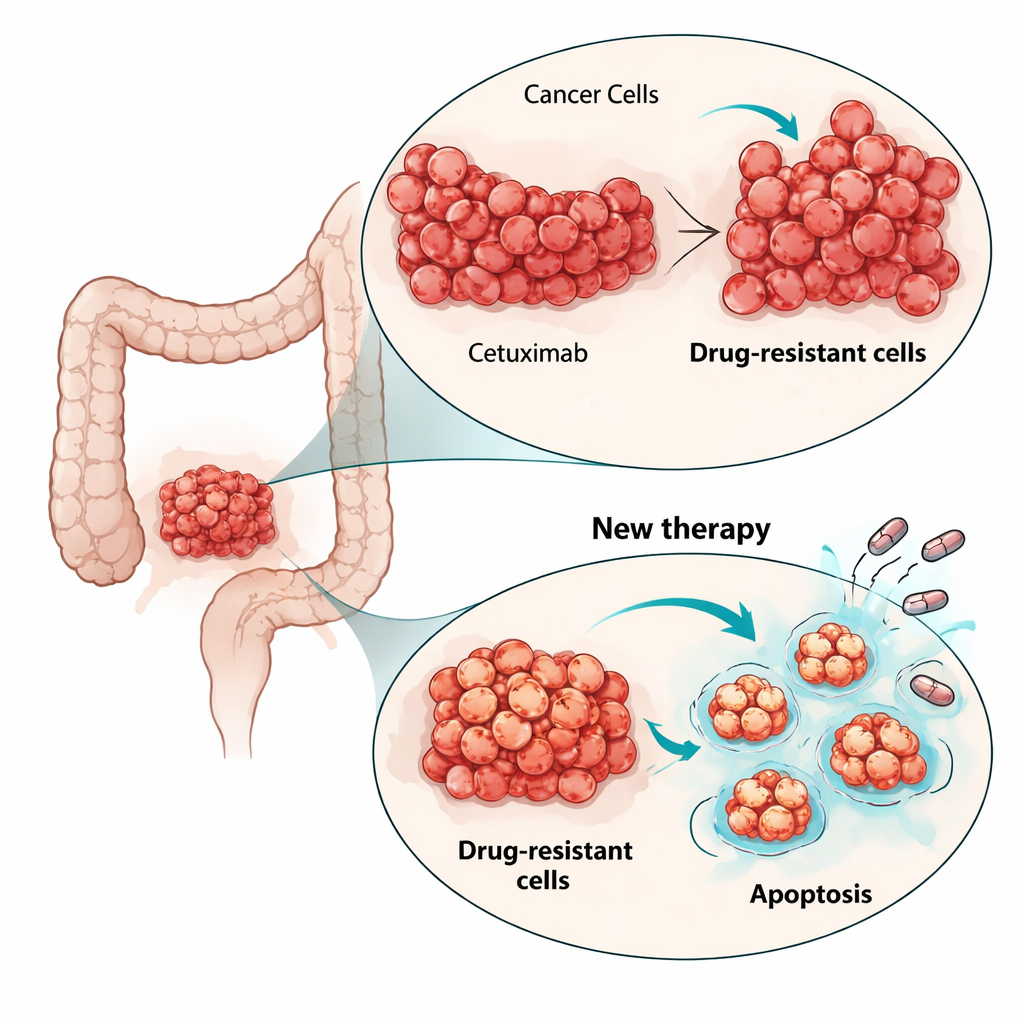
Atacar el sistema de soporte vital del cáncer
Los científicos dirigieron su atención a la apoptosis, el programa de suicidio celular incorporado que los cánceres a menudo suprimen. El análisis de expresión génica mostró que las vías relacionadas con la apoptosis estaban alteradas en las células resistentes. En particular, la proteína anti-muerte BCL-xL era más alta en una población resistente y moderadamente aumentada en la otra, mientras que otra proteína de supervivencia, MCL-1, también estaba presente. El equipo probó pequeñas moléculas llamadas miméticos BH3 diseñadas para bloquear estas proteínas de supervivencia y liberar la maquinaria de muerte. En cultivos celulares bidimensionales, las tres líneas celulares —parental y resistentes— eran sensibles a fármacos que bloquean BCL-xL o MCL-1, pero, de forma llamativa, dosis más bajas mataban con mayor eficacia a las células resistentes a cetuximab. Añadir una baja dosis del inhibidor del proteasoma bortezomib, que ayuda a acumular señales pro-muerte, aumentó aún más la muerte celular, especialmente cuando se combinó con el bloqueador de MCL-1.
De placas planas a mini-tumores 3D y tejidos de pacientes
Dado que las capas celulares planas no pueden imitar totalmente los tumores en el organismo, el equipo cultivó las células como esferoides tridimensionales incrustados en gel, reflejando mejor la arquitectura y los retos de penetración de fármacos de los tumores reales. De nuevo, bloquear BCL-xL o MCL-1 redujo la viabilidad de los esferoides, y la combinación de estos fármacos con bortezomib provocó caídas drásticas en la actividad metabólica y signos claros de muerte celular. Para evaluar si esta vulnerabilidad existe en material tumoral humano más realista, utilizaron cortes finos de cánceres colorrectales resistentes a cetuximab cultivados en ratones a partir de tumores de pacientes (xenoinjertos derivados del paciente). Estos modelos eran todos tipo salvaje para KRAS, como las células LIM1215 originales, pero portaban mutaciones adicionales diversas, incluidas en BRAF y TP53, reflejando la variedad genética observada en la clínica. 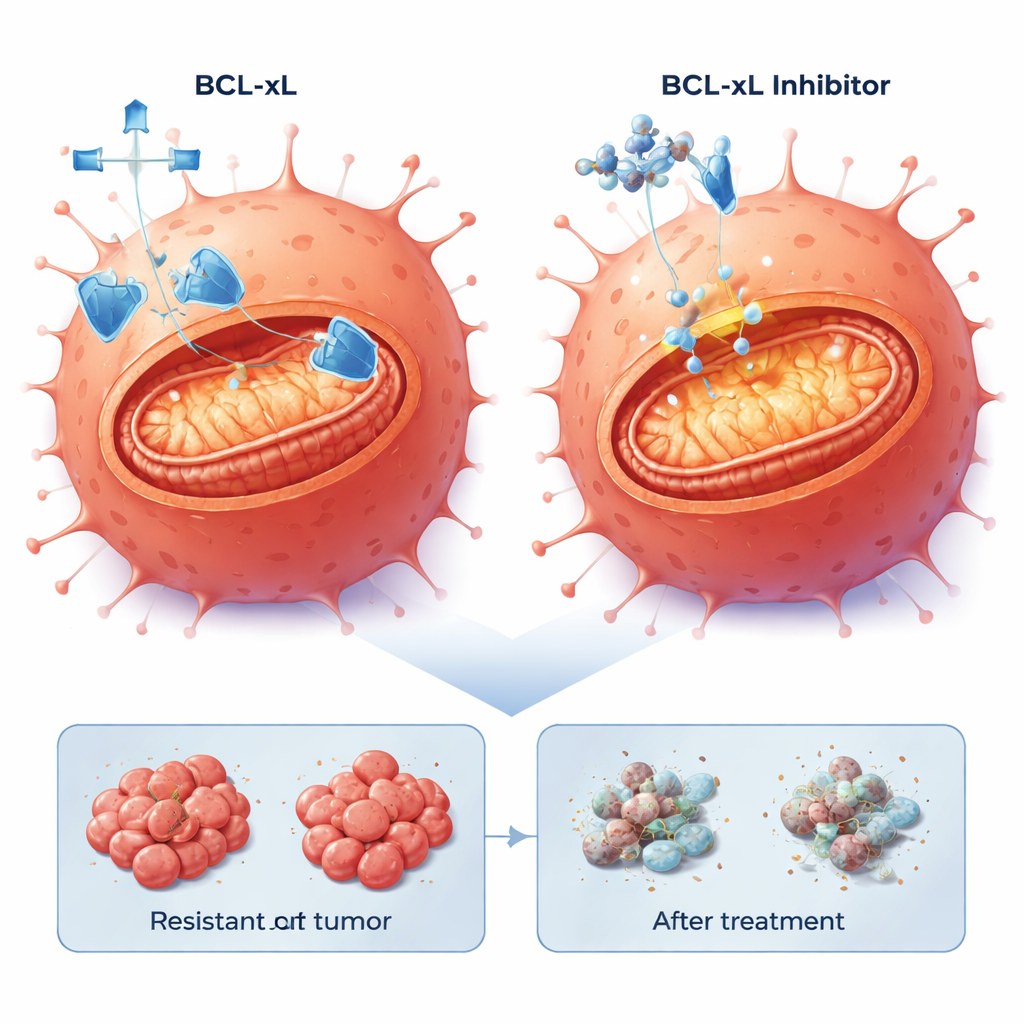
Apuntar a BCL-xL funciona en tumores resistentes diversos
En estos cortes tumorales derivados de pacientes, la combinación de un inhibidor de BCL-xL con bortezomib a baja dosis desencadenó de forma consistente una muerte celular robusta en el 20–40% de las células tumorales en cuatro modelos diferentes, incluidos aquellos con mutaciones BRAF agresivas. En cambio, bloquear MCL-1 con bortezomib produjo efectos fuertes solo en un subconjunto de tumores. Es importante que la capacidad de las células resistentes para sufrir apoptosis se conservara: una vez eliminado el “salvavidas” BCL-xL, el programa interno de muerte todavía podía activarse, independientemente de la ruta genética específica que el tumor hubiera adoptado para escapar del cetuximab.
Qué significa esto para los pacientes
Para las personas cuyo cáncer colorrectal deja de responder al cetuximab, este estudio ofrece un optimismo cauteloso. Sugiere que incluso después de que los tumores se vuelvan resistentes a la terapia dirigida contra EGFR, muchas células cancerosas siguen listas para morir si se bloquea una proteína clave de supervivencia, BCL-xL. Aunque los inhibidores de BCL-xL pueden tener efectos secundarios, especialmente sobre las plaquetas sanguíneas, el trabajo apunta a estrategias de combinación y optimización de dosis que podrían limitar la toxicidad mientras explotan un talón de Aquiles compartido por tumores difíciles de tratar. En el futuro, los fármacos que desactiven BCL-xL podrían formar la columna vertebral de nuevos tratamientos de segunda línea para el cáncer colorrectal refractario a cetuximab, menos dependientes del paisaje mutacional cambiante del tumor.
Cita: Asmanidou, S., Thiel, J., Ekstrom, T.L. et al. BCL-xL as a therapeutic target in cetuximab-refractory colorectal cancer. Cell Death Dis 17, 187 (2026). https://doi.org/10.1038/s41419-026-08434-5
Palabras clave: cáncer colorrectal, resistencia a fármacos, cetuximab, inhibición de BCL-xL, apoptosis