Clear Sky Science · es
LAP2α impulsa la tumorigénesis mamaria al mitigar el estrés de replicación
Por qué esto importa para el cáncer de mama
Los tumores mamarios crecen en parte porque las células cancerosas encuentran maneras de sobrevivir al estrés constante mientras copian su ADN. Este estudio revela cómo una proteína menos conocida, denominada LAP2α, ayuda a las células de cáncer de mama a proteger su ADN durante la replicación, favoreciendo así el crecimiento tumoral y dificultando el tratamiento. Comprender este sistema de apoyo oculto sugiere nuevas vías para debilitar los tumores y mejorar el efecto de los fármacos existentes.
Un ayudante oculto dentro de los núcleos de las células tumorales
Cada vez que una célula se divide, debe copiar su ADN con precisión. En las células cancerosas, este proceso está especialmente tensionado: las señales de crecimiento permanecen en posición de “activado” y la maquinaria de replicación se lleva al límite. Esta presión, conocida como estrés de replicación, deja tramos de ADN monocatenario que deben ser rápidamente recubiertos y estabilizados por un complejo proteico llamado RPA. Los autores ya habían descubierto que LAP2α, una proteína vinculada al armazón interno del núcleo, puede unirse a RPA y ayudarle a alcanzar el ADN dañado. En el trabajo actual se plantearon si esta asociación LAP2α–RPA realmente impulsa el desarrollo de tumores mamarios y afecta la respuesta de los tumores al tratamiento.
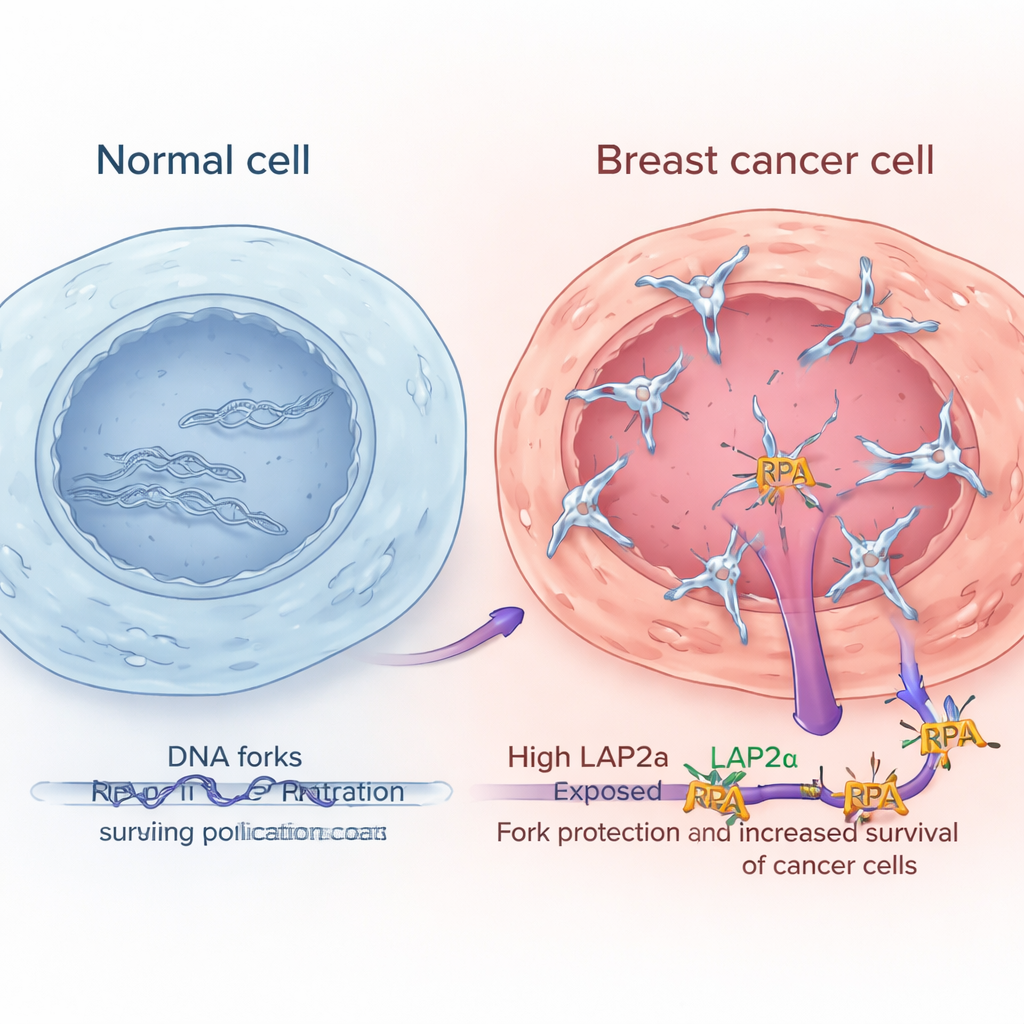
Niveles altos de LAP2α señalan tumores mamarios más agresivos
Mediante el análisis de grandes conjuntos públicos de expresión génica y el examen de muestras tumorales al microscopio, los investigadores mostraron que LAP2α es consistentemente más abundante en tejido de cáncer de mama que en el tejido mamario normal adyacente. Sus niveles aumentan con el grado tumoral, lo que significa que los cánceres más anormales y agresivos tienden a presentar más LAP2α. Este patrón apareció en varios subtipos principales de cáncer de mama, incluidos los positivos para receptores hormonales, los enriquecidos en HER2 y los triple negativos. Importante para los pacientes, aquellos cuyos tumores mostraban alta expresión de LAP2α tendieron a tener peores supervivencias. En contraste, los componentes centrales de RPA en sí no mostraron cambios similares ni vínculos claros con el pronóstico, lo que sugiere que es la función potenciada de LAP2α, más que un aumento simple de RPA, la que ayuda a las células cancerosas a sobrellevar mejor el estrés de replicación.
Apagar LAP2α frena los tumores y expone puntos débiles
Para ir más allá de las correlaciones, el equipo empleó modelos de ratón de cáncer de mama en los que LAP2α podía eliminarse selectivamente. Una vez formados los tumores mamarios, la eliminación genética de LAP2α provocó un crecimiento tumoral más lento y prolongó la supervivencia de los animales. Las células tumorales sin LAP2α se dividían menos y mostraban más signos de daño en el ADN, evidenciado por un aumento en el marcado de marcadores de rotura de ADN y una reducción del recubrimiento de RPA sobre el ADN. Cuando estas células tumorales deficientes en LAP2α se trasplantaron a nuevos ratones, de nuevo formaron tumores más pequeños y mostraron mayor sensibilidad a quimioterapias que dañan el ADN, incluido el platino cisplatino y un inhibidor de PARP. Experimentos similares en líneas celulares humanas de cáncer de mama confirmaron que reducir LAP2α hacía a las células más vulnerables a varios fármacos genotóxicos, mientras que restaurar LAP2α normal—pero no una forma mutante que no puede unirse a RPA—rescataba tanto la protección del ADN como la resistencia a los fármacos.
Cómo LAP2α ayuda a proteger las hebras de ADN frágiles
Para diseccionar el mecanismo, los investigadores recrearon los pasos de unión al ADN en ensayos de tubo de ensayo. Mezclaron RPA purificada, ADN monocatenario y bien LAP2α normal o una variante incapaz de interactuar con RPA. Encontraron que LAP2α aumentaba directamente la eficiencia con la que RPA recubría el ADN monocatenario y ayudaba a RPA a estirar y estabilizar estas regiones frágiles, actuando en gran medida como un facilitador o chaperón de carga. Cuando el ADN estaba presente, RPA tendía a desprenderse de LAP2α y comprometerse plenamente a unirse a la hebra simple, lo que muestra que LAP2α no forma parte de la capa protectora final sino que entrega RPA al ADN. Sin una interacción funcional LAP2α–RPA, más forquillas de replicación colapsaron, se acumularon roturas de ADN y las células cancerosas eran más propensas a morir, especialmente cuando la quimioterapia inducía daño adicional.
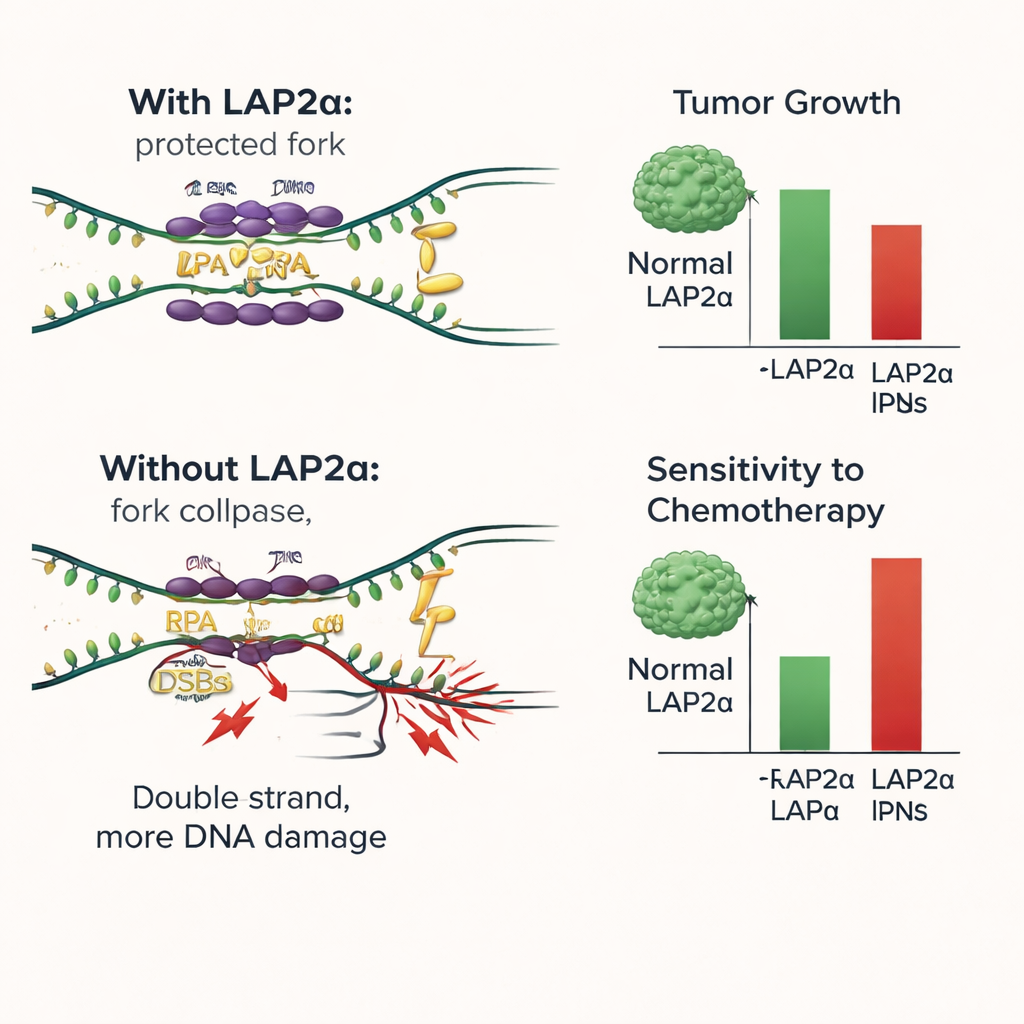
Qué implica esto para el tratamiento futuro del cáncer de mama
En términos sencillos, este estudio muestra que LAP2α actúa como un asistente entre bastidores que ayuda a las células de cáncer de mama a sobrevivir la tensión de copiar su ADN. Al cargar eficazmente RPA sobre el ADN vulnerable, LAP2α reduce el daño y sostiene el crecimiento tumoral continuado. Eliminar o desactivar LAP2α inclina la balanza: el daño en el ADN se acumula, las células dejan de dividirse y los fármacos convencionales que atacan el ADN se vuelven más efectivos. Estos hallazgos sugieren que LAP2α podría usarse como marcador de mal pronóstico y como nuevo objetivo terapéutico. Fármacos que bloqueen LAP2α o su unión a RPA podrían aumentar la eficacia de tratamientos existentes como agentes de platino e inhibidores de PARP, especialmente en tumores que dependen en gran medida de este sistema de amortiguación del estrés.
Cita: Ma, Y., Qin, Y., Bao, P. et al. LAP2α drives breast tumorigenesis by mitigating replication stress. Cell Death Dis 17, 201 (2026). https://doi.org/10.1038/s41419-026-08433-6
Palabras clave: cáncer de mama, estrés de replicación del ADN, LAP2 alfa, proteína de replicación A, sensibilidad a la quimioterapia