Clear Sky Science · es
Apuntar a la biosíntesis de glicerofosfolípidos supera la quimiorresistencia provocada por la pérdida de SLFN11 en el sarcoma de Ewing
Por qué esta investigación importa en el cáncer infantil
El sarcoma de Ewing es un cáncer poco frecuente pero agresivo que afecta mayoritariamente a niños y adolescentes. Muchos pacientes responden bien inicialmente a la quimioterapia, pero en los casos en que el cáncer reaparece, los tratamientos actuales a menudo fracasan. Este estudio plantea una pregunta urgente: cuando las células del sarcoma de Ewing se hacen resistentes a la quimioterapia, ¿qué cambios internos les permiten sobrevivir y pueden esas alteraciones convertirse en nuevas vulnerabilidades que los médicos puedan atacar?
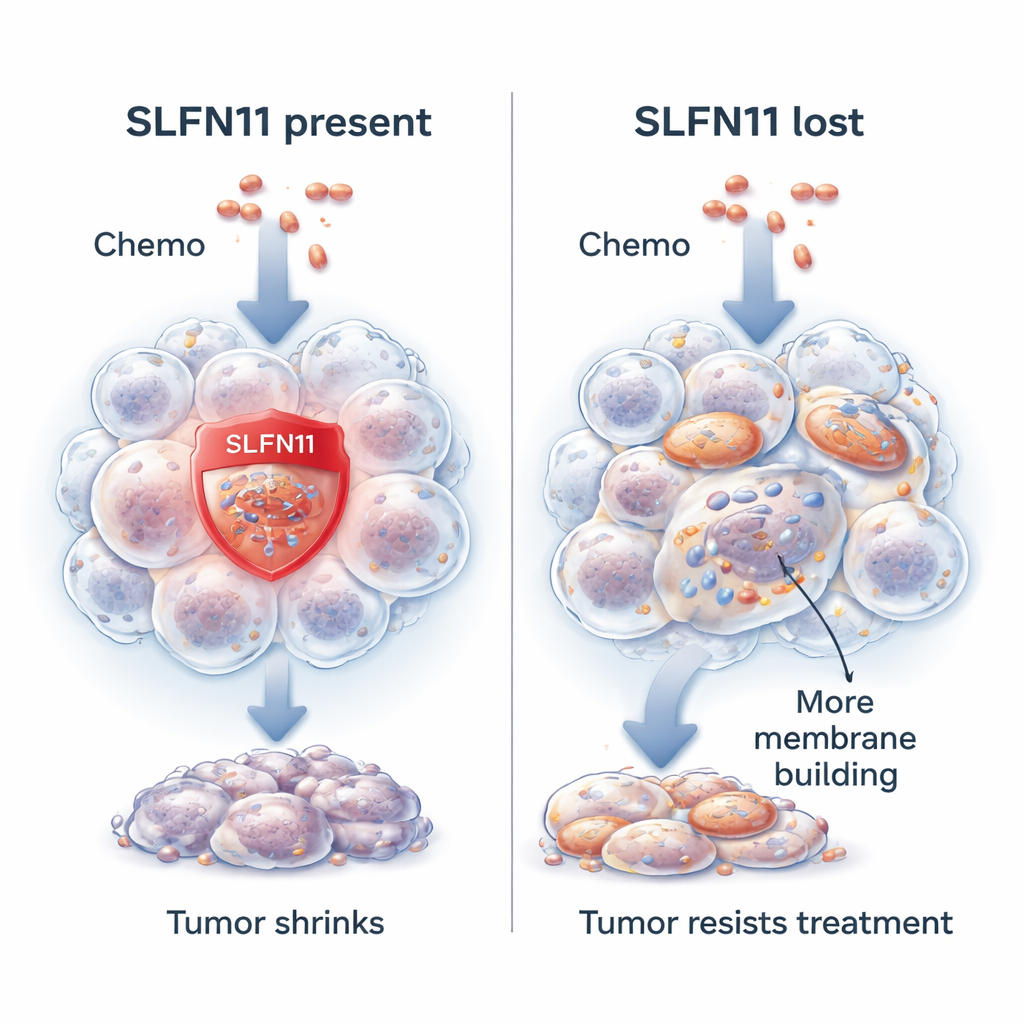
Un gen que facilita matar a las células cancerosas
Los investigadores se centran en un gen llamado SLFN11. En muchos tumores de sarcoma de Ewing, SLFN11 está muy activo y hace que las células cancerosas sean mucho más sensibles a fármacos que dañan el ADN, el plano genético de la célula. Cuando se administran estos fármacos, SLFN11 ayuda a bloquear la reparación del ADN y empuja a la célula cancerosa hacia la muerte. Los pacientes cuyos tumores tienen niveles más altos de SLFN11 tienden a vivir más y a responder mejor al tratamiento. Sin embargo, en aproximadamente uno de cada diez tumores, SLFN11 está ausente desde el inicio o se pierde durante el tratamiento. Cuando eso ocurre, la misma quimioterapia es mucho menos efectiva, aunque las células cancerosas siguen siendo perfectamente capaces de proliferar.
Cómo las células cancerosas reprograman su uso de combustible y grasas
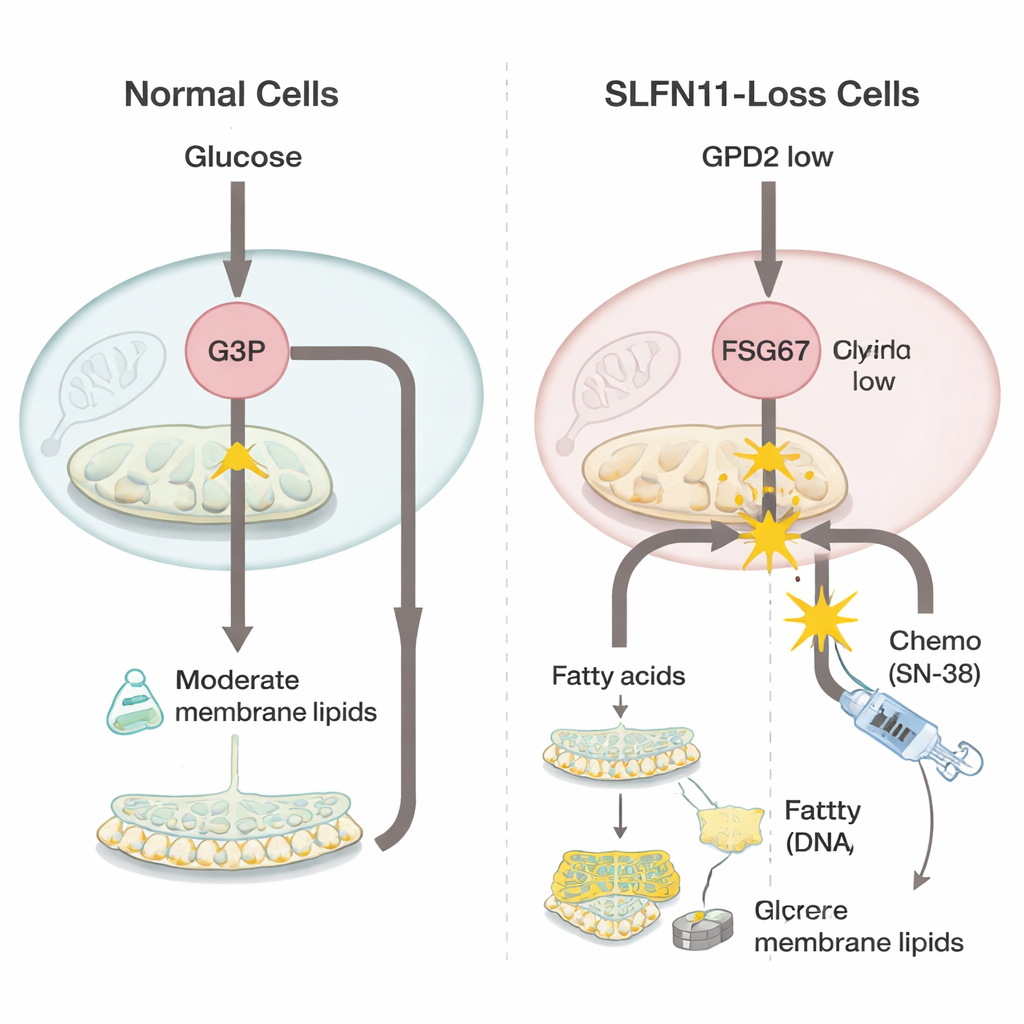
Para entender qué cambia cuando se pierde SLFN11, el equipo comparó células de sarcoma de Ewing con y sin este gen usando potentes herramientas “ómicas” que miden miles de genes y pequeñas moléculas a la vez. Descubrieron que las células carentes de SLFN11 reducen la expresión de una enzima mitocondrial llamada GPD2, que normalmente ayuda a oxidar una molécula llamada glicerol‑3‑fosfato como parte de la producción de energía. Cuando GPD2 está disminuida, el glicerol‑3‑fosfato se acumula. En lugar de desperdiciarse, este sustrato adicional se desvía hacia la síntesis de más moléculas grasas que forman las membranas celulares, un grupo conocido como glicerofosfolípidos. Las células también mostraron señales de producir grasas más flexibles y desaturadas, lo que puede ayudar a los tumores de rápido crecimiento a adaptarse al estrés.
Convertir un truco de supervivencia en un punto débil
Puesto que estas células deficientes en SLFN11 dependen más de la construcción de membranas, los científicos probaron si bloquear este proceso podría restaurar la sensibilidad a la quimioterapia. Utilizaron un compuesto llamado FSG67, que inhibe un paso clave en la producción de glicerofosfolípidos. Por sí solo, el fármaco estándar que daña el ADN, SN‑38, había perdido gran parte de su potencia en las células sin SLFN11, reflejando el problema clínico de la resistencia. Pero cuando SN‑38 se combinó con FSG67, las células previamente resistentes fueron mucho más afectadas, y los dos fármacos actuaron de forma sinérgica, mejor de lo esperado por sus efectos individuales. En contraste, en las células que conservaban SLFN11 y ya eran muy sensibles a SN‑38, añadir FSG67 aportó poco beneficio adicional e incluso pudo ser ligeramente contraproducente. Este patrón sugiere que la nueva dependencia de la síntesis de grasas y membranas es específica del estado resistente con bajos niveles de SLFN11.
Una posible señal no invasiva de tumores difíciles de tratar
Los investigadores se preguntaron luego si esta reprogramación metabólica podría detectarse en tumores reales, no solo en cultivos celulares. Hicieron crecer tumores de sarcoma de Ewing en ratones, con y sin SLFN11, y emplearon resonancia magnética nuclear (RMN) para examinar la composición química de los extractos tumorales. Los tumores sin SLFN11 mostraron una mayor proporción de dos moléculas que contienen colina vinculadas al recambio de membrana: fosfocolina y glicerofosfocolina. Una alta relación fosfocolina/glicerofosfocolina se ha asociado en otros cánceres con un comportamiento más agresivo y peor respuesta al tratamiento. Dado que las señales de colina pueden medirse con técnicas de imagen avanzadas, este tipo de cambio podría algún día servir como marcador no invasivo para identificar tumores de sarcoma de Ewing que han adoptado este modo resistente centrado en la construcción de membranas.
Qué podría significar esto para tratamientos futuros
En conjunto, el estudio muestra que cuando las células de sarcoma de Ewing pierden SLFN11 y se vuelven menos sensibles a la quimioterapia que daña el ADN, compensan reprogramando su metabolismo hacia la síntesis de más lípidos de membrana. Este cambio no solo ayuda a las células a sobrevivir; además crea un nuevo talón de Aquiles. Bloquear la producción de glicerofosfolípidos con un fármaco como FSG67 puede restaurar en parte la capacidad letal de la quimioterapia en estas células resistentes. Aunque FSG67 en sí no es aún un fármaco clínico, el trabajo apunta a una estrategia en la que los médicos podrían en el futuro clasificar los tumores según el estado de SLFN11 y sus rasgos metabólicos, y luego combinar terapias que dañen el ADN con inhibidores dirigidos de la síntesis de grasas y membranas para superar la resistencia.
Cita: Chakraborty, K., Burman, R., Satheesh, S. et al. Targeting glycerophospholipid biosynthesis overcomes chemoresistance driven by SLFN11 loss in Ewing sarcoma. Cell Death Dis 17, 190 (2026). https://doi.org/10.1038/s41419-026-08432-7
Palabras clave: Sarcoma de Ewing, quimiorresistencia, SLFN11, metabolismo del cáncer, biosíntesis de lípidos