Clear Sky Science · es
Modulación de células inmunitarias y reprogramación metabólica en la efierocitosis
Cómo nuestro cuerpo limpia en silencio las células moribundas
Cada día, miles de millones de nuestras células llegan al final de su vida. Sin embargo, no sentimos ese recambio microscópico, ni enfermamos por los restos. Esta limpieza silenciosa la realizan células inmunitarias y tisulares que reconocen y engullen células en proceso de morir, evitando inflamación perjudicial. La revisión analizada explica cómo este proceso de limpieza, denominado efierocitosis, no solo mantiene los tejidos ordenados, sino que también reconfigura el metabolismo de las células encargadas de limpiar, influyendo en si nuestro sistema inmune se calma, combate una infección o —si algo falla— contribuye a la enfermedad.
Los recolectores silenciosos del cuerpo
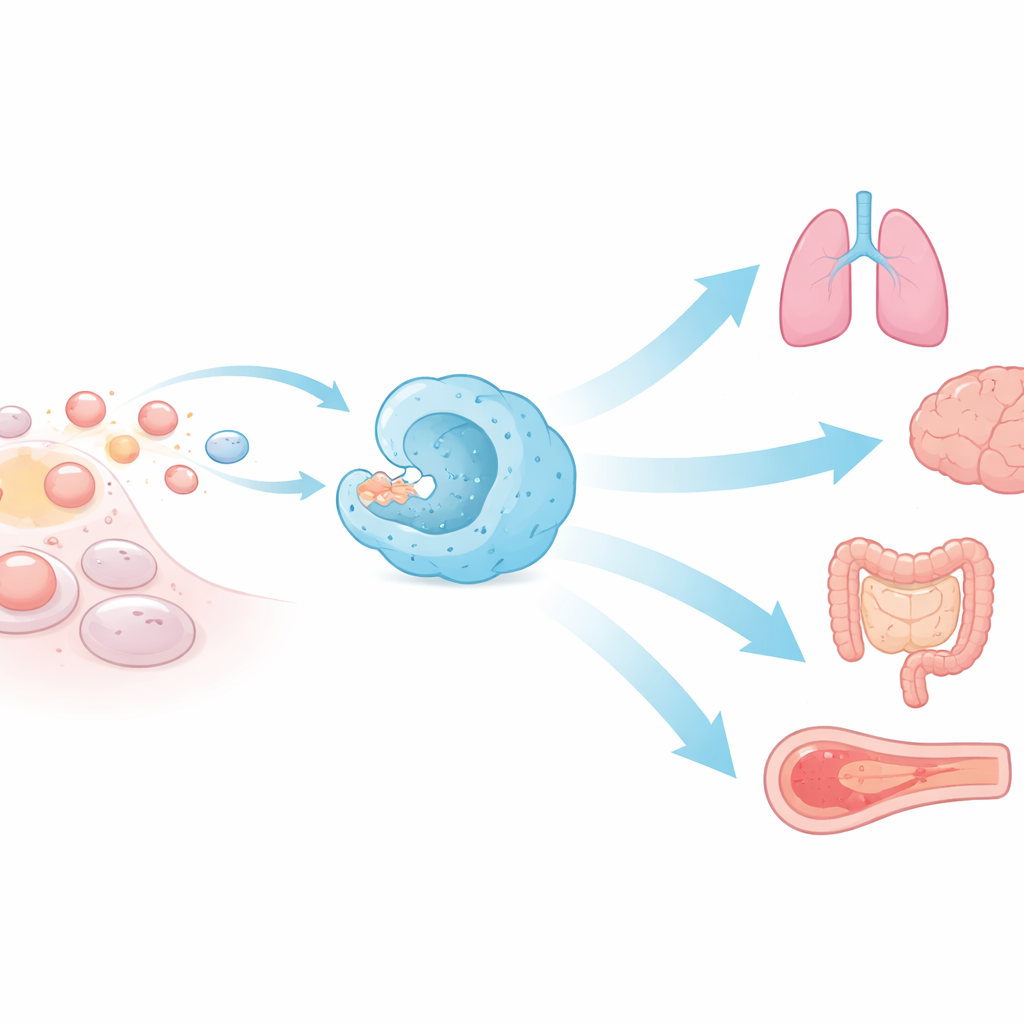
Efierocitosis es el nombre que recibe la captura y eliminación de células apoptóticas, o que mueren por programas celulares. Células inmunitarias especializadas, conocidas como macrófagos y células dendríticas, realizan la mayor parte de este trabajo, pero muchas células no inmunitarias —como las epiteliales del intestino, pulmón, ojo y testículos— también pueden intervenir. Las células moribundas emiten señales químicas de “búscame” que atraen a los fagocitos cercanos, luego muestran banderas de “cómeme” en su superficie mientras apagan las señales de “no me comas”. Una vez reconocidas, se envuelven en un bolsillo de membrana, se introducen y se degradan en compartimentos llenos de enzimas. Esta coreografía rápida y en varios pasos explica por qué las células apoptóticas rara vez se ven al microscopio a pesar de la enorme pérdida celular diaria.
Una limpieza que protege los órganos
Una efierocitosis eficiente protege la estructura y función de muchos órganos. En el ojo, la incapacidad de las células retinianas para eliminar fragmentos de fotorreceptores en descomposición conduce a la pérdida de visión. En los testículos, la mala eliminación de células germinales moribundas puede causar infertilidad. Durante el embarazo, la efierocitosis de células placentarias favorece la tolerancia materna al amortiguar moléculas inflamatorias y aumentar las señales calmantes. En el cerebro, la microglía poda neuronas en exceso y apoya un cableado sano, mientras que en el intestino, las células de Paneth y otros fagocitos limpian las células moribundas para prevenir inflamación intestinal crónica. En los pulmones, los macrófagos de las vías aéreas eliminan continuamente células muertas, evitando la liberación de señales de peligro que pueden impulsar asma, enfermedad pulmonar obstructiva crónica o daño viral severo.
Cuando las infecciones convierten la limpieza en un arma de doble filo
Durante las infecciones, la efierocitosis se vuelve más compleja. Los patógenos con frecuencia desencadenan la muerte celular, y el consiguiente engullimiento de cadáveres infectados puede debilitar o fortalecer la defensa del huésped. Algunos virus y bacterias explotan el lado antiinflamatorio de la efierocitosis para ocultarse del ataque inmune o para difundirse, usando las vesículas engullidas como “caballos de Troya”. En otros contextos, tragar células muertas e infectadas entrega fragmentos microbianos a macrófagos y células dendríticas, que luego presentan esos fragmentos a células T y movilizan respuestas inmunitarias protectoras. Dependiendo del microbio y del tejido, la efierocitosis puede sesgar a las células T colaboradoras hacia distintos perfiles inmunitarios, favoreciendo la eliminación bacteriana o, si se presentan moléculas propias junto a las microbianas, la aparición de células T autoreactivas que atacan los propios tejidos del organismo.
Combustible de los caídos: cómo se reconfigura el metabolismo
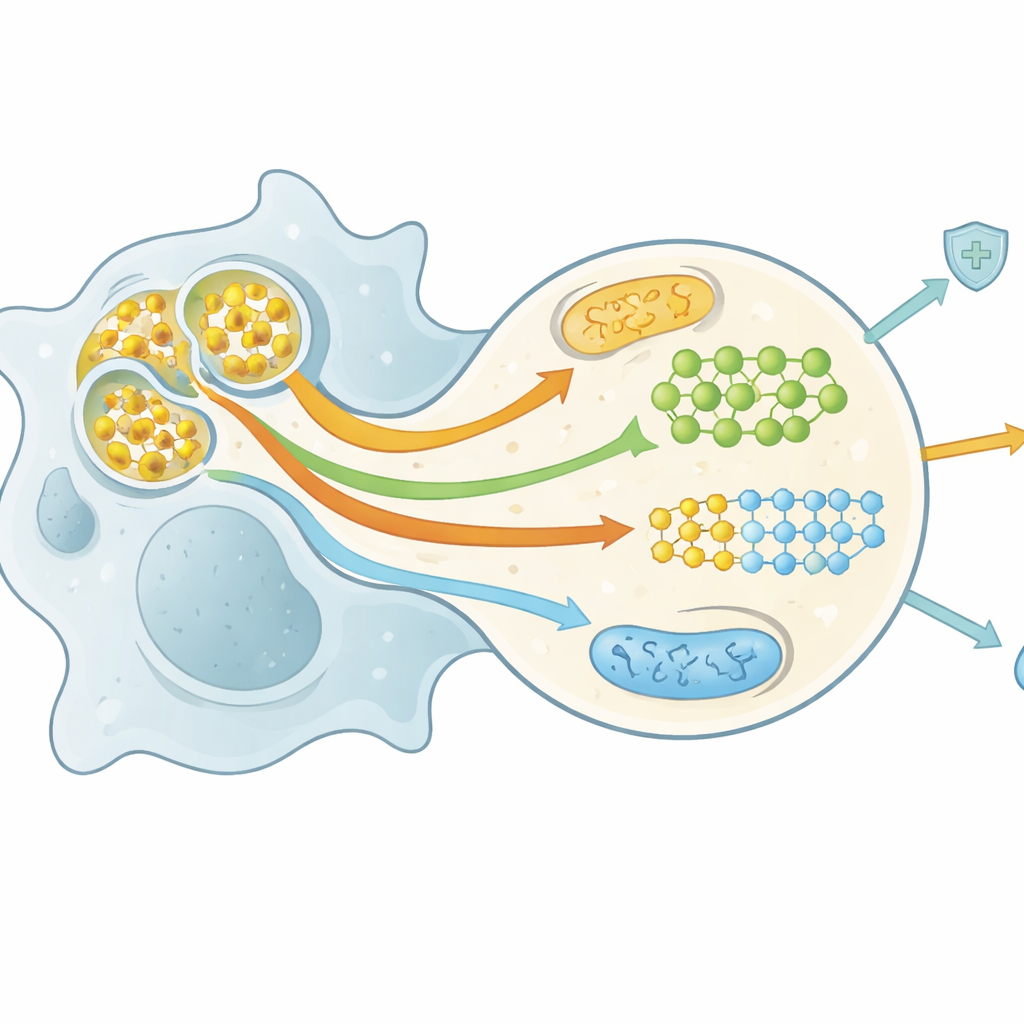
Degradar una célula entera exige mucha energía, pero también inunda al fagocito con nutrientes —lípidos, azúcares, aminoácidos y nucleótidos. Los autores describen un campo en crecimiento, a veces denominado efierometabolismo, que sigue cómo este aluvión de nutrientes reprograma el metabolismo de macrófagos y células dendríticas. Los lípidos de las células moribundas activan receptores nucleares que aumentan la exportación de colesterol, favorecen la oxidación mitocondrial de grasas y promueven un estado antiinflamatorio y de reparación tisular. Aminoácidos como arginina, metionina y triptófano se reciclan en moléculas que permiten rondas repetidas de engullimiento y desencadenan señales pro-resolutivas. Estallidos cortos de degradación de glucosa y rutas relacionadas suministran energía, mantienen el equilibrio redox y ayudan a conservar receptores y membranas en el estado adecuado para una limpieza continua. Estos cambios metabólicos entrelazados determinan si las células efierocíticas permanecen tolerantes, cambian a un modo reparador o conservan una fuerte actividad antimicrobiana.
Preguntas abiertas y vías terapéuticas futuras
La revisión destaca que no todos los efierocitos, o comedores celulares, se comportan igual. Las células inmunitarias profesionales y las células tisulares pueden depender de programas metabólicos distintos, y diferentes formas de muerte celular —como necrosis o ferroptosis— probablemente dejen huellas metabólicas e inmunitarias diferentes. Entre las incógnitas clave está cómo las señales mixtas procedentes de componentes propios y microbianos dentro de la misma célula moribunda moldean las vías energéticas y la inmunidad a largo plazo. Al mapear estos vínculos entre limpieza, metabolismo y destino inmunitario, los investigadores esperan diseñar terapias que orienten suavemente la efierocitosis: potenciándola para resolver inflamación crónica y ayudar en la reparación de heridas, o afinándola para preservar la fuerza antimicrobiana sin precipitar la autoinmunidad. En esencia, comprender cómo el cuerpo se nutre de sus propios desechos celulares podría desbloquear nuevas maneras de mantener el equilibrio saludable entre inflamación, infección y tolerancia.
Cita: Oliveira, K.C., Marcos, C.M., Penteado, L.d.A. et al. Modulation of immune cells and metabolic reprogramming in efferocytosis. Cell Death Dis 17, 257 (2026). https://doi.org/10.1038/s41419-026-08431-8
Palabras clave: efierocitosis, tolerancia inmunitaria, inmunidad innata, inmunometabolismo, inflamación crónica