Clear Sky Science · es
Dirigir la IGFBP2 exosomal en hipoxia supera la evasión inmune mediada por CD47 en glioblastoma
Por qué privar de oxígeno a los tumores puede salir contraproducente
Los médicos saben desde hace tiempo que el glioblastoma, un cáncer cerebral letal, suele crecer en regiones con escasez de oxígeno. Estos bolsillos hipóxicos dificultan el tratamiento del tumor. Este estudio revela cómo el bajo oxígeno ayuda a las células cancerosas a ocultarse del sistema inmunitario y sugiere una nueva terapia combinada que podría facilitar que el organismo las ataque.
Un tumor cerebral mortal que esquiva nuestras defensas
El glioblastoma es el tumor cerebral común más agresivo en adultos, con supervivencias típicamente medidas en meses. Aunque las células inmunitarias infiltran estos tumores, las células cancerosas con frecuencia evitan ser destruidas. Una vía clave de escape es una proteína de superficie llamada CD47, a veces denominada la señal de “no me comas”, que indica a células inmunitarias cercanas como los macrófagos que no fagociten ni destruyan la célula tumoral. Ya se están probando fármacos que bloquean CD47, pero los resultados en tumores sólidos como el glioblastoma han sido variables, lo que sugiere que otros factores del microambiente tumoral pueden estar minando estas terapias.
Zonas hipóxicas y pequeños paquetes cancerosos
Mediante secuenciación de ARN a nivel de célula única, los investigadores cartografiaron miles de células de distintas regiones de muestras de glioblastoma, comparando el núcleo hipoxémico del tumor con su borde exterior. Encontraron un subtipo celular particularmente agresivo en el núcleo hipóxico, denominado células GBM de tipo mesenquimal, que expresaba de forma marcada CD47 y una proteína llamada IGFBP2. Al mismo tiempo, descubrieron que estas células del núcleo liberaban gran número de vesículas de tamaño nanométrico conocidas como exosomas, que llevaban IGFBP2 en su superficie. Dado que los exosomas pueden viajar por el cerebro e incluso llegar al torrente sanguíneo, pueden difundir señales mucho más allá de su sitio de origen. 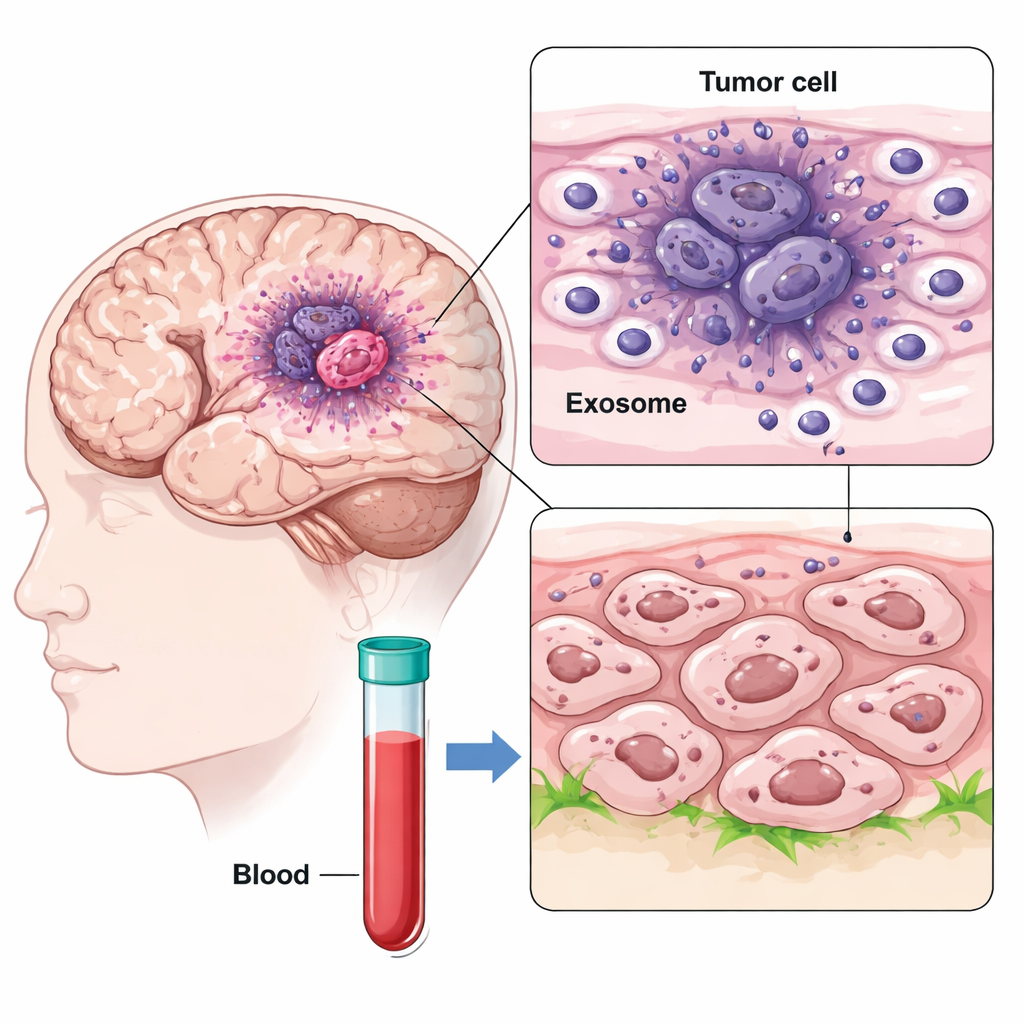
Cómo una proteína asociada potencia la señal de “no me comas”
El equipo investigó luego la función de IGFBP2. Demostraron que en condiciones de bajo oxígeno, una proteína sensor de hipoxia llamada HIF-2α activa el gen IGFBP2 en las células tumorales. IGFBP2 se une entonces a receptores específicos denominados integrinas en la superficie de los exosomas, decorando su membrana externa. Cuando estos exosomas recubiertos de IGFBP2 se fusionan con otras células tumorales, activan una cadena de señales intracelulares que involucra proteínas conocidas como FAK y STAT3. Esta cascada aumenta finalmente la cantidad de CD47 en la superficie de la célula tumoral, reforzando el mensaje de “no me comas” hacia los macrófagos y protegiendo aún más a las células cancerosas del ataque inmunitario. 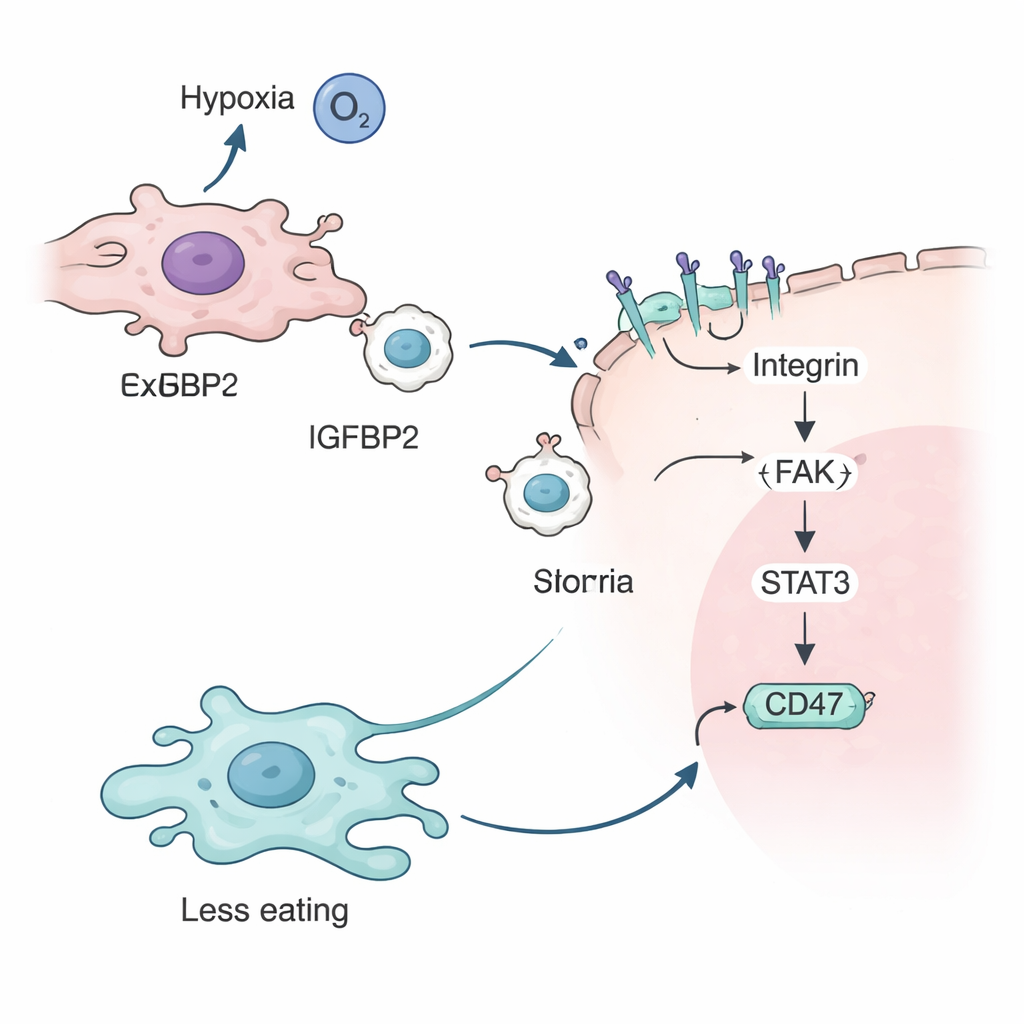
Pruebas en muestras de pacientes y modelos animales
Para vincular estos hallazgos de laboratorio con la enfermedad real, los investigadores examinaron tejido tumoral y sangre de personas con glioma. Encontraron que los niveles de IGFBP2 eran más elevados tanto en los tumores como en los exosomas sanguíneos de pacientes con enfermedad más avanzada, lo que sugiere que los exosomas positivos para IGFBP2 podrían servir como marcador en sangre del grado tumoral. En modelos murinos, reducir IGFBP2 en células de glioblastoma las hizo más vulnerables a la fagocitosis por macrófagos, ralentizó el crecimiento tumoral y prolongó la supervivencia. A la inversa, añadir exosomas ricos en IGFBP2 aumentó los niveles de CD47, redujo la fagocitosis por las células inmunitarias y aceleró la progresión tumoral.
Un prometedor golpe combinado para la terapia
Finalmente, el equipo probó si bloquear IGFBP2 podía mejorar la eficacia de la terapia dirigida a CD47. En ratones con tumores cerebrales, el tratamiento con anticuerpos contra IGFBP2 y CD47 condujo a una mayor actividad de los macrófagos, tumores de menor tamaño y una supervivencia más larga que cualquiera de los tratamientos por separado. Al cortar la señal impulsada por la hipoxia de IGFBP2 y bloquear directamente la señal de “no me comas” de CD47, esta terapia combinada atacó el camuflaje inmunitario del tumor desde dos frentes. Para los pacientes, estos hallazgos sugieren que medir IGFBP2 en exosomas sanguíneos podría ayudar a identificar a quienes tienen más probabilidades de beneficiarse de la inmunoterapia basada en CD47, y que combinar inhibidores de IGFBP2 y CD47 podría ser una estrategia más potente contra el glioblastoma que cualquiera de los fármacos por separado.
Cita: Qi, Y., Zhao, R., Zhang, X. et al. Targeting hypoxic exosomal IGFBP2 overcomes CD47-mediated immune evasion in glioblastoma. Cell Death Dis 17, 192 (2026). https://doi.org/10.1038/s41419-026-08430-9
Palabras clave: glioblastoma, exosomas, evasión inmune, CD47, hipoxia