Clear Sky Science · es
HSPA5 promueve la estabilidad de YAP/TAZ independientemente de la vía Hippo e induce la transición proneuronal a mesenquimal en glioblastoma
Por qué importa este estudio sobre cáncer cerebral
El glioblastoma es uno de los cánceres cerebrales más letales, en parte porque muchos tumores evolucionan con el tiempo hacia un estado más resistente al tratamiento. Este estudio revela cómo una proteína común de respuesta al estrés, HSPA5, contribuye a impulsar ese cambio y mantiene vivos durante más tiempo de lo debido a moléculas que favorecen el tumor. Entender este "truco de supervivencia" sugiere nuevas formas de hacer que el glioblastoma sea menos agresivo y más sensible a las terapias existentes.
Un tumor que cambia de personalidad
Médicos y científicos reconocen ahora que el glioblastoma no es una sola enfermedad, sino una mezcla de subtipos moleculares. Dos variantes principales son la forma “proneuronal”, que suele ser algo menos agresiva, y la forma “mesenquimal”, que es más invasiva, más resistente al tratamiento y asociada a recaídas más precoces. Los tumores pueden evolucionar del estado proneuronal al mesenquimal, un proceso que los autores denominan transición proneuronal a mesenquimal, o PMT. El equipo se propuso descubrir qué proteínas de respuesta al estrés podrían estar impulsando a los tumores por este peligroso camino.
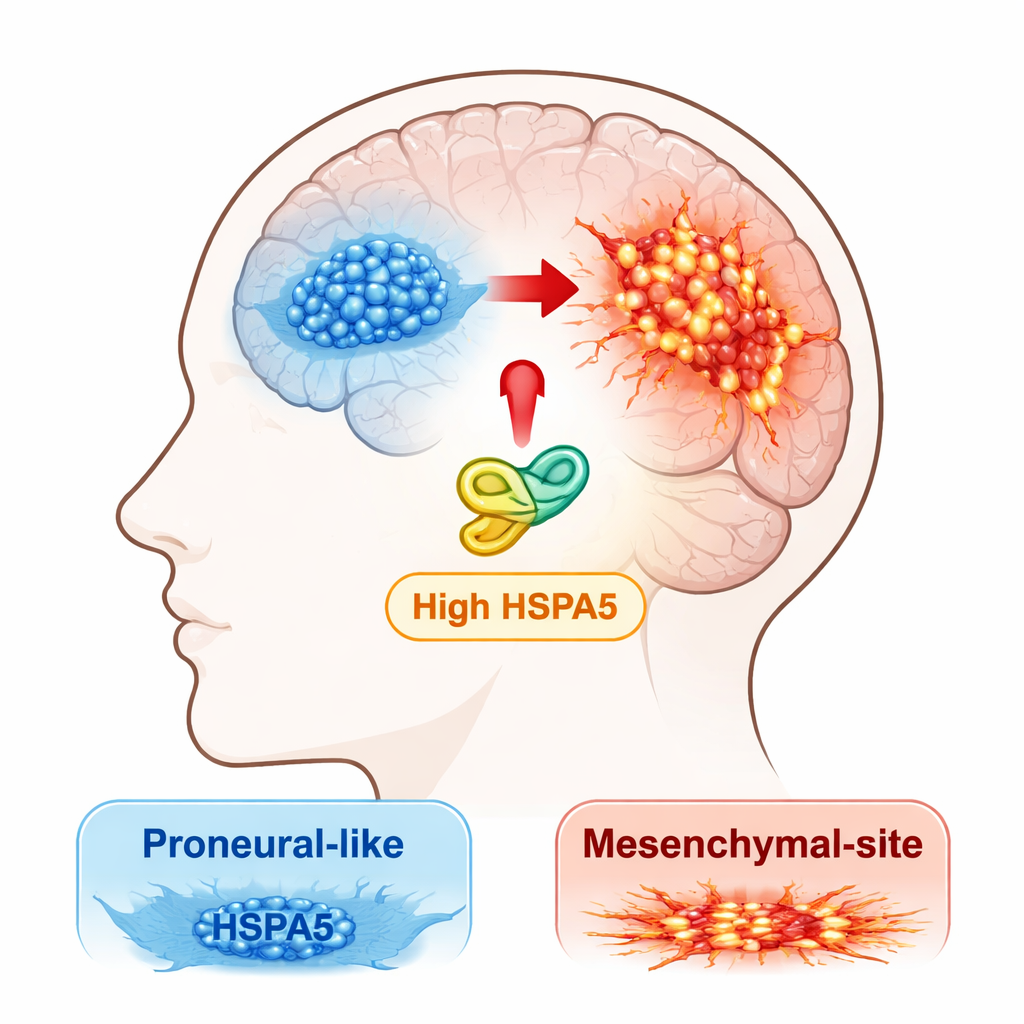
Una proteína auxiliar del estrés en el punto de mira
Los investigadores empezaron analizando grandes bases de datos públicas de cáncer y sus propias muestras de pacientes en busca de miembros de la familia HSP70, un grupo de proteínas “chaperonas” que ayudan a plegar y proteger otras proteínas bajo estrés. Una chaperona, HSPA5, destacó. Su actividad era máxima en el subtipo mesenquimal del glioblastoma y claramente mayor en los tumores que en el tejido cerebral normal. Los pacientes cuyos tumores mostraban más HSPA5 tendían a tener una supervivencia global peor, lo que la señala como un posible impulsor de la enfermedad agresiva en lugar de un mero acompañante.
Forzar a las células a volverse más agresivas
Para explorar qué hace realmente HSPA5 dentro de las células tumorales, el equipo cultivó células primarias de glioblastoma tomadas directamente de pacientes y las separó en grupos con rasgos proneuronales y mesenquimales. Cuando forzaron a las células proneuronales a producir más HSPA5, esas células empezaron a comportarse más como mesenquimales: proliferaban más rápido, migraban e invadían con mayor facilidad y activaban marcadores mesenquimales característicos como CD44 y c‑MET, mientras que reducían marcadores proneuronales como SOX2 y OLIG2. Lo contrario también ocurrió: disminuir los niveles de HSPA5 en células mesenquimales aminoró su crecimiento e invasividad y las empujó parcialmente hacia un perfil menos agresivo.
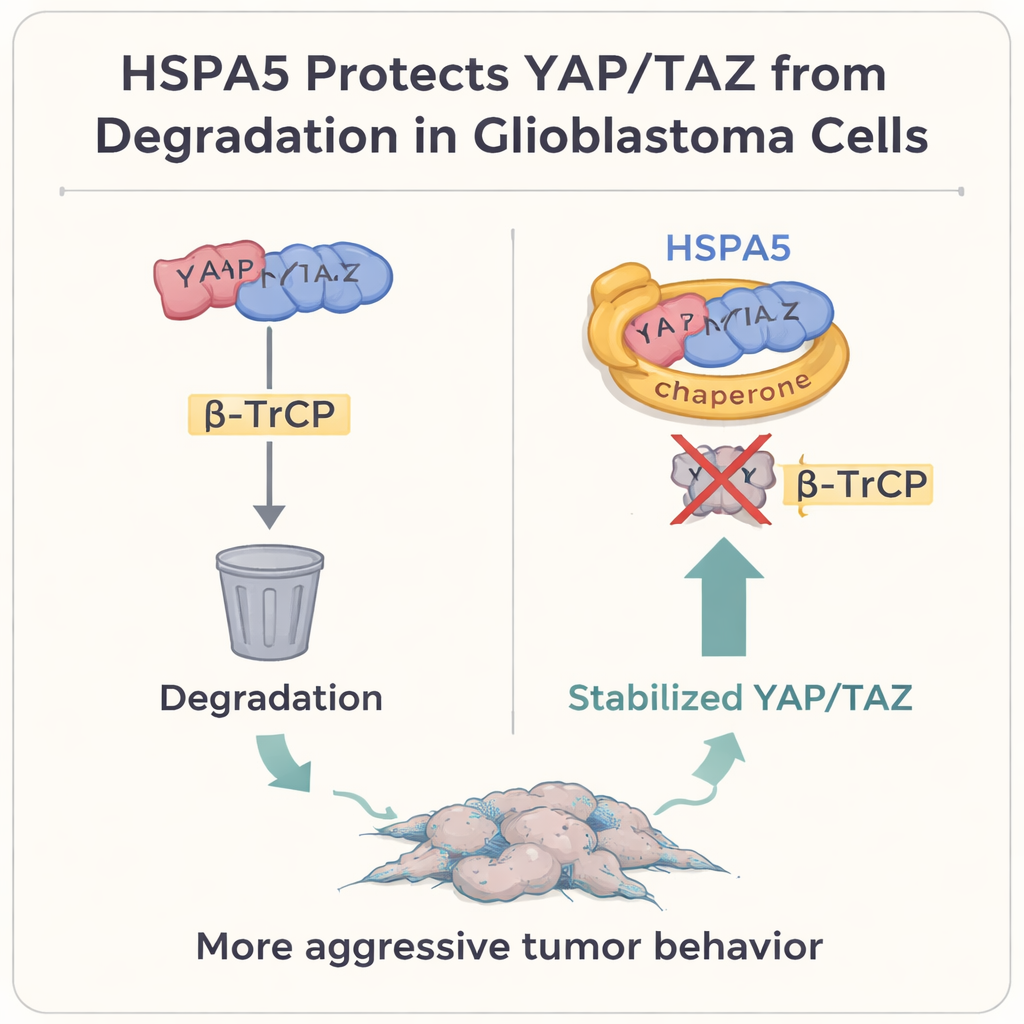
Protegiendo interruptores clave de crecimiento del “cubo de la basura” celular
Al profundizar, los autores se centraron en dos reguladores potentes del crecimiento, YAP y TAZ, que están en el núcleo de la vía de señalización Hippo. En muchos tumores sólidos, incluido el glioblastoma, estas proteínas actúan como conmutadores maestros que promueven el crecimiento celular, la plasticidad y el estado mesenquimal. Normalmente, cuando las células quieren frenar este programa, etiquetan a YAP y TAZ para su destrucción mediante una proteína llamada β‑TrCP, que las acompaña hasta la “basura” celular, el proteasoma. El estudio muestra que HSPA5 se une físicamente a YAP y TAZ, usando su dominio de unión a sustrato como un guante protector. Al hacerlo, impide que β‑TrCP se enganche, evita que YAP/TAZ sean ubiquitinadas y degradadas, y permite que se acumulen en el núcleo donde activan genes mesenquimales, incluidos CD44 y c‑MET.
De placas de cultivo y ratones a tumores de pacientes
El equipo confirmó este mecanismo de varias maneras. Bloquear HSPA5 aceleró la desaparición de las proteínas YAP y TAZ, salvo si se inhibía químicamente el proteasoma, y aumentó las señales de “etiqueta de basura” sobre ellas. Reactivar YAP y TAZ rescató la pérdida de crecimiento e invasión observada al reducir HSPA5, mientras que silenciar YAP/TAZ eliminó los efectos pro‑tumorales de la sobreexpresión de HSPA5. En modelos murinos donde se implantaron células humanas de glioblastoma en el cerebro, los tumores con alta HSPA5 crecieron más y mataron a los animales antes; reducir HSPA5, o interrumpir su apoyo a YAP/TAZ, ralentizó el crecimiento y prolongó la supervivencia. Finalmente, en muestras humanas emparejadas tomadas de los mismos pacientes antes y después de la recidiva, los tumores recurrentes, más mesenquimales, mostraron niveles más altos de HSPA5, YAP, TAZ y marcadores mesenquimales que los tumores originales con rasgos proneuronales.
Qué significa esto para el tratamiento futuro del cáncer cerebral
En términos sencillos, este trabajo sugiere que las células de glioblastoma explotan una ayuda de respuesta al estrés, HSPA5, para proteger interruptores cruciales de crecimiento (YAP y TAZ) de ser degradados. Esa protección ayuda a los tumores a cambiar y mantener una identidad más agresiva y resistente al tratamiento. Dado que ya existen inhibidores de pequeña molécula contra HSPA5 y las células tumorales pueden depender más de esta chaperona que las células normales, el eje HSPA5–YAP/TAZ ofrece un objetivo terapéutico atractivo. Terapias que debiliten este escudo protector podrían hacer a las células de glioblastoma menos adaptables, menos invasivas y más vulnerables a tratamientos estándar como la quimioterapia y la radioterapia.
Cita: Gui, S., Yu, W., Song, Z. et al. HSPA5 promotes YAP/TAZ stability independently of the Hippo pathway and induces proneural-to-mesenchymal transition in glioblastoma. Cell Death Dis 17, 208 (2026). https://doi.org/10.1038/s41419-026-08428-3
Palabras clave: glioblastoma, HSPA5, YAP/TAZ, plasticidad tumoral, transición mesenquimal