Clear Sky Science · es
El arresto del ciclo celular G0/G1 mediado por p16 conduce a SASP y fibrosis en la dystrofia endotelial corneal de Fuchs
Por qué importa esta enfermedad ocular
A medida que envejecen, una de las amenazas menos conocidas para la visión es una afección llamada dystrofia endotelial corneal de Fuchs (FECD), que nubla lentamente la ventana frontal normalmente transparente del ojo. Este artículo explora por qué ciertas células en la superficie interna de la córnea se desgastan y se fibrensan con el tiempo, y por qué las mujeres se ven afectadas con más frecuencia. Comprender estos cambios ocultos podría abrir la puerta a medicamentos que retrasen o incluso eviten la necesidad de trasplantes de córnea.
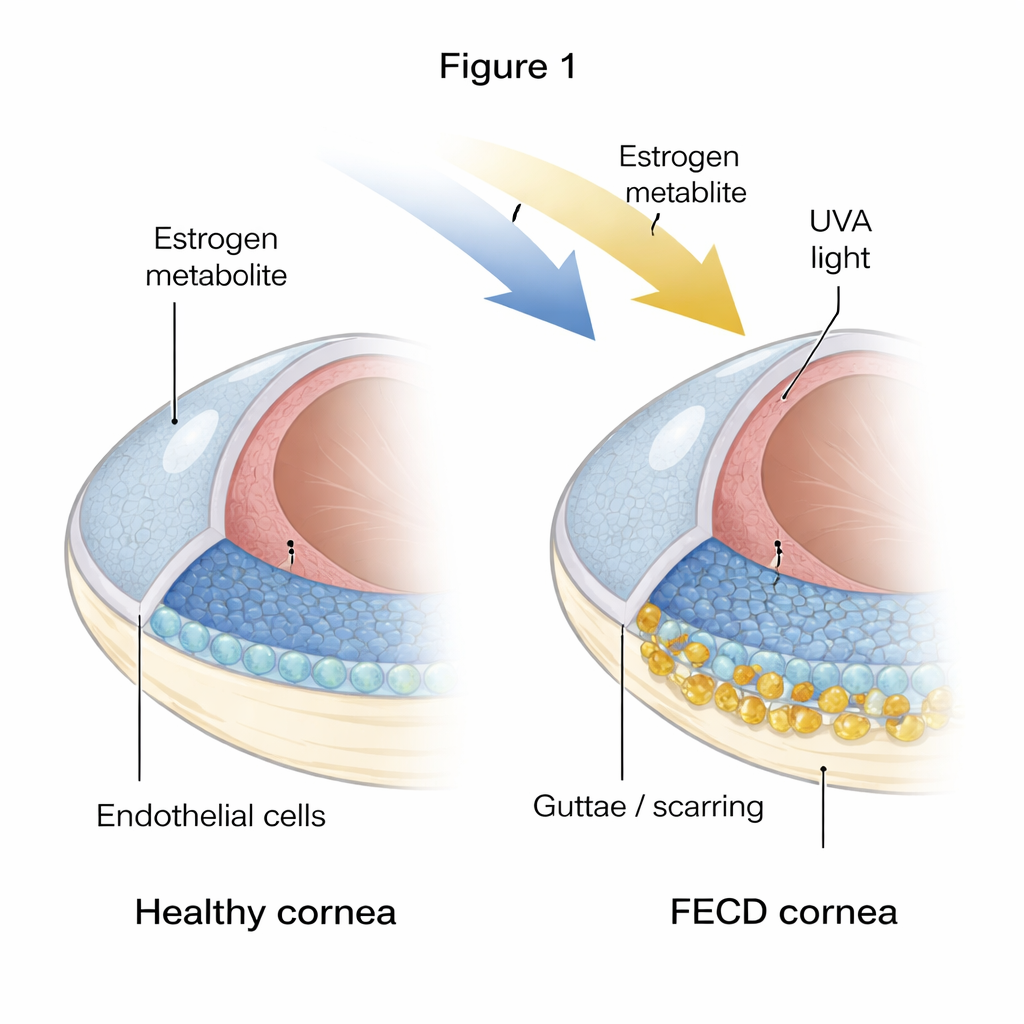
El frágil revestimiento interno de la córnea
La córnea debe mantenerse precisamente deshidratada para permanecer transparente, una tarea a cargo de una sola capa de células hexagonales llamadas células endoteliales corneales. En la FECD, muchas de estas células mueren y la capa se vuelve parcheada e irregular. Al mismo tiempo, aparecen protuberancias duras y material engrosado, conocidas como guttae y matriz extracelular en exceso, en la superficie interna. Los autores compararon córneas de donantes sanos con córneas de pacientes con FECD y encontraron fuertes indicios de que el tejido enfermo está tanto “envejecido” como fibrótico: las células mostraron marcadores de senescencia (un estado de parada permanente) y de fibrosis (células comportándose más como formadoras de cicatriz y depositando tejido extra).
El estrés crónico por luz y hormonas empuja a las células a un callejón sin salida
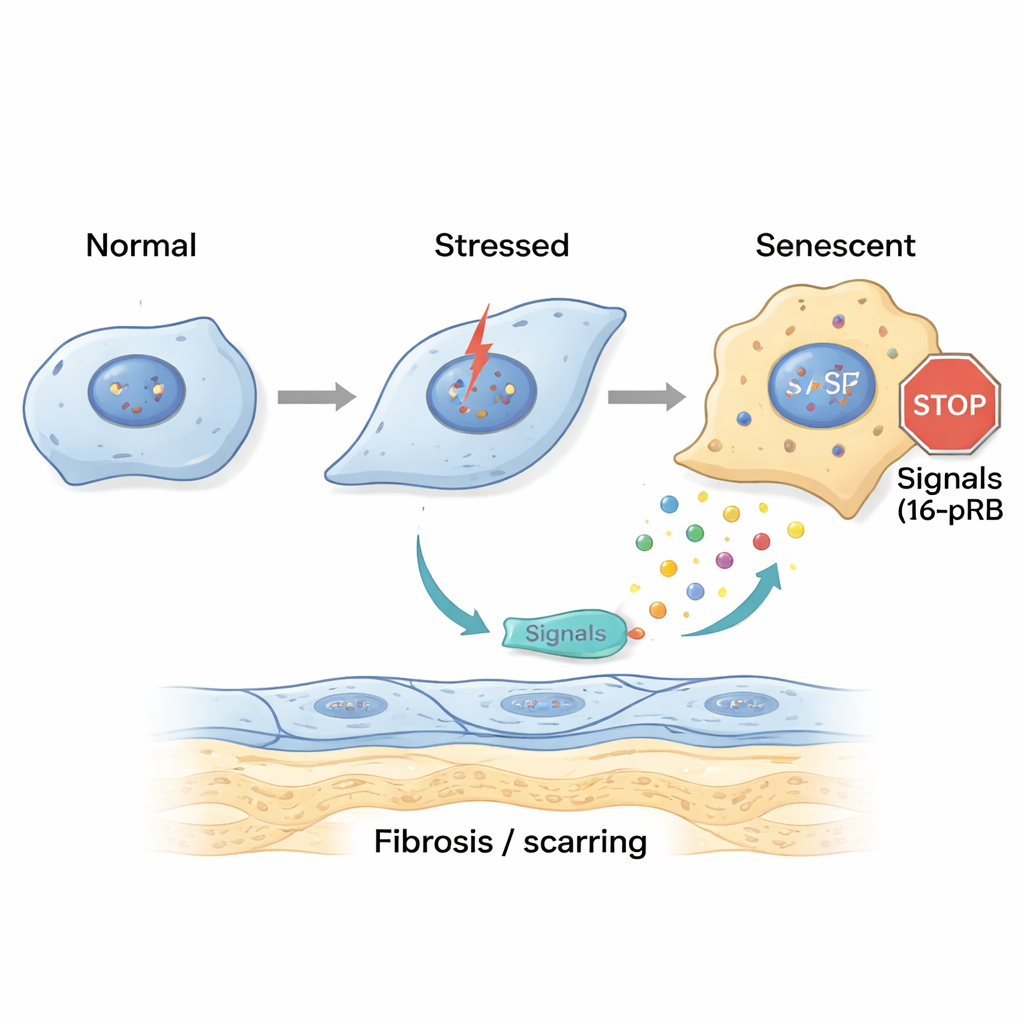
Para investigar cómo comienza este daño, los investigadores recrearon en el laboratorio un estrés similar al de la FECD. Expusieron células endoteliales corneales sanas a luz ultravioleta A (UVA) y a 4-hidroxiestradiol, un subproducto oxidado del estrógeno vinculado con daño en el ADN. Un golpe corto y único de estrés hizo que las células se detuvieran temporalmente en una fase tardía del ciclo celular y comenzaran una transición temprana hacia un estado más parecido a fibroblastos, pero todavía conservaban cierta capacidad de recuperación. En contraste, la exposición repetida y crónica llevó a las células a un estado diferente: se acumularon en una fase temprana del ciclo celular llamada G0/G1 y activaron un gen llamado p16, que bloquea el ciclo celular a través de su proteína asociada pRB. Estas células se volvieron grandes, planas e inequívocamente senescentes, al tiempo que expresaban fuertemente marcadores de fibrosis y proteínas que constituyen las guttae engrosadas en la FECD.
Las células senescentes envían señales dañinas y propagan la cicatrización
Las células senescentes no permanecen en silencio; secretan una mezcla de moléculas señalizadoras conocida como fenotipo secretor asociado a la senescencia (SASP). El equipo recogió el fluido de células corneales estresadas y lo aplicó a células nuevas y a córneas de donantes sanos. El SASP “agudo” provocó signos tempranos de cambio en la forma celular, mientras que el SASP “crónico” empujó a muchas células hacia la senescencia e incrementó genes vinculados a la fibrosis y a la deposición de matriz extra. Pruebas detalladas mostraron que el SASP crónico era rico en mensajeros inflamatorios como IL-8 e IL-17, conocidos por promover el envejecimiento celular, la cicatrización fibrótica y el reclutamiento de células inmunes. Cuando los investigadores bloquearon la vía de IL-17 o el receptor de IL-8 CXCR2, las células expuestas al SASP crónico mostraron menos marcadores de senescencia y menos fibrosis, lo que sugiere que estas señales son impulsores clave de la enfermedad.
Eliminar las células desgastadas para proteger la visión
Dado que las células senescentes p16-positivas estaban tan estrechamente vinculadas con la cicatrización, los autores probaron si eliminarlas podría proteger la córnea. En un modelo murino en el que la luz UVA desencadena cambios similares a la FECD, trataron a los animales con una combinación de fármacos senolíticos, Dasatinib más Quercetina, que mata selectivamente a las células senescentes. En comparación con los ratones no tratados, los tratados con senolíticos conservaron un mosaico endotelial más regular, preservaron más células en general y mostraron menos marcadores de senescencia, fibrosis y matriz en exceso. En otras palabras, eliminar las células más dañadas alivió la carga de secreciones nocivas y ayudó a mantener una superficie corneal más sana.
Qué significa esto para las personas con FECD
Para los pacientes, la FECD suele conducir actualmente a un trasplante de córnea cuando la visión se vuelve demasiado turbia. Este estudio sugiere un camino diferente: la enfermedad podría ser impulsada por una acumulación lenta de células estresadas y no divisorias que tanto no cumplen su función como envenenan activamente a sus vecinas con señales inflamatorias y fibróticas. Dirigirse a esas señales con fármacos contra las vías de IL-17 o IL-8, o usar terapias senolíticas para eliminar selectivamente las células más dañadas, podría algún día retrasar la fibrosis, preservar más tejido natural del ojo y posponer o reducir la necesidad de cirugía.
Cita: Parekh, M., Adhikari, Y., Deshpande, N. et al. p16-mediated G0/G1 cell cycle arrest leads to SASP and fibrosis in Fuchs endothelial corneal dystrophy. Cell Death Dis 17, 197 (2026). https://doi.org/10.1038/s41419-026-08425-6
Palabras clave: distrofia de Fuchs, endotelio corneal, senescencia celular, fibrosis, terapia senolítica