Clear Sky Science · es
El ADN mitocondrial impulsa la activación del eje NLRP3-IL-1β en microglía al unirse a NLRP3, conduciendo a neurodegeneración en modelos de enfermedad de Parkinson
Por qué esto importa para la enfermedad de Parkinson
La enfermedad de Parkinson es conocida sobre todo por los temblores y la lentitud del movimiento, pero bajo esos síntomas se libra una batalla compleja dentro del cerebro. Este estudio descubre cómo pequeños fragmentos de material genético procedentes de mitocondrias dañadas en las células inmunitarias del cerebro pueden encender inflamación que, de forma gradual, mata a las neuronas productoras de dopamina necesarias para el movimiento fluido. Comprender esta reacción en cadena abre nuevos objetivos de fármacos muy específicos que podrían ralentizar o prevenir el daño similar al Parkinson.
Células inmunitarias cerebrales y centrales energéticas bajo estrés
El cerebro contiene no solo neuronas sino también microglía, sus células inmunitarias residentes. En la enfermedad de Parkinson, estas microglías a menudo se sobreactivan, liberando moléculas tóxicas y señales inflamatorias que dañan a las neuronas cercanas. Los autores se centraron en las mitocondrias, las “centrales energéticas” de las células, que poseen su propio ADN. Cuando las mitocondrias se lesionan —por toxinas, envejecimiento u otros estreses— su ADN puede oxidarse, un tipo de daño químico causado por especies reactivas de oxígeno. Debido a que el ADN mitocondrial se parece al ADN bacteriano, estos fragmentos dañados pueden actuar como señales de alarma dentro del cerebro, alertando al sistema inmune y potencialmente impulsando una inflamación crónica.
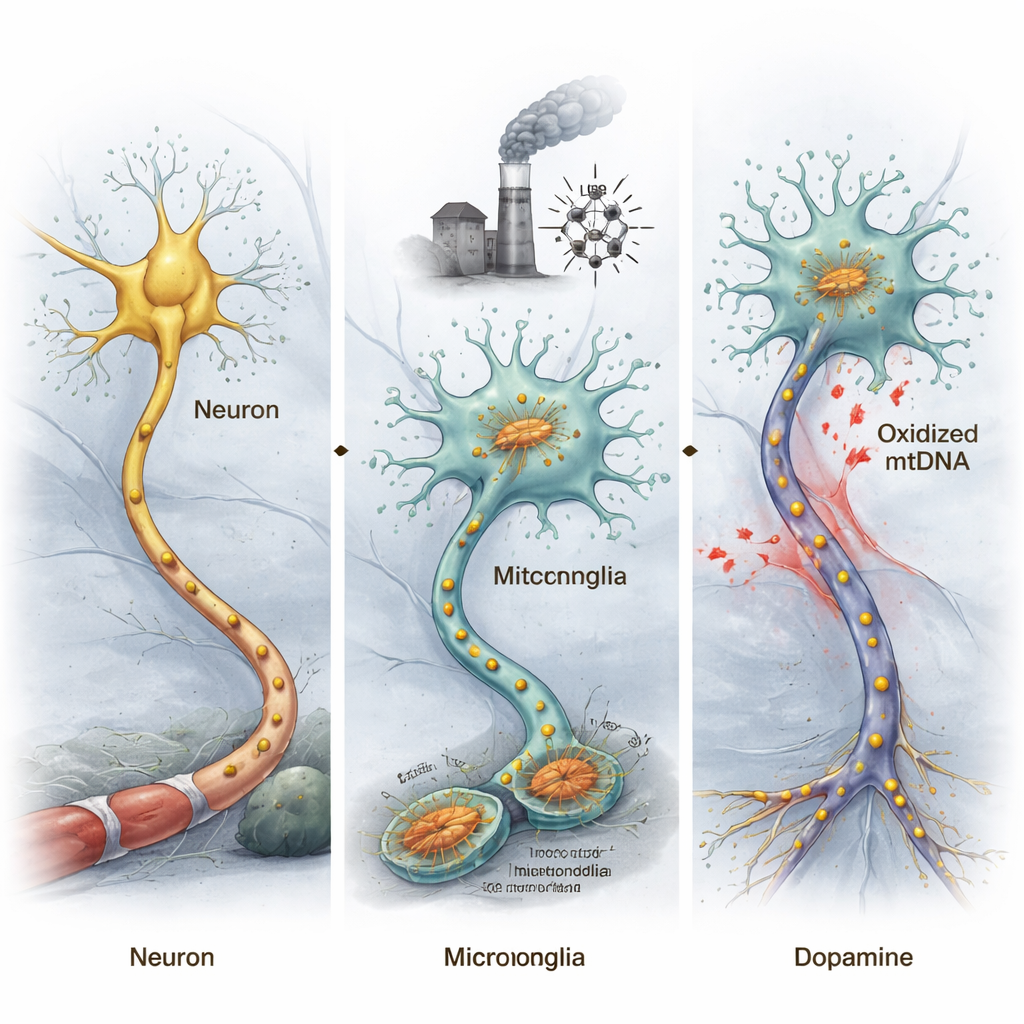
El ADN mitocondrial dañado puede empujar a ratones hacia una enfermedad similar al Parkinson
Para probar si el ADN mitocondrial oxidado (ox-mtDNA) puede realmente desencadenar cambios parecidos al Parkinson, los investigadores extrajeron ox-mtDNA de microglías estresadas e inyectaron ese material directamente en una región cerebral que normalmente contiene neuronas productoras de dopamina importantes para el movimiento. Los ratones expuestos a este ox-mtDNA mostraron reducción del movimiento en pruebas conductuales y pérdida de estas neuronas dopaminérgicas, reproduciendo rasgos centrales de la enfermedad de Parkinson. Al separar neuronas y microglías del mesencéfalo y analizar su actividad génica, el equipo halló que los genes vinculados a Parkinson se volvieron más anómalos en las neuronas, mientras que los genes relacionados con la inflamación se activaron con fuerza en las microglías.
Un interruptor molecular de alarma dentro de la microglía
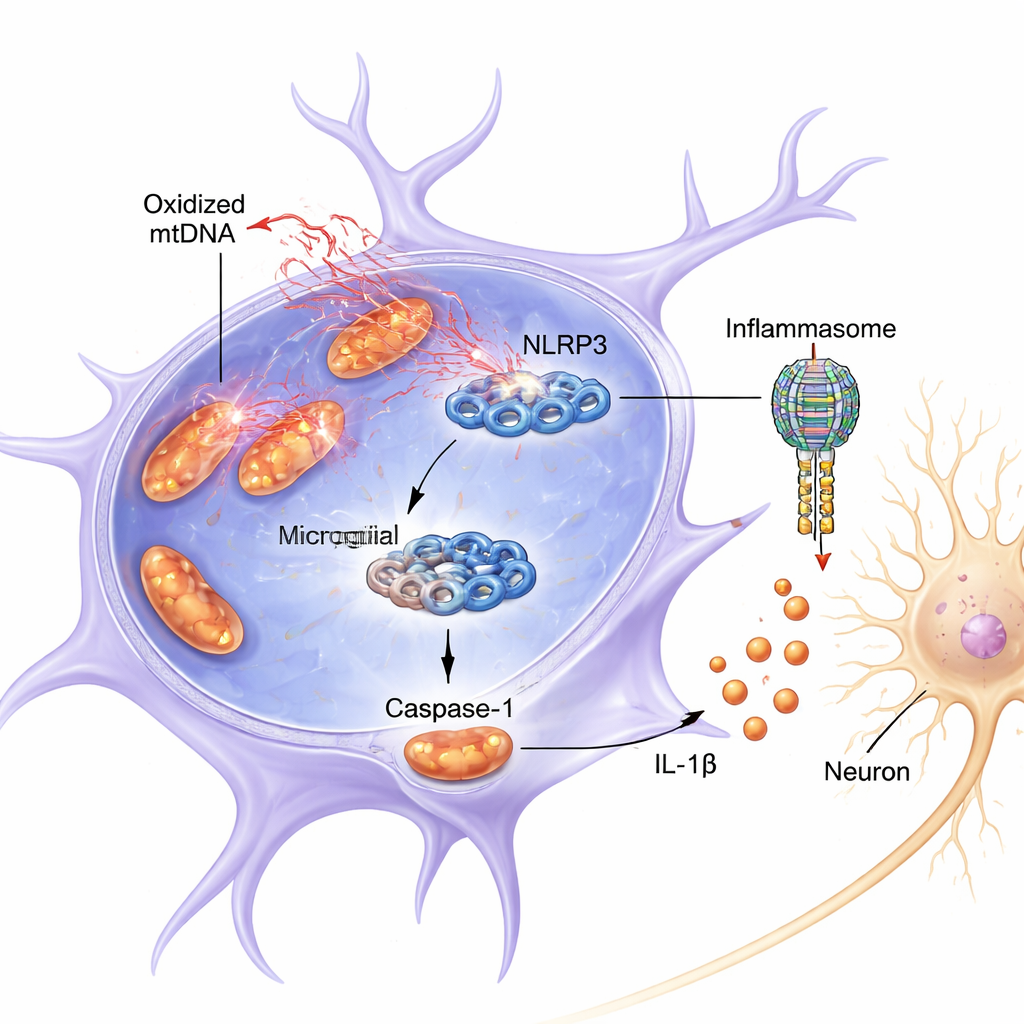
El estudio se centró en un complejo proteico en microglía llamado NLRP3, parte de un ensamblaje mayor conocido como inflamasoma. Cuando se activa, NLRP3 ayuda a activar la caspasa-1, una enzima que corta la molécula inflamatoria IL-1β para convertirla en su forma activa y dañina. Tanto en ratones como en células en cultivo, la combinación de una señal de cebado inflamatorio (LPS, un componente bacteriano) y la toxina de tipo pesticida rotenona hizo que las mitocondrias en microglía liberaran ADN mitocondrial oxidado al citosol. Esta liberación coincidió con una activación más intensa de NLRP3, mayor caspasa-1 escindida (activa) y niveles más altos de IL-1β. El medio tomado de estas microglías sobreactivadas fue directamente tóxico para neuronas de tipo dopaminérgico cultivadas en placa, reduciendo su supervivencia y el nivel de su marcador clave, la tirosina hidroxilasa.
Unión directa: cómo el ADN oxidado activa el interruptor NLRP3
Más allá de una simple correlación, los autores mostraron que el ox-mtDNA no solo está presente durante la inflamación: parece unirse físicamente a NLRP3 y activarlo. Cuando bloquearon la liberación de ADN mitocondrial con un fármaco, la activación de caspasa-1 y de IL-1β disminuyó. Por el contrario, la entrega directa de ADN mitocondrial oxidado a microglías potenció fuertemente la señalización de NLRP3, más que el mtDNA no oxidado. Mediante experimentos bioquímicos de pull-down detectaron mtDNA, rico en marcadores de daño oxidativo, unido a NLRP3. Modelado computacional y química de proteínas revelaron que el ox-mtDNA se une a un segmento cargado positivamente y flexible de NLRP3 (una “región intrínsecamente desordenada” que abarca los aminoácidos 180–187). Cuando se eliminó este tramo crítico de NLRP3, su capacidad para unirse al ox-mtDNA y activar caspasa-1 se redujo considerablemente.
Apagar el inflamasoma preserva neuronas
Los investigadores preguntaron entonces si interferir con NLRP3 podría proteger a las neuronas. En microglías en cultivo, reducir genéticamente NLRP3 disminuyó bruscamente la activación de caspasa-1 e IL-1β tras el tratamiento con LPS y rotenona, y el medio condicionado de estas células fue mucho menos tóxico para las neuronas de tipo dopaminérgico. En ratones, un inhibidor selectivo de NLRP3 (MCC950) redujo la activación microglial, preservó las neuronas dopaminérgicas y disminuyó las proteínas relacionadas con el inflamasoma en modelos inducidos ya sea por LPS más rotenona o por inyección de mtDNA. En conjunto, estos experimentos muestran que la cadena ox-mtDNA–NLRP3–IL-1β no solo se asocia con el daño; es necesaria para gran parte de la pérdida neuronal observada.
Qué significa esto para las futuras terapias del Parkinson
Para el público general, el mensaje clave es que el ADN mitocondrial dañado que se filtra desde las células inmunitarias del cerebro puede unirse directamente a un “interruptor de alarma” interno (NLRP3), provocando una ola de inflamación que daña las neuronas dopaminérgicas y conduce a una enfermedad parecida al Parkinson en modelos. Dado que esta interacción depende de un tramo corto y definido de la proteína NLRP3 y de la naturaleza oxidada del ADN mitocondrial, ofrece dianas farmacológicas muy precisas. Terapias que prevengan el daño o la fuga del ADN mitocondrial, bloqueen su unión a NLRP3 o inhiban NLRP3 podrían, en principio, enfriar esta cascada inflamatoria y ralentizar la progresión de la enfermedad de Parkinson.
Cita: Gan, Q., Fu, X., Zhou, T. et al. Mitochondrial DNA drives NLRP3-IL-1β axis activation in microglia by binding to NLRP3, leading to neurodegeneration in Parkinson’s disease models. Cell Death Dis 17, 213 (2026). https://doi.org/10.1038/s41419-026-08424-7
Palabras clave: Enfermedad de Parkinson, microglía, ADN mitocondrial, inflamasoma NLRP3, neuroinflamación