Clear Sky Science · es
Lactilación de SLC26A3 en el microambiente tumoral ácido promueve la progresión maligna del carcinoma colorrectal
Por qué importa la acidez tumoral
El cáncer colorrectal sigue siendo uno de los tipos de cáncer más letales a nivel mundial, en parte porque los tumores con frecuencia reaparecen, se diseminan o dejan de responder a los fármacos. Este estudio explora un culpable poco valorado detrás de ese comportamiento: el entorno ácido, rico en ácido láctico, dentro de los tumores. Al desvelar cómo este ambiente hostil desestabiliza una proteína de membrana protectora llamada SLC26A3, los autores revelan una nueva cadena de eventos que ayuda a las células tumorales a volverse más parecidas a células madre, invasivas y resistentes a los tratamientos, ofreciendo ideas nuevas para la terapia.
Un vecindario hostil alrededor de las células cancerosas
Los tumores de rápido crecimiento consumen grandes cantidades de azúcar y oxígeno, liberando ácido láctico e iones de hidrógeno que acidifican su entorno. Utilizando grandes conjuntos de datos de pacientes y muestras de tejido, los investigadores muestran que este estado ácido, seguido por una proteína marcadora llamada CA9, va de la mano con tumores colorrectales agresivos. En cánceres más avanzados, los niveles de CA9 son altos, mientras que los de SLC26A3 son consistentemente bajos. SLC26A3 normalmente se localiza en la superficie de las células del colon y ayuda a equilibrar sales y bicarbonato, lo que a su vez contribuye a controlar la acidez. En muestras tumorales, líneas celulares cancerosas y análisis de célula única, el equipo encuentra que cuando aumenta la acidez, los niveles de SLC26A3 disminuyen, especialmente en las células malignas con rasgos tipo célula madre. 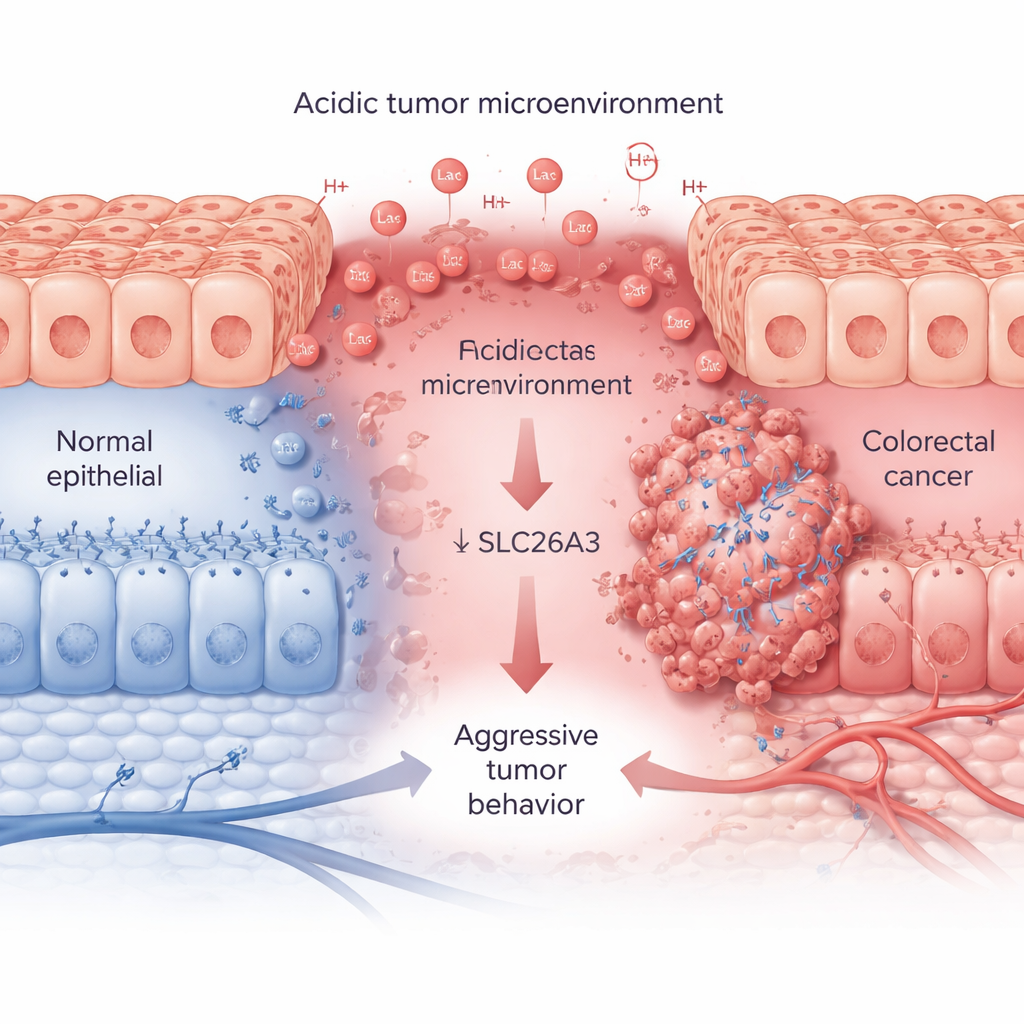
Cómo el ácido láctico marca un objetivo para la destrucción
Los autores se preguntan entonces por qué SLC26A3 disminuye en tumores ácidos. Se centran en la lactilación, una etiqueta química recientemente descubierta derivada del ácido láctico que puede añadirse a proteínas. Cuando las células de cáncer colorrectal se exponen al ácido láctico o se cultivan en condiciones ácidas, SLC26A3 se vuelve fuertemente lactilada. Un análisis proteico detallado identifica un sitio clave, un aminoácido llamado K536, donde se añade esta marca. La lactilación en K536 hace que SLC26A3 sea menos estable: la proteína tiene más probabilidades de ser etiquetada con ubiquitina, una señal celular de “desechar esto”, y ser enviada a la maquinaria de reciclaje celular. Bloquear la enzima p300, que ayuda a añadir marcas de lactilación, protege parcialmente a SLC26A3 de la degradación. Como resultado, la acidez y el lactato instauran un bucle de retroalimentación dañino: más lactato conduce a más lactilación, lo que reduce SLC26A3, desajusta aún más el equilibrio del pH y favorece un microambiente todavía más ácido.
Desactivar un freno sobre la capacidad de las células para adquirir rasgos madre y diseminarse
Con SLC26A3 agotado, las células cancerosas se comportan de forma más agresiva. En cultivo celular, las células tumorales colorrectales con rasgos tipo célula madre expresan de forma natural menos SLC26A3 que sus contrapartes no madre. Cuando los investigadores reducen intencionadamente los niveles de SLC26A3, las células tumorales forman más esferas (un sello de la pluripotencia), se autorrenuevan con mayor eficiencia, invaden a través de membranas artificiales y migran más rápido en ensayos de herida por raspado. También se vuelven menos sensibles a quimioterápicos comunes como oxaliplatino y 5‑fluorouracilo. Por el contrario, aumentar SLC26A3 reduce los marcadores de pluripotencia y ralentiza la invasión y migración, pero este beneficio se ve atenuado cuando se añade lactato extra, lo que subraya cómo la acidez puede anular el efecto protector.
Un vínculo oculto con el control genético
Más allá de ayudar a regular la acidez, SLC26A3 actúa como un andamiaje que une dos proteínas fijadoras de ARN, HuR y CUGBP1. Estas proteínas controlan la vida útil de muchos ARNm que codifican proteínas relevantes para el cáncer. Cuando SLC26A3 es abundante, secuestra parte de HuR y CUGBP1, limitando la capacidad de estas proteínas para estabilizar o desestabilizar ciertos mensajes relacionados con el cáncer. Cuando SLC26A3 se pierde por lactilación y degradación, HuR y CUGBP1 quedan más libres para unirse a ARNm oncogénicos que promueven la pluripotencia, la transición epitelio‑mesénquima (EMT), la invasión y la supervivencia. Los experimentos muestran que HuR ayuda a estabilizar ARNm de marcadores de pluripotencia y proteínas de unión celular, mientras que CUGBP1 puede oponerse a HuR en algunos objetivos, reduciendo la integridad de las uniones y favoreciendo la EMT: ambos procesos facilitan la diseminación tumoral.
Reequilibrar el entorno para combatir el cáncer
Para comprobar si estos hallazgos pueden traducirse en estrategias terapéuticas, los investigadores usan modelos murinos de cáncer colorrectal. Neutralizar la acidez tumoral con bicarbonato de sodio, bloquear el transporte de lactato con un inhibidor de MCT1 o sobreexpresar SLC26A3 ralentizan el crecimiento tumoral. Combinar la restauración de SLC26A3 con quimioterapia reduce aún más los tumores. En datos de pacientes, niveles más altos de SLC26A3 se correlacionan con mejor supervivencia, menos recurrencia, menos metástasis y mejores respuestas a la quimioterapia, lo que sugiere que esta proteína podría servir tanto como biomarcador como diana terapéutica. 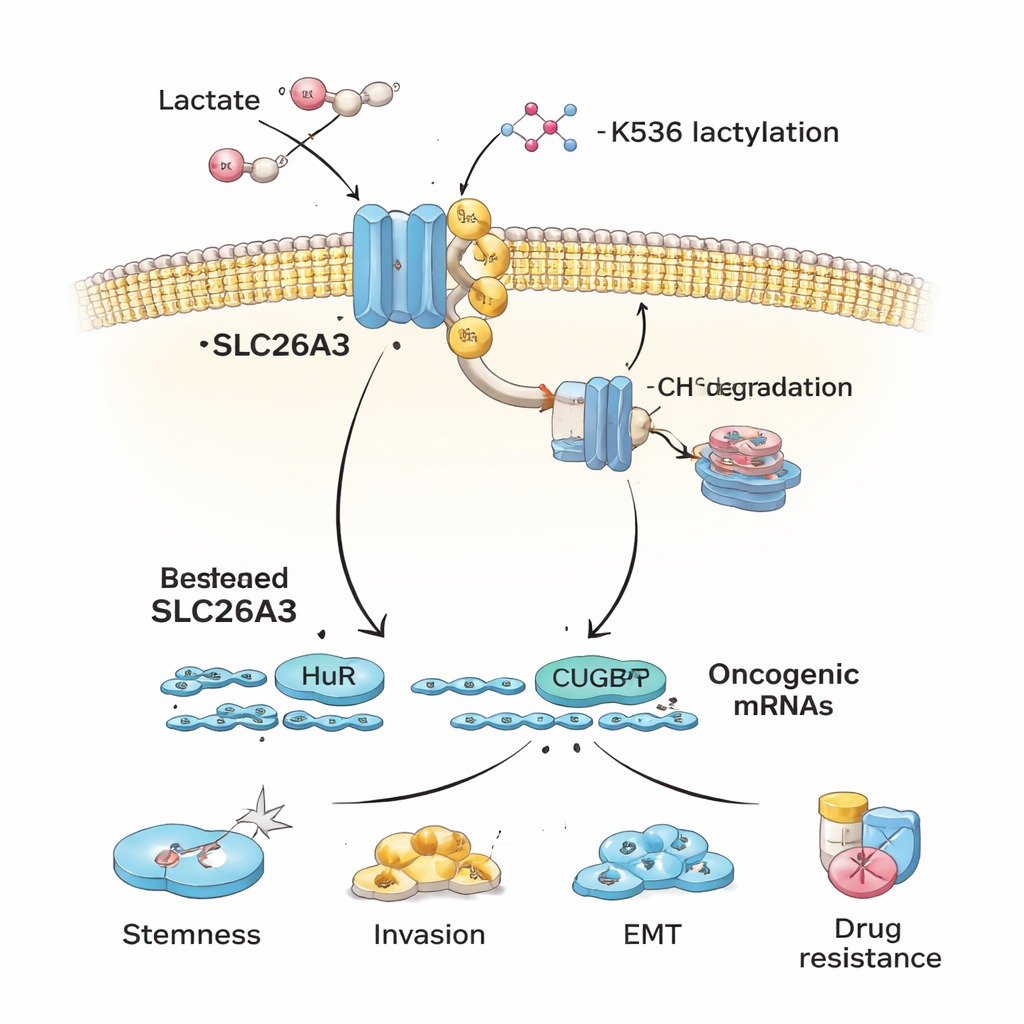
Qué implica esto para los pacientes
En términos sencillos, este estudio muestra que los tumores colorrectales prosperan en un baño agrio y rico en ácido láctico que “etiqueta” y destruye químicamente a un guardián protector, SLC26A3. Una vez que este guardián desaparece, las células cancerosas adoptan con mayor facilidad rasgos tipo célula madre, se diseminan y resisten los tratamientos, ayudadas por potentes reguladores de ARN dentro de la célula. Al amortiguar la acidez tumoral, bloquear el manejo del lactato o restaurar SLC26A3, podría ser posible debilitar ese bucle maligno de retroalimentación y mejorar la efectividad de las terapias estándar. Aunque tales enfoques aún requieren pruebas clínicas rigurosas, abren un ángulo prometedor sobre cómo controlar los entornos químicos del tumor podría ayudar a afrontar el cáncer colorrectal.
Cita: Chen, C., Cai, D., Liu, X. et al. Lactylation of SLC26A3 in the acidic tumor microenvironment promotes malignant progression of colorectal carcinoma. Cell Death Dis 17, 164 (2026). https://doi.org/10.1038/s41419-026-08422-9
Palabras clave: cáncer colorrectal, microambiente tumoral, lactilación, células madre cancerosas, resistencia a la quimioterapia