Clear Sky Science · es
Apuntar a GNG4 inhibe la progresión tumoral y restaura la sensibilidad a enzalutamida en el cáncer de próstata al suprimir la autofagia
Por qué esta investigación importa
Para muchos hombres con cáncer de próstata avanzado, medicamentos potentes que bloquean hormonas como la enzalutamida funcionan bien al principio pero luego van perdiendo eficacia gradualmente. Este estudio descubre un truco de supervivencia oculto que usan las células tumorales y señala a una proteína específica, llamada GNG4, que ayuda a los cánceres a seguir creciendo y a resistir el tratamiento. Entender este mecanismo podría conducir a terapias combinadas que hagan que los fármacos actuales funcionen mejor y durante más tiempo.
Un interruptor proteico a la vista de todos
Las células de cáncer de próstata están fuertemente impulsadas por hormonas masculinas, por lo que la atención estándar para la enfermedad avanzada corta estas señales. Sin embargo, la mayoría de los tumores acaban volviéndose “resistentes a la castración” y comienzan a crecer de nuevo. Los autores buscaron genes que estuvieran mucho más activos en tejido tumoral que en la próstata normal adyacente de los mismos pacientes. Entre varios candidatos, GNG4 destacó: cuando redujeron sus niveles en células de cáncer de próstata, el crecimiento celular tumoral cayó bruscamente. Los análisis de cientos de muestras de pacientes confirmaron que GNG4 es más alto en cánceres de próstata primarios que en tejido normal y está especialmente elevado en tumores más agresivos y de mayor grado.
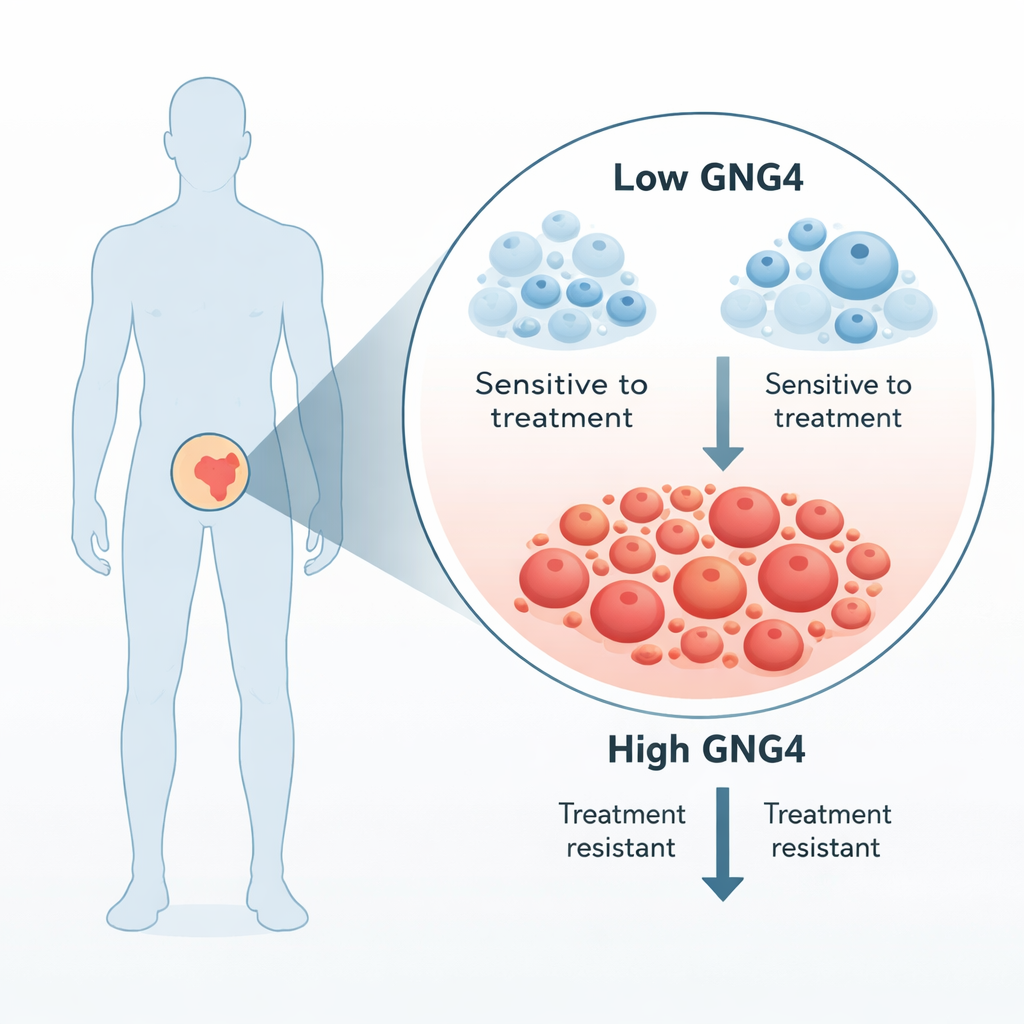
Cómo GNG4 ayuda a los tumores a prosperar
GNG4 forma parte de una familia de señalización más amplia conocida como proteínas G, que se sitúan en la membrana celular y retransmiten señales del exterior al interior de la célula. El equipo demostró que reducir GNG4 en líneas celulares de cáncer de próstata ralentizaba la división celular, empujaba a las células a detenerse en un punto de control del ciclo celular e incrementaba la muerte celular programada. Estos cambios también redujeron la capacidad de las células cancerosas para migrar y cerrar heridas en pruebas de laboratorio, y los tumores formados por células deficientes en GNG4 crecieron más despacio en ratones. En conjunto, estos hallazgos sugieren que GNG4 actúa como un pedal de aceleración para el crecimiento y la diseminación del cáncer de próstata.
Autofagia: la despensa de emergencia de la célula cancerosa
Los investigadores se centraron a continuación en un proceso llamado autofagia, por el cual las células descomponen y reciclan sus propios componentes para sobrevivir al estrés, como la inanición o el tratamiento farmacológico. En muchos cánceres avanzados, la autofagia funciona como una despensa de emergencia que ayuda a las células tumorales a soportar condiciones adversas. En este estudio, las células de cáncer de próstata con alta actividad de GNG4 mostraron más signos de autofagia activa, mientras que las células con GNG4 reducido presentaban menos estructuras de reciclaje y niveles más bajos de marcadores clave de autofagia. Cuando se sobreexpresó GNG4, las células toleraron mejor la enzalutamida y sufrieron menos muerte celular. Bloquear la autofagia con un inhibidor químico eliminó gran parte de esta protección, lo que indica que GNG4 ayuda a los tumores a soportar el tratamiento en gran medida aumentando este sistema de reciclaje.
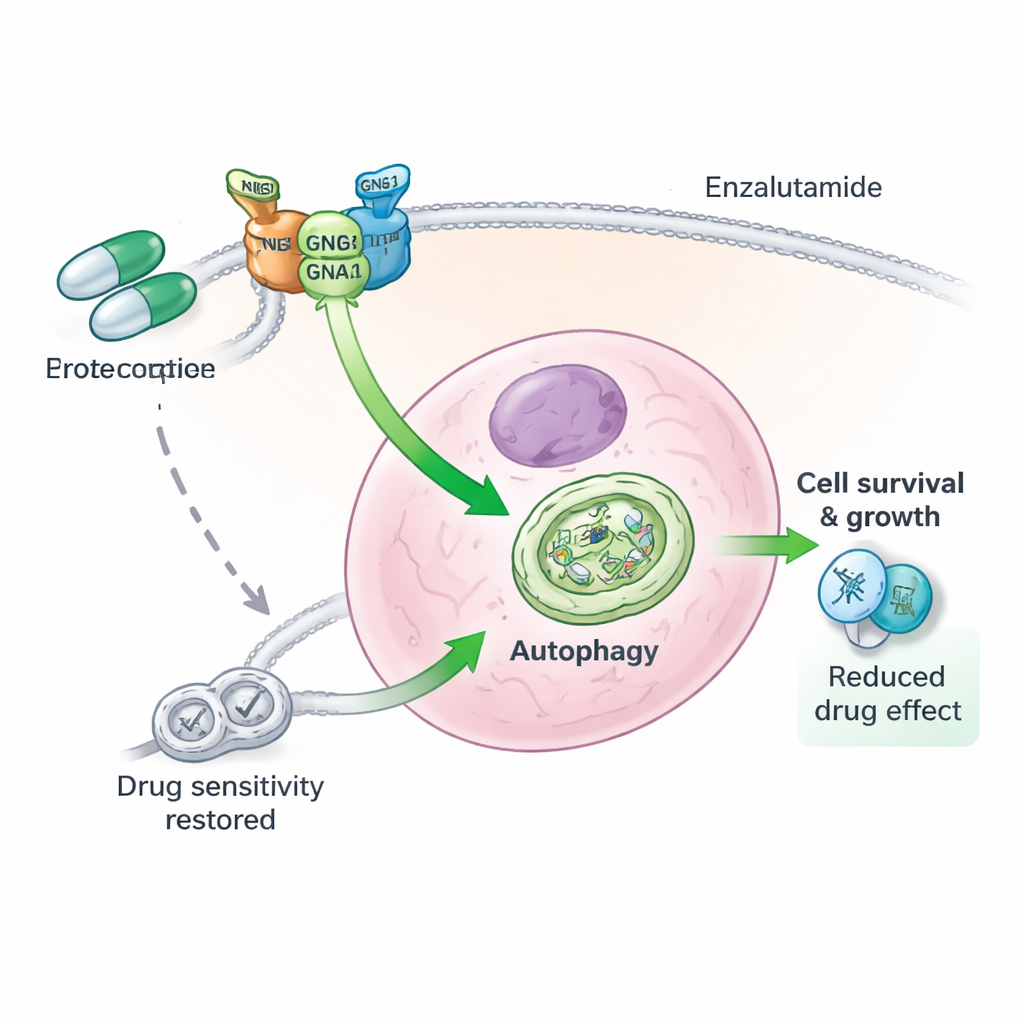
Un equipo proteico de tres piezas detrás de la resistencia a fármacos
Al profundizar, los autores descubrieron que GNG4 no actúa solo. Se asocia físicamente con otro componente de proteínas G, GNB1, para estabilizar una tercera proteína, GNAI3. Juntas, estas tres subunidades forman un complejo funcional que potencia la autofagia dentro de las células de cáncer de próstata. Cuando se redujo GNG4, la proteína GNAI3 fue etiquetada más rápidamente para su destrucción y degradada por la maquinaria de eliminación celular, lo que apagó la señal de autofagia. Eliminar la propia GNAI3 anuló las ventajas de crecimiento y supervivencia conferidas por el exceso de GNG4, tanto en células en cultivo como en tumores de ratón. En otras palabras, GNG4 impulsa la malignidad y la resistencia al estrés en gran medida a través de este eje GNG4–GNB1–GNAI3.
Hacer que los fármacos actuales funcionen mejor
Finalmente, el equipo preguntó qué ocurre cuando se combina el bloqueo de GNG4 con enzalutamida, un fármaco líder para el cáncer de próstata avanzado. En el laboratorio, la reducción de GNG4 hizo que las células cancerosas fueran notablemente más sensibles a la enzalutamida y redujo su capacidad para formar colonias tras el tratamiento. En ratones, los tumores con GNG4 disminuida se redujeron más cuando se administró enzalutamida que los tumores con niveles normales de GNG4, sin toxicidad adicional evidente. Bloquear la autofagia directamente produjo mejoras similares. Estos resultados sugieren que interferir con la autofagia impulsada por GNG4 puede despojar a las células tumorales de un mecanismo vital de adaptación, permitiendo que las terapias bloqueadoras de hormonas existentes inflijan un golpe más fuerte y duradero.
Qué significa esto para los pacientes
Para un público no especializado, el mensaje clave es que algunos cánceres de próstata sobreviven al tratamiento activando un sistema interno de reciclaje que actúa como un generador de respaldo. Este estudio identifica a GNG4 como un interruptor principal que enciende ese sistema, trabajando junto a proteínas asociadas para proteger a las células cancerosas de la enzalutamida. Al apagar este interruptor, ya sea apuntando directamente a GNG4 o moderando la autofagia de forma segura, las terapias futuras podrían ralentizar el crecimiento tumoral y restaurar la sensibilidad a los fármacos en hombres cuyos cánceres se han vuelto difíciles de tratar.
Cita: Chen, L., Zhang, J., Hu, Y. et al. Targeting GNG4 inhibits tumor progression and restores enzalutamide sensitivity in prostate cancer by suppressing autophagy. Cell Death Dis 17, 160 (2026). https://doi.org/10.1038/s41419-026-08421-w
Palabras clave: cáncer de próstata, resistencia a fármacos, autofagia, proteínas G, enzalutamida