Clear Sky Science · es
DNA-PKcs orquesta la senescencia inducida por la depleción de CTLA-4 en células cancerosas
Convertir el interruptor de crecimiento del cáncer en una señal de paro
Los fármacos oncológicos basados en el sistema inmune suelen centrarse en una molécula llamada CTLA-4, presente en células inmunitarias, para ayudar al cuerpo a atacar los tumores. Este estudio revela un giro sorprendente: CTLA-4 también se encuentra dentro de las propias células tumorales y puede actuar como un ayudante oculto del crecimiento. Cuando los científicos eliminaron deliberadamente este CTLA-4 interno en células de melanoma, las células cancerosas dejaron de multiplicarse y entraron en un estado de “jubilación” a largo plazo conocido como senescencia celular. Comprender este papel inesperado abre nuevas vías para frenar o incluso reducir los tumores al dirigirse a CTLA-4 dentro de las células cancerosas, no solo en las células inmunitarias.
Cuando las células eligen la jubilación en lugar del crecimiento descontrolado
Las células normalmente se dividen, reparan y, cuando están dañadas irreparablemente, o bien mueren o entran en senescencia, una detención permanente de su crecimiento. Las células senescentes típicamente aumentan de tamaño, cambian de forma y producen marcadores específicos que los científicos pueden detectar en el laboratorio. Los investigadores hallaron que al reducir CTLA-4 en células de melanoma de ratón y humanas, las células se hicieron más grandes, su proliferación cayó drásticamente y aumentaron señales clásicas de senescencia, incluyendo enzimas detectables mediante tinciones especiales y proteínas como p16 y p21 que bloquean el ciclo celular. Estos cambios se observaron tanto cuando CTLA-4 fue silenciado temporalmente como cuando fue eliminado de forma permanente mediante herramientas de edición genética.
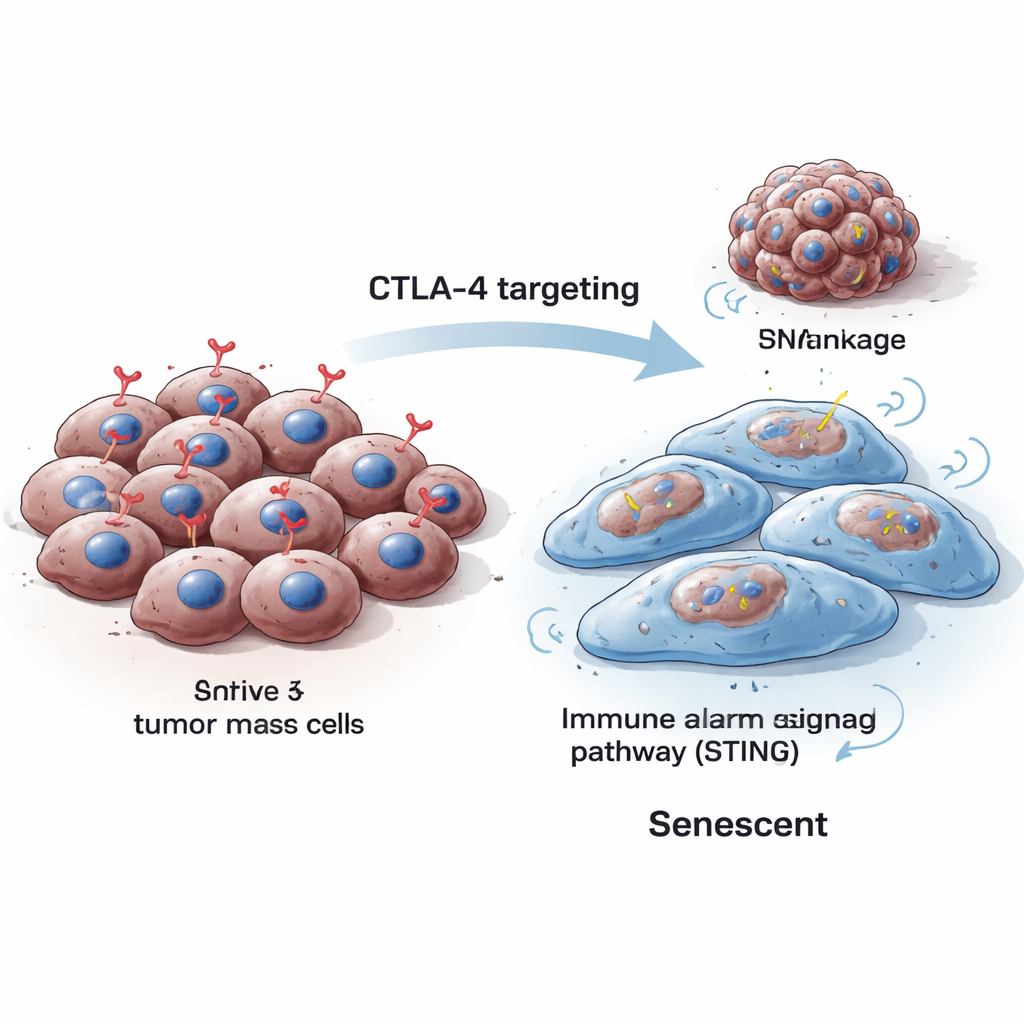
Grietas en el plano genético conducen a un punto muerto
Para entender por qué la pérdida de CTLA-4 empuja a las células cancerosas hacia la senescencia, el equipo examinó cómo estas células gestionan su ADN durante la división. Descubrieron que la depleción de CTLA-4 redujo los niveles de Aurora B, una proteína que ayuda a que los cromosomas se separen limpiamente durante la división celular. Cuando Aurora B disminuyó, las células desarrollaron inestabilidad genómica: aparecieron minúsculos cuerpos extra con ADN llamados micronúcleos y aumentaron los marcadores de daño en el ADN. Este tipo de estrés sobre el ADN es conocido por empujar a las células hacia la senescencia en lugar del crecimiento descontrolado. De manera importante, restaurar Aurora B ayudó a reducir estos micronúcleos, vinculando directamente la pérdida de CTLA-4 con un manejo defectuoso de los cromosomas y daño en el ADN.
El daño en el ADN pone en marcha una red de alarma interna
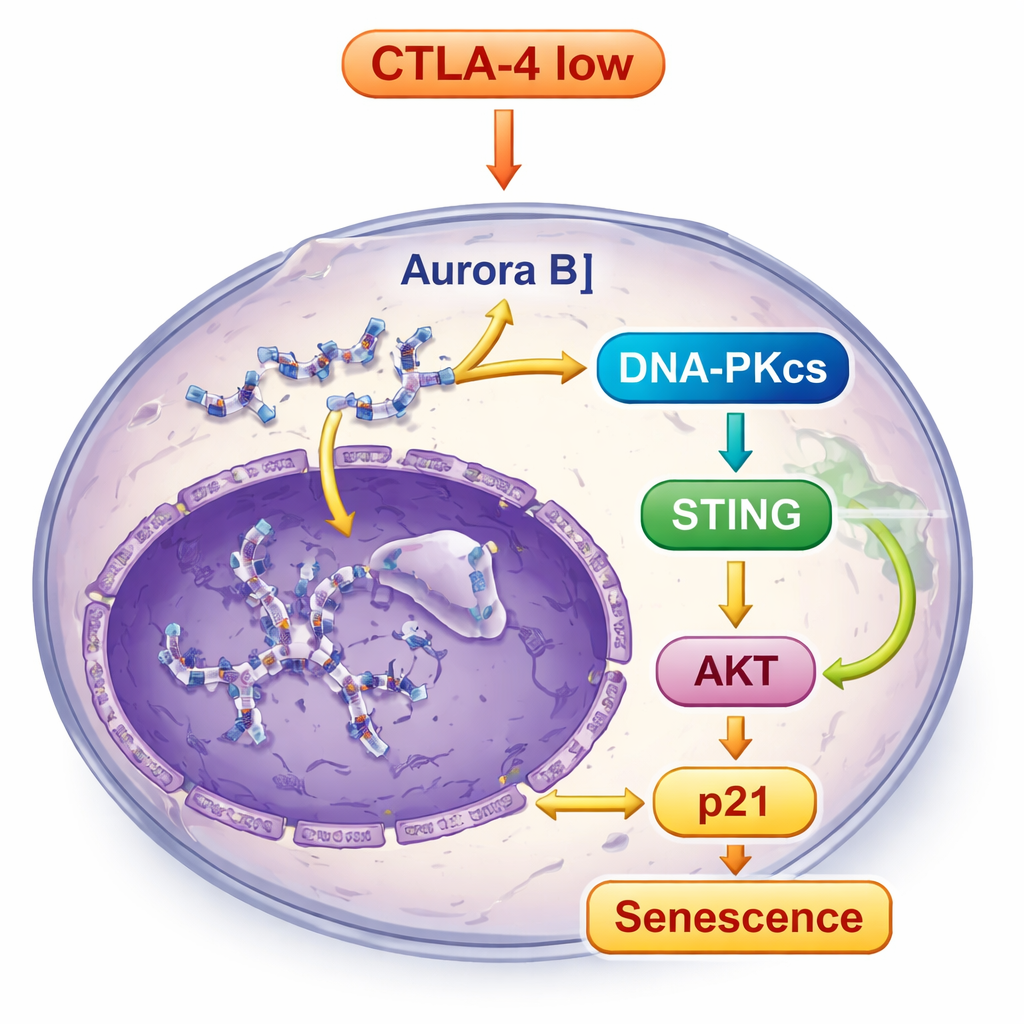
El ADN fragmentado y desplazado en las células privadas de CTLA-4 no pasó desapercibido. Activó DNA-PKcs, un sensor del daño en el ADN, que a su vez desencadenó la vía STING, un sistema de alarma integrado que responde al ADN errante dentro de las células. Una vez activada STING, señaló a moléculas aguas abajo, incluidas TBK1 e IRF3, y también potenció otra ruta clave de control del crecimiento, la vía AKT. En lugar de promover el crecimiento, esta señalización conjunta incrementó finalmente p21, un potente freno del ciclo celular, reforzando el estado senescente. Cuando los científicos bloquearon DNA-PKcs, la activación de STING y las características de senescencia se redujeron considerablemente, demostrando que DNA-PKcs se sitúa en el centro de esta cadena de alarma.
De cultivos celulares a tumores en animales vivos
Las placas de laboratorio solo cuentan parte de la historia, por lo que los investigadores evaluaron si la pérdida de CTLA-4 afectaría tumores reales en ratones. Implantaron células de melanoma con o sin CTLA-4 en lados opuestos de los mismos animales. Los tumores carentes de CTLA-4 crecieron más despacio, pesaron menos y tuvieron menor volumen que sus homólogos que contenían CTLA-4. Estos tumores deficientes en CTLA-4 también mostraron tinción de senescencia más intensa y niveles más altos de daño en el ADN y activación de la vía STING. El análisis de datos de pacientes con cáncer procedentes de grandes bases públicas respaldó además la relación: en varios tipos de cáncer, la expresión de CTLA-4 tendía a estar inversamente relacionada con DNA-PKcs y otros componentes de reparación del ADN, haciendo eco de los hallazgos de laboratorio en la enfermedad humana.
Qué significa esto para futuros tratamientos contra el cáncer
En conjunto, el estudio muestra que CTLA-4 dentro de las células cancerosas les ayuda a mantener la estabilidad genética y a seguir dividiéndose. Cuando se elimina CTLA-4, los cromosomas se vuelven inestables, se acumulan roturas en el ADN y una vía de alarma interna —centrada en DNA-PKcs y STING— empuja a las células hacia un arresto permanente del crecimiento. Para un público general, esto significa que apagar CTLA-4 en las células tumorales empuja a los cánceres lejos del comportamiento peligroso y de rápido crecimiento y hacia un estado más seguro de “jubilación”. Estos hallazgos sugieren que futuras terapias contra el cáncer podrían diseñarse no solo para liberar el sistema inmune bloqueando CTLA-4 en las células inmunitarias, sino también para desarmar directamente los tumores apuntando a CTLA-4 dentro de las células cancerosas y aprovechando la senescencia como un freno intrínseco al crecimiento tumoral.
Cita: Lee, JJ., Rhee, W.J., Kim, S.Y. et al. DNA-PKcs orchestrates CTLA-4 depletion-induced senescence in cancer cells. Cell Death Dis 17, 204 (2026). https://doi.org/10.1038/s41419-026-08419-4
Palabras clave: senescencia celular, melanoma, CTLA-4, daño en el ADN, vía STING