Clear Sky Science · es
Transporte citoplasma‑núcleo de TET2: un freno intrínseco en la progresión del cáncer colorrectal
Cómo las células cancerosas llevan su propio freno
El cáncer colorrectal es uno de los cánceres más frecuentes en el mundo y a menudo se vuelve mortal cuando las células tumorales aprenden a invadir el tejido circundante y a diseminarse a otros órganos. Este estudio revela que muchas de esas células cancerosas llevan en realidad un “sistema de freno” interno: una proteína llamada TET2, que puede ralentizar su avance cuando se desplaza al núcleo celular. Comprender cómo se activa y desactiva este freno incorporado podría abrir nuevas vías para contener el crecimiento tumoral en lugar de limitarse a intentar eliminar las células cancerosas por completo.
Observando el movimiento de una proteína clave dentro de las células tumorales
Los investigadores se centraron en TET2, una proteína que ayuda a controlar qué genes están encendidos o apagados al eliminar ciertas marcas químicas del ADN. En muestras de tejido de cientos de pacientes con cáncer colorrectal, rastrearon dónde se localiza TET2 dentro de las células tumorales. Encontraron cuatro patrones principales: mayoritariamente en el núcleo, mayoritariamente en el citoplasma o fuertemente sesgado hacia uno u otro compartimento. Los pacientes cuyos tumores mostraban más TET2 en el núcleo tendían a vivir más tiempo, mientras que aquellos cuyos tumores mantenían TET2 en el citoplasma tuvieron peores resultados. A medida que los cánceres avanzaban a estadios clínicos más avanzados, el TET2 nuclear se volvía más raro, lo que sugiere que perder esta protección nuclear forma parte del proceso por el que los tumores se vuelven más agresivos.
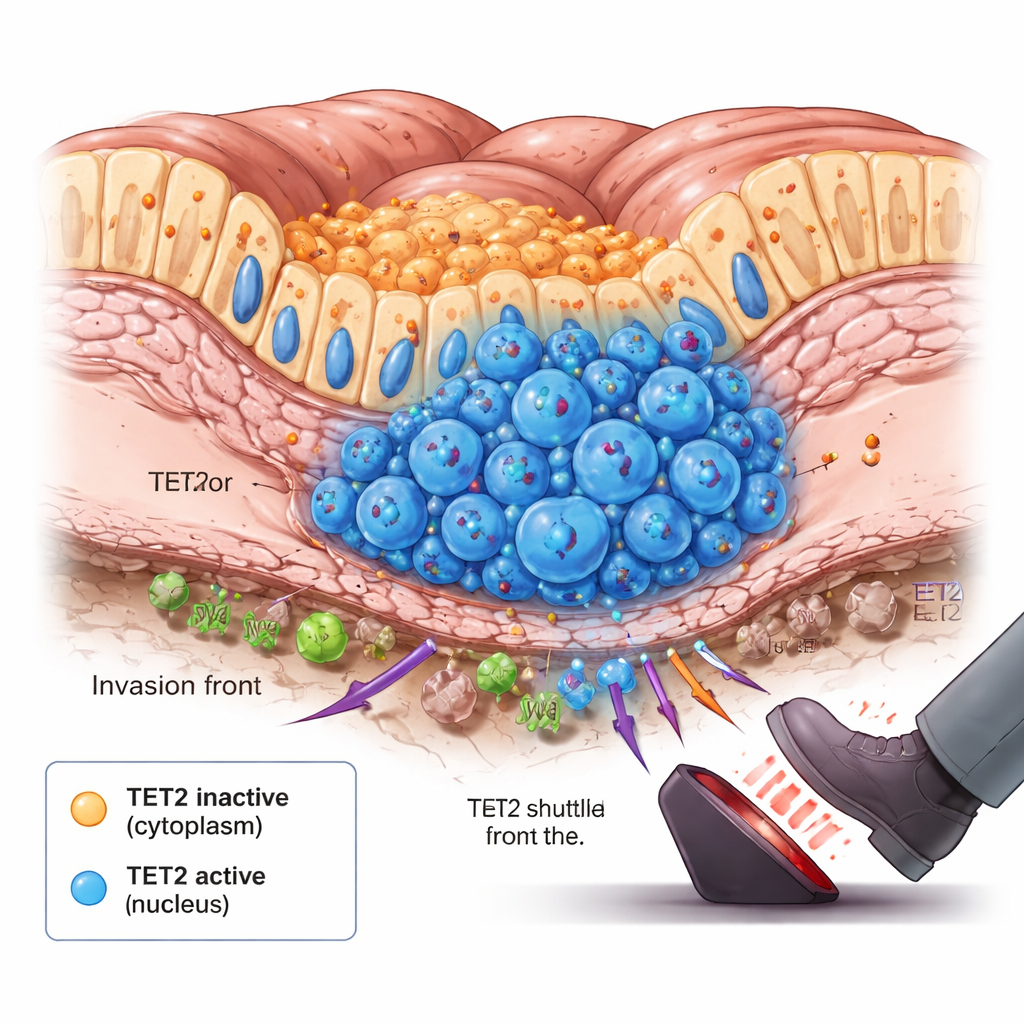
La línea frontal del tumor y el momento del cambio
Al indagar más, el equipo observó algo sorprendente: en tumores que estaban empezando a diseminarse, hubo un ligero aumento de células en las que TET2 se había trasladado al núcleo. Estas células se agruparon en la base del revestimiento intestinal, en el frente de invasión donde las células cancerosas empiezan a penetrar tejido más profundo. Experimentos en animales y modelos de cultivo celular a largo plazo que imitan el crecimiento tumoral mostraron un patrón similar a lo largo del tiempo. Al principio, TET2 permanecía en el citoplasma y estaba mayormente inactivo. A medida que los tumores crecían y las regiones internas se quedaban sin oxígeno y nutrientes, señales intracelulares desencadenaron el transporte de TET2 al núcleo en subpoblaciones específicas. Una vez allí, TET2 comenzó a eliminar marcas de metilación del ADN y a frenar el crecimiento tumoral, actuando como un freno de emergencia cuando el cáncer cruzaba un umbral peligroso.
Cuando las señales de "adelante" también activan un freno
Los tumores colorrectales a menudo dependen de dos programas potentes de "adelante": un proceso de cambio de forma llamado transición epitelio‑mesénquima (EMT), que facilita que las células se vuelvan más móviles e invasivas, y la vía de señalización WNT, que potencia el crecimiento y la supervivencia. Estas vías suelen considerarse puramente perjudiciales en el cáncer. Sin embargo, este estudio muestra que cuando EMT y WNT se activan con fuerza, también contribuyen a llevar TET2 al núcleo. Usando fármacos y herramientas genéticas en cultivos celulares, los científicos demostraron que activar EMT o WNT aumentaba el número de células que trasladaban TET2 a sus núcleos, mientras que bloquear estas vías producía el efecto contrario. Una vez en el núcleo, el TET2 activo atenuaba los genes relacionados con EMT y WNT, reduciendo la migración celular y ralentizando la proliferación. En otras palabras, las mismas señales que favorecen el crecimiento tumoral también despiertan una fuerza contraria interna.
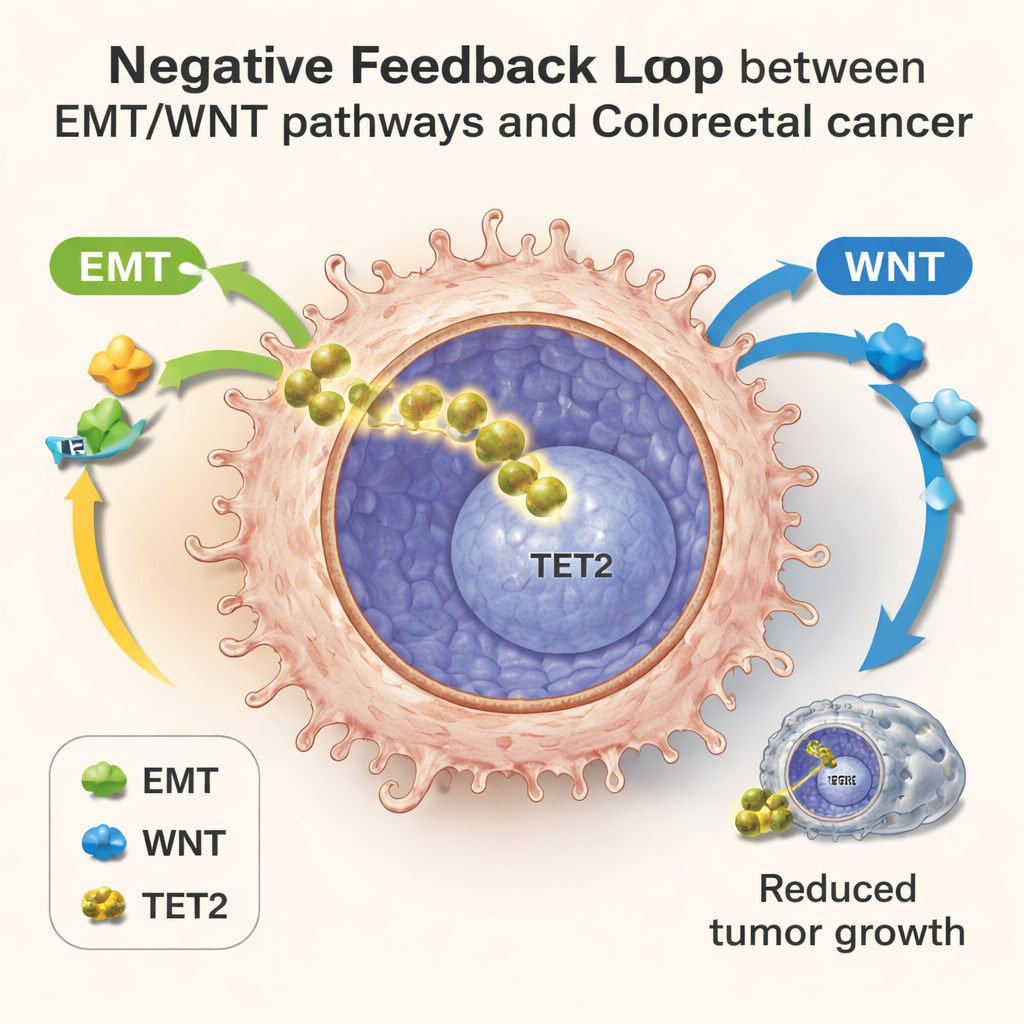
Las células individuales revelan un circuito de retroalimentación oculto
Para mapear este tira y afloja en detalle, el equipo empleó secuenciación de ARN de célula única, que lee qué genes están activos en miles de células individuales a la vez. En colonias cultivadas en laboratorio, en tumores de ratón y en muestras de pacientes con cáncer colorrectal, vieron células distribuidas a lo largo de una línea temporal de progresión. Las células tempranas mostraban uso energético normal y actividad débil de EMT/WNT; las células posteriores mostraban un reencuadre metabólico, señales fuertes de EMT/WNT y luego aumento de los genes diana de TET2. En estos pasos avanzados, las células con mayor actividad de TET2 tenían niveles más bajos de genes relacionados con la invasión y se asociaban con mejores resultados clínicos, incluso entre tumores que ya habían empezado a diseminarse. Este patrón respalda la idea de un bucle de retroalimentación negativa: el estrés metabólico y la activación de EMT/WNT empujan a TET2 al núcleo, y el TET2 nuclear a su vez restringe esos mismos programas agresivos.
Qué significa esto para futuros tratamientos contra el cáncer
Para los no especialistas, el mensaje clave es que la progresión del cáncer colorrectal no es un simple interruptor de "bueno/malo". En su lugar, existe un mecanismo de seguridad interno y retardado: a medida que las células tumorales se vuelven más invasivas, también activan TET2 en sus núcleos, lo que las frena parcialmente. Con el tiempo, muchos tumores escapan perdiendo TET2 nuclear o superando sus efectos. Si se hallan maneras de mantener TET2 en el núcleo o potenciar su actividad —posiblemente en combinación con fármacos que modulen EMT o WNT— los médicos podrían reforzar este freno natural y ralentizar la diseminación del cáncer. En lugar de limitarse a atacar las células cancerosas desde el exterior, las terapias futuras podrían funcionar restaurando y amplificando este sistema de control interno.
Cita: Li, C., Meng, F., He, J. et al. Cytoplasm-nucleus shuttling of TET2: an intrinsic brake in colorectal cancer progression. Cell Death Dis 17, 163 (2026). https://doi.org/10.1038/s41419-026-08418-5
Palabras clave: cáncer colorrectal, TET2, epigenética, EMT señalización WNT, progresión del cáncer