Clear Sky Science · es
Apuntar a ENO1 reprograma la polarización de macrófagos para desencadenar inmunidad antitumoral y mejora el efecto terapéutico de la radioterapia
Convertir los escudos tumorales en objetivos
El cáncer sobrevive a menudo no solo por crecer rápido, sino por desactivar silenciosamente las defensas del organismo. Este estudio explora una molécula oculta en las células cancerosas, llamada ENO1, que ayuda a los tumores a evadir el sistema inmune y a resistir la radioterapia. Al desarrollar un nuevo anticuerpo que apunta a ENO1, los investigadores muestran que es posible drenar el tumor de sus químicos protectores, activar las células inmunitarias y mejorar la eficacia de la radiación en modelos de cáncer colorrectal y de mama triple negativo. 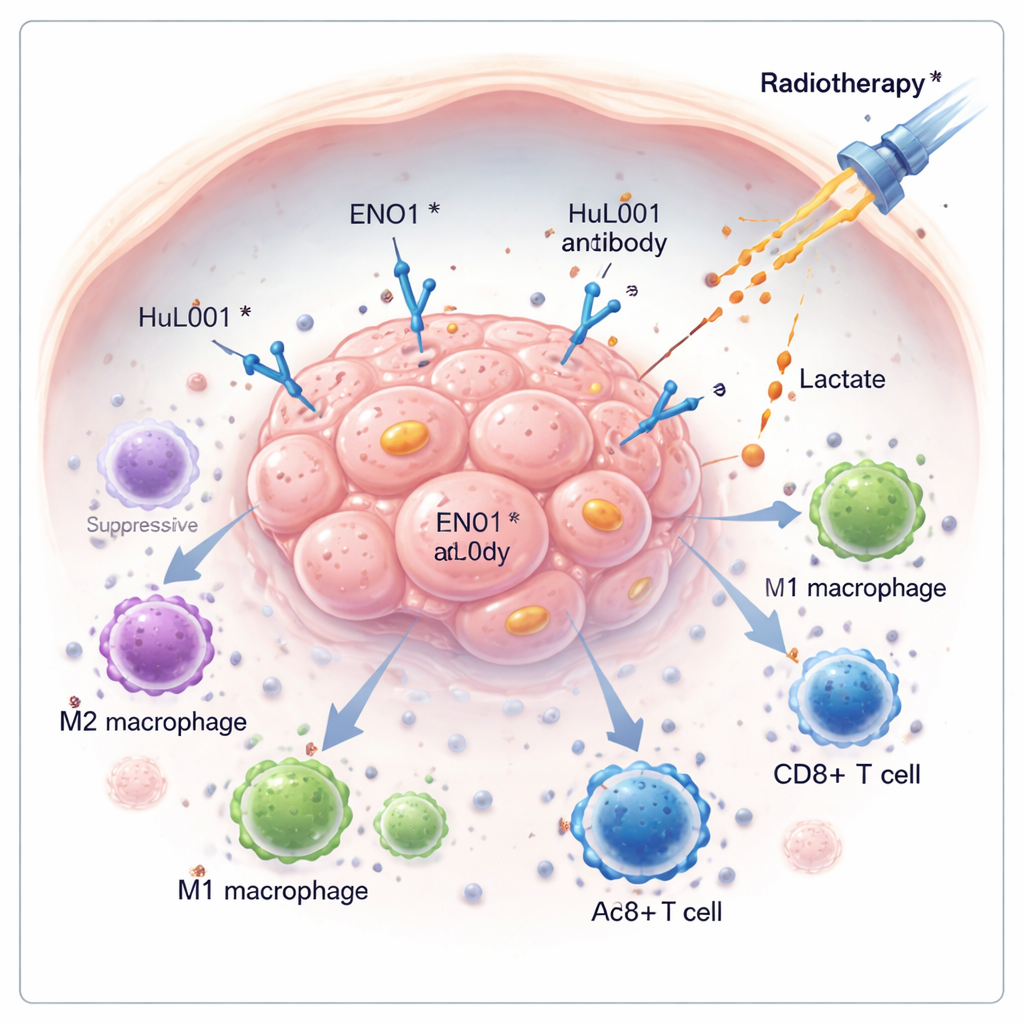
Un truco metabólico que silencia la inmunidad
Muchos tumores reconfiguran su uso de la energía, descomponiendo el azúcar de una manera que produce grandes cantidades de ácido láctico aun cuando hay oxígeno disponible. Este ácido láctico se bombea fuera de las células cancerosas y se acumula alrededor del tumor, convirtiendo el entorno en un nicho ácido y hostil que debilita el ataque inmunitario. En este trabajo, los autores se centran en ENO1, una enzima implicada en la degradación de azúcares que también puede aparecer en la superficie de las células tumorales. Cuando está en la superficie celular, ENO1 se asocia con otra proteína, un transportador llamado MCT4, para ayudar a exportar lactato, alimentando un ambiente que favorece el crecimiento tumoral y suprime a las células inmunitarias.
Cómo la radiación puede volverse contraproducente
La radioterapia está diseñada para dañar el ADN tumoral y desencadenar respuestas inmunitarias, pero también tiene efectos dentro del microambiente tumoral. El equipo descubrió que señales impulsadas por una molécula llamada TGFβ1, que se ven aumentadas por la radiación, activan una enzima (PRMT5) que modifica químicamente a ENO1 y la moviliza a la superficie de las células cancerosas. Una vez allí, ENO1 interactúa físicamente con MCT4 para estabilizarlo y favorecer la exportación de lactato. Niveles más altos de ENO1 en la superficie se encontraron en pacientes con cáncer colorrectal avanzado y cáncer de mama triple negativo y se asociaron con más metástasis y peor supervivencia, lo que sugiere que la radiación puede, sin querer, reforzar un escudo inmunosupresor impulsado por el lactato alrededor de los tumores.
Reprogramando células inmunes amigas y enemigas
En el halo ácido alrededor de los tumores, las células inmunitarias llamadas macrófagos se empujan hacia un estado «sanador» (a menudo llamado M2) que en realidad ayuda a los tumores al apagar la inflamación y favorecer la reparación, en lugar de matar las células cancerosas. Los investigadores crearon un anticuerpo humanizado, HuL001, que reconoce ENO1 tanto en células tumorales de ratón como humanas. En cultivo celular y en modelos murinos, HuL001 interrumpió el soporte de ENO1 a MCT4, redujo la liberación de lactato y desplazó a los macrófagos fuera del estado M2 promotor del tumor hacia un estado M1, más agresivo contra el cáncer y mejor en fagocitar células tumorales. Es importante: HuL001 no mató simplemente a los macrófagos; más bien los reeducó mientras aumentaba directamente la muerte de las células cancerosas.
Haciendo que la radiación rinda más
Cuando HuL001 se combinó con radioterapia en modelos murinos de cáncer colorrectal y de mama triple negativo, los tumores se redujeron más, volvieron a crecer más despacio y en muchos animales desaparecieron por completo. 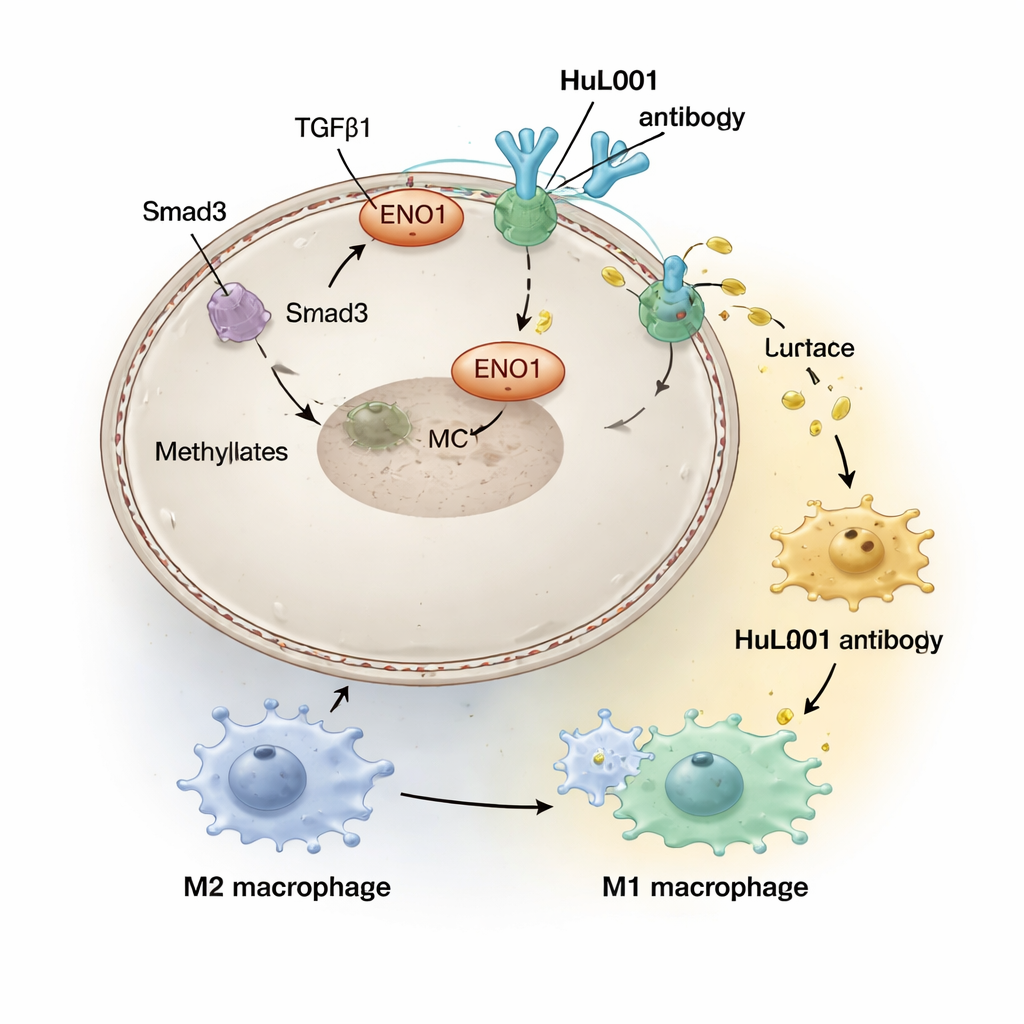
De vías complejas a una promesa práctica
Para no especialistas, el mensaje de este estudio es que la química de un tumor y su vecindario de células inmunitarias están profundamente entrelazados. ENO1 se sitúa en una intersección: ayuda a los tumores a metabolizar azúcar, exportar ácido láctico y reclutar el tipo equivocado de ayuda inmunitaria. Al bloquear ENO1 en la superficie con un anticuerpo dirigido, los investigadores pudieron reducir la acumulación dañina de lactato, convertir a los macrófagos de ayudantes del tumor en combatientes del tumor y hacer la radiación más efectiva en modelos de cáncer difíciles de tratar. Aunque HuL001 aún no es un fármaco clínico, el trabajo sugiere que apuntar a guardianes metabólicos como ENO1 podría convertirse en una forma potente de volver las propias defensas del tumor contra él y potenciar terapias existentes como la radioterapia.
Cita: Lin, YS., Chang, HY., Hong, WZ. et al. Targeting ENO1 reprograms macrophage polarization to trigger antitumor immunity and improves the therapeutic effect of radiotherapy. Cell Death Dis 17, 194 (2026). https://doi.org/10.1038/s41419-026-08416-7
Palabras clave: metabolismo tumoral, polarización de macrófagos, radioterapia, inmunoterapia, lactato