Clear Sky Science · es
Sec8: un nuevo regulador positivo de RIG-I en la defensa antiviral frente a virus de ARN
Cómo nuestras células detectan virus sigilosos
Muchos virus peligrosos, incluida la gripe y virus emergentes de origen animal, contienen su material genético en forma de ARN. Nuestras células dependen de sistemas de alarma internos para detectar rápidamente a estos invasores y desencadenar una respuesta antiviral. Este trabajo explora una proteína celular poco conocida llamada Sec8 y muestra que desempeña discretamente un papel central en mantener a uno de nuestros sensores virales clave, RIG‑I, vivo y activo el tiempo suficiente para protegernos.
Una alarma celular bajo amenaza
RIG‑I es una “alarma anti‑intrusos” molecular que patrulla el interior de las células en busca de fragmentos de ARN viral. Cuando detecta ARN sospechoso, cambia de forma, se activa y envía señales que finalmente inducen interferones de tipo I: potentes moléculas de advertencia que ayudan a las células vecinas a resistir la infección y a activar defensas inmunitarias. Dado que una alarma sobreactivada puede causar inflamación dañina o enfermedades autoinmunes, las células controlan estrictamente los niveles de RIG‑I. Varias proteínas pueden marcar a RIG‑I para su destrucción añadiendo pequeñas cadenas de ubiquitina, dirigiéndolo así al “trituradora” celular llamado proteasoma. Hasta ahora no estaba claro qué factores celulares adicionales protegen a RIG‑I de ser destruido prematuramente, especialmente durante una infección activa por virus de ARN.
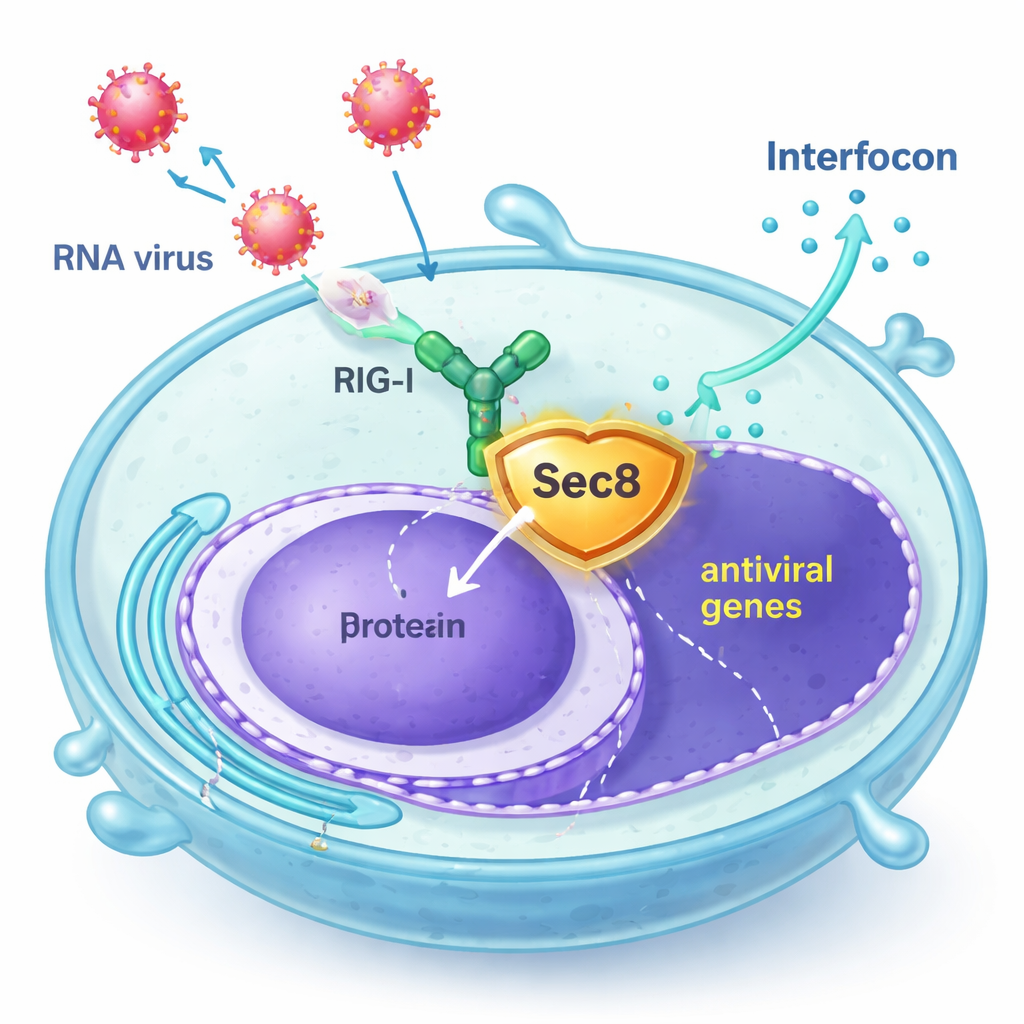
Sec8 interviene como guardaespaldas
Los autores descubrieron que Sec8, conocido sobre todo como parte de un complejo de ocho proteínas que ayuda a que vesículas secretoras se fusionen con la superficie celular, en realidad potencia la señalización antiviral. En líneas celulares humanas y en células inmunitarias primarias de ratón, aumentar los niveles de Sec8 condujo a una mayor activación de genes relacionados con el interferón tras la infección con virus de ARN como el virus de la estomatitis vesicular (VSV) y el virus de Sendai, o tras la exposición a ARN viral sintético. Por el contrario, reducir Sec8 disminuyó la producción de interferón y de genes estimulados por interferón, dejando a las células menos capaces de resistir la replicación viral. Estos hallazgos sugieren que Sec8 actúa no solo en la secreción, sino como un regulador positivo dentro de la vía de alarma antiviral.
Bloqueando la trituradora celular
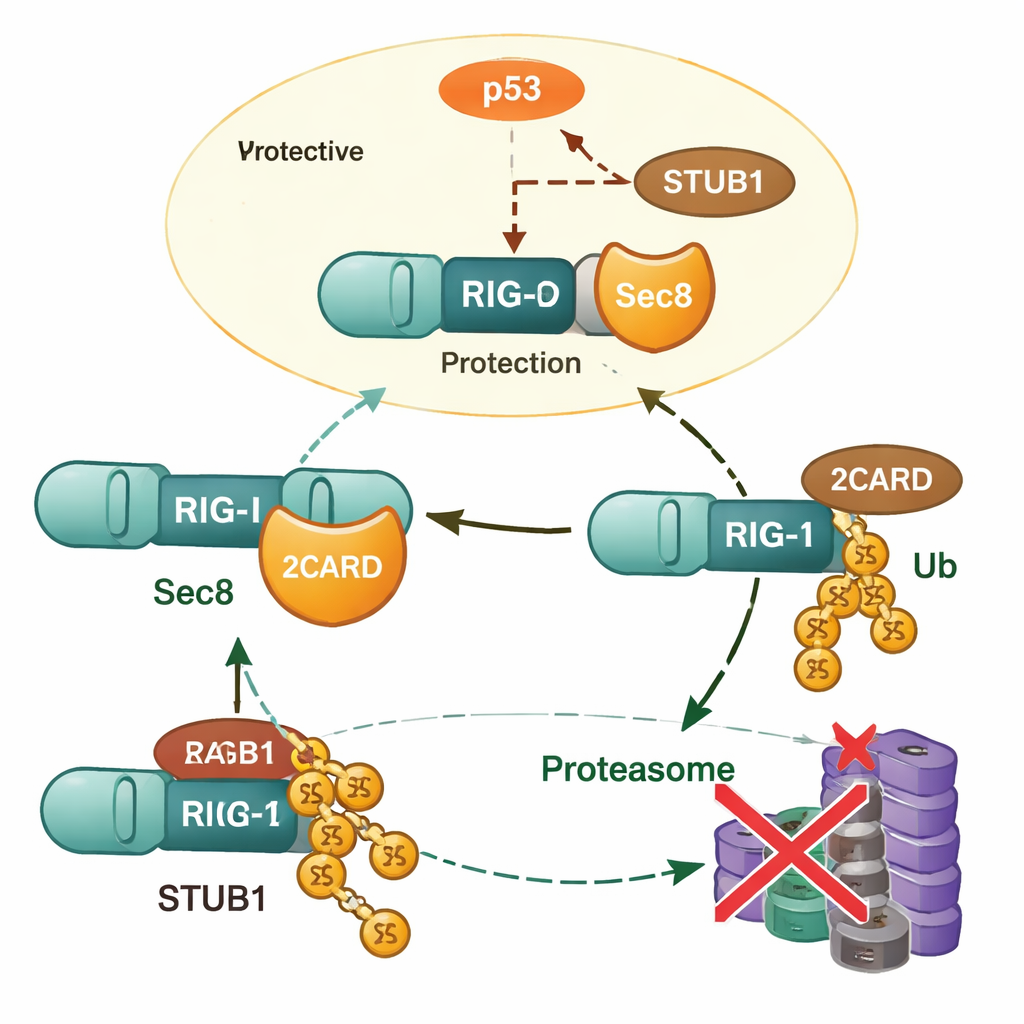
Indagando más, los investigadores encontraron que Sec8 no aumenta la expresión génica de RIG‑I; en cambio, evita que la proteína RIG‑I sea degradada. Cuando Sec8 fue eliminado, los niveles de RIG‑I descendieron más rápido, y esta pérdida pudo ser prevenida por fármacos que bloquean el proteasoma, implicando así la maquinaria celular de reciclaje de proteínas. El equipo identificó a otra proteína, STUB1, como un “marcador” clave que añade un tipo específico de cadena de ubiquitina (enlazada por K48) a RIG‑I en un aminoácido llamado lisina 190. Esta marca señala a RIG‑I para su destrucción. Sec8 interfiere con este proceso de dos maneras: compite físicamente con STUB1 por unirse a la misma región de activación de RIG‑I, y reduce la cantidad de STUB1 que la célula produce en primer lugar.
Sec8, p53 y el control del marcador
Para explicar cómo Sec8 reduce la producción de STUB1, los autores estudiaron la regulación génica. Identificaron un tramo corto de ADN que actúa como el interruptor central (promotor) del gen STUB1 y mostraron que la famosa proteína supresora de tumores p53 se une a esa región y eleva los niveles de STUB1. Sec8 atenúa tanto la cantidad como la fosforilación activadora de p53, de modo que p53 ya no puede impulsar la producción de STUB1 con la misma eficacia. Cuando p53 fue bloqueada o STUB1 silenciada, los efectos nocivos de perder Sec8 sobre la producción de interferón y el crecimiento viral se revirtieron en gran medida. Esto sitúa a Sec8 en la cima de una cadena reguladora que va desde p53 a STUB1 y, finalmente, a la estabilidad de RIG‑I.
Del placa de cultivo a animales vivos
El equipo probó entonces la importancia de Sec8 en ratones diseñados genéticamente para carecer del gen Sec8 específicamente en ciertas células inmunitarias. Tras la infección con VSV, estos animales produjeron menos interferón, mostraron cantidades más altas de virus en órganos como el bazo, el hígado y los pulmones, y presentaron mayor daño pulmonar, más pérdida de peso y menor supervivencia que los ratones de control. Estos resultados in vivo confirmaron que Sec8 no es un actor menor, sino un protector significativo frente a la infección por virus de ARN en un organismo completo.
Por qué esto importa para futuras terapias
En términos claros, este estudio muestra que Sec8 actúa como un guardaespaldas para el sensor antiviral RIG‑I. Al mantener a raya a la proteína “marcadora” STUB1 y al proteger directamente a RIG‑I de ser enviado a la trituradora celular, Sec8 permite que las células monten una respuesta de interferón oportuna y controlen mejor los virus de ARN. Comprender este eje recién descrito p53–STUB1–RIG‑I abre la puerta a futuras estrategias antivirales que estabilicen RIG‑I o imiten las acciones protectoras de Sec8, potencialmente mejorando nuestras defensas contra una amplia gama de infecciones virales basadas en ARN.
Cita: Wang, L., Ma, W., Hou, P. et al. Sec8: a novel positive regulator of RIG-I in anti-RNA viral defense. Cell Death Dis 17, 165 (2026). https://doi.org/10.1038/s41419-026-08414-9
Palabras clave: inmunidad innata, virus de ARN, RIG-I, ubiquitinación, señalización de interferón