Clear Sky Science · es
La transmisión de lactato desde células tumorales hipóxicas promueve la senescencia y la polarización M2 de macrófagos a través del eje DNMT1-NHE7 para acelerar la progresión del cáncer endometrial
Por qué importa privar a los tumores de oxígeno
El cáncer endometrial, que se origina en el revestimiento del útero, está aumentando en incidencia a nivel mundial. Muchos tumores avanzados son difíciles de tratar porque recurren, se diseminan o resisten las terapias estándar. Este estudio examina lo que sucede dentro de estos tumores cuando sufren falta de oxígeno —una característica común en cánceres de crecimiento rápido— y demuestra cómo un producto de desecho sencillo, el lactato, puede reprogramar las células inmunitarias cercanas para ayudar al cáncer en vez de combatirlo.
El bajo oxígeno convierte a los tumores en fábricas de lactato
A medida que las células del cáncer endometrial se multiplican, su suministro sanguíneo no da abasto y se crean zonas de baja oxigenación, o hipoxia. Las células responden activando un regulador maestro llamado HIF1A que reconfigura su forma de obtener energía. En lugar de depender principalmente de vías eficientes, las células aumentan la glucólisis, un proceso rápido pero menos eficiente que genera grandes cantidades de lactato. Los investigadores analizaron datos tumorales de cientos de pacientes y hallaron que niveles más altos de HIF1A se asociaban con mayor actividad de numerosos genes relacionados con la glucólisis y de transportadores que expulsan lactato desde las células cancerosas. Los pacientes cuyos tumores presentaban más HIF1A tendían a tener un peor pronóstico, lo que sugiere que este cambio metabólico está estrechamente vinculado a una enfermedad más agresiva.
Cómo los desechos del tumor reconfiguran a las células inmunitarias útiles
Los macrófagos son células inmunitarias que pueden atacar a los tumores o, por el contrario, apoyarlos, dependiendo de su estado. En este trabajo, el equipo mostró que bajo hipoxia, las células del cáncer endometrial liberan mucho más lactato al entorno. Este lactato se exporta mediante un transportador llamado MCT3 en las células tumorales y luego es importado por los macrófagos a través de otro transportador, MCT1. Una vez dentro, el lactato empuja a los macrófagos fuera de un modo defensivo y hacia el llamado estado M2, asociado con reparación de tejidos, supresión de la inflamación y, desgraciadamente, apoyo al crecimiento tumoral. En experimentos de laboratorio, los macrófagos expuestos a fluidos tumorales ricos en lactato mostraron más marcadores del tipo M2, y los fluidos que secretaron a su vez potenciaron el crecimiento, la movilidad y la invasión de las células cancerosas. 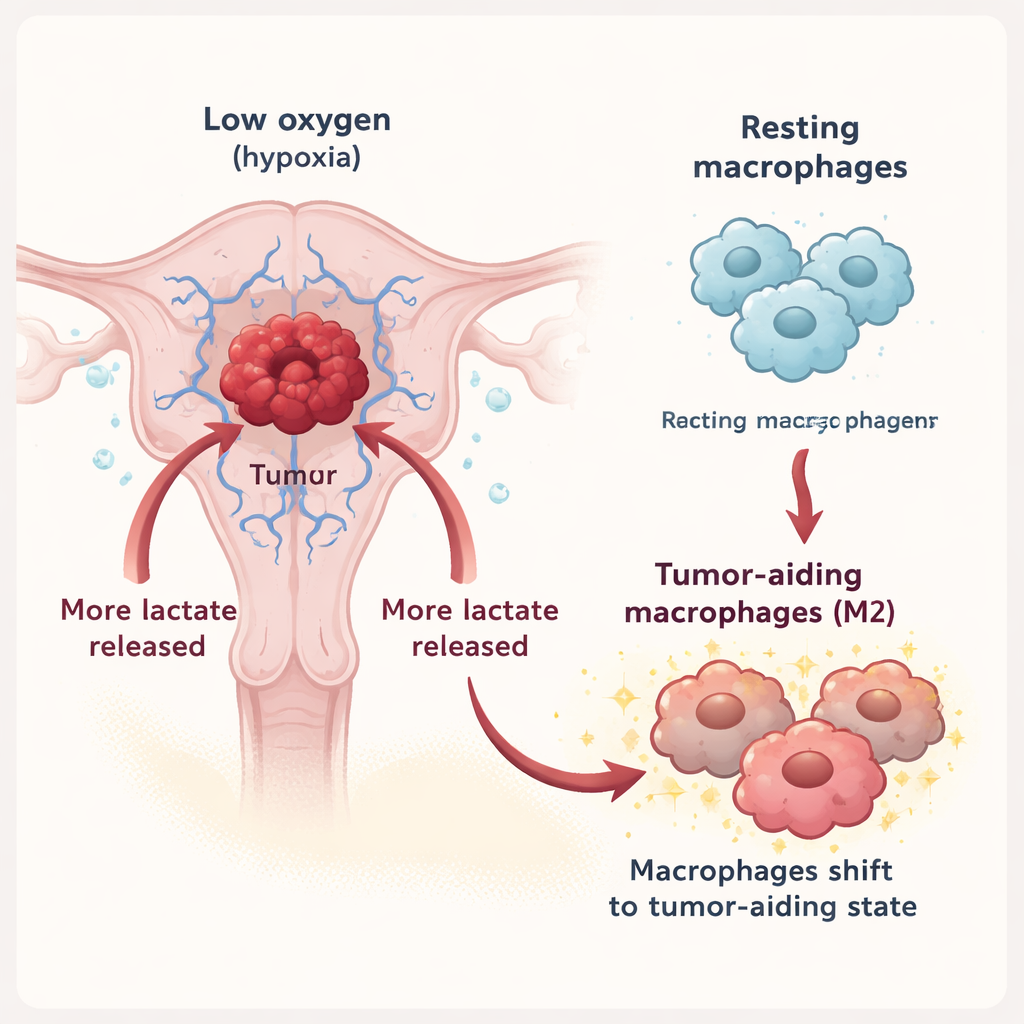
Un interruptor epigenético que silencia una “válvula de pH” celular
El estudio avanza un paso más al descubrir el interruptor molecular dentro de los macrófagos que conecta el lactato derivado del tumor con este comportamiento nocivo. El lactato no solo flota libremente; puede modificar las proteínas histonas en el núcleo —una marca química conocida como lactilación— que influye en qué genes se activan o silencian. Los investigadores encontraron que el lactato aumenta una marca histona específica en la región de control del gen DNMT1, elevando su actividad. DNMT1 es una enzima que añade grupos metilo al ADN y puede silenciar genes. Uno de sus blancos aquí es NHE7, una proteína que ayuda a controlar la acidez en ciertos compartimentos celulares. Cuando DNMT1 aumenta, incrementa la metilación del gen NHE7, reprimiéndolo. La reducción de NHE7 altera el equilibrio del pH interno y activa una vía de señalización conocida como MAPK. Esta vía, a su vez, empuja a los macrófagos hacia el estado M2 que favorece al tumor y hacia una forma de envejecimiento llamada senescencia, que los fija en un modo crónico y pro‑tumoral.
De la reacción en cadena molecular a tumores de crecimiento más rápido
Para comprobar si esta cadena de sucesos tiene efecto en organismos vivos, los científicos crearon modelos murinos en los que células humanas de cáncer endometrial crecían junto con macrófagos similares a los humanos. Cuando se suministró lactato adicional, los tumores crecieron más, mostraron más células en división y contenían más macrófagos tipo M2 y senescentes con alto DNMT1 y bajo NHE7. De manera notable, cuando los macrófagos fueron modificados para sobreexpresar NHE7, esto atenuó el efecto potenciador del lactato sobre el tumor: los tumores fueron más pequeños, presentaron más células en muerte y contenían menos macrófagos M2 y senescentes. Bloquear la enzima DNMT1 o la vía MAPK también debilitó la capacidad del lactato para reprogramar macrófagos, reforzando la idea de que estas moléculas forman un eje conectado. 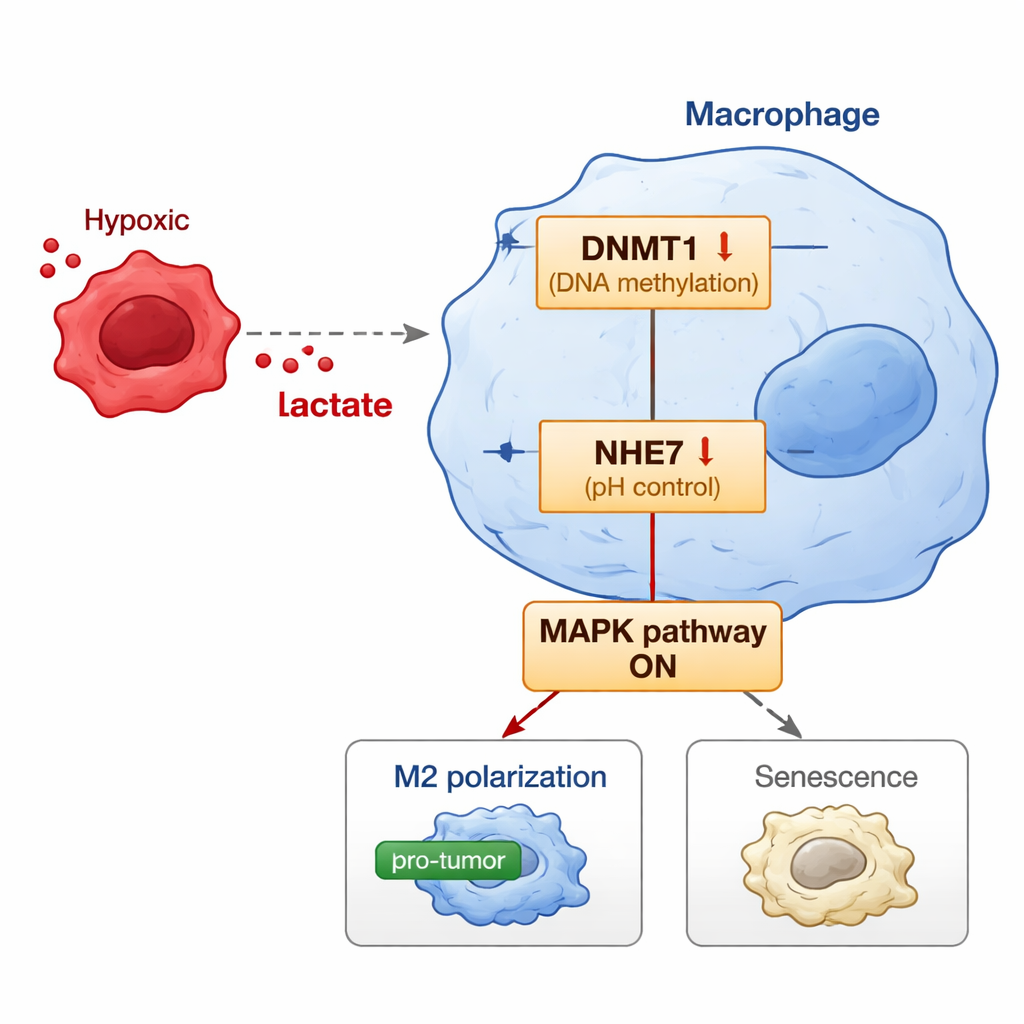
Convertir las propias artimañas del tumor en blancos terapéuticos
Para el público general, el mensaje clave es que los tumores endometriales pueden emplear la hipoxia y el lactato —antes considerados simples residuos celulares— para “lavar el cerebro” a las células inmunitarias cercanas y hacer que ayuden al cáncer. Lo hacen mediante un relevo epigenético: el lactato aumenta DNMT1, que silencia NHE7, lo que a su vez activa señales que fijan a los macrófagos en un estado envejecido y favorable al tumor. Interferir en cualquier paso de esta cadena lactato–DNMT1–NHE7–MAPK podría restaurar una mayor actividad inmunitaria antitumoral y frenar el crecimiento del cáncer. Este trabajo apunta a terapias futuras que no solo ataquen las células cancerosas directamente, sino que también reeduquen a las células inmunitarias circundantes que el tumor ha puesto a su favor.
Cita: Yang, S., Ma, Y., Wu, T. et al. Lactate transmission from hypoxic tumor cells promotes macrophage senescence and M2 polarization via the DNMT1-NHE7 axis to accelerate endometrial cancer progression. Cell Death Dis 17, 185 (2026). https://doi.org/10.1038/s41419-026-08411-y
Palabras clave: cáncer endometrial, microambiente tumoral, metabolismo del lactato, polarización de macrófagos, regulación epigenética