Clear Sky Science · es
Más allá del metabolismo: explorando las implicaciones regulatorias y terapéuticas del lactato y la lactilación en la muerte celular regulada por el cáncer
Por qué un “producto de desecho” de la glucosa importa en el cáncer
Durante décadas, el lactato —la sustancia que hace que los músculos sobreesforzados ardan— fue descartado como basura celular. Este artículo de revisión muestra que en el cáncer el lactato está lejos de ser un desecho. Actúa como combustible, como señal química e incluso como un interruptor que puede decidir si las células tumorales viven o mueren. Comprender este papel oculto puede abrir nuevas vías para inducir que las células cancerosas se autodestruyan mientras se preserva el tejido sano.
El atajo de la glucosa que reconecta las células cancerosas
Las células cancerosas son famosas por su “diente dulce”. Incluso cuando el oxígeno es abundante, prefieren descomponer la glucosa rápidamente en lactato en lugar de oxidarla completamente en las mitocondrias, un cambio conocido como efecto Warburg. Esta estrategia permite a los tumores generar energía y bloques de construcción a gran velocidad. La avalancha resultante de lactato se expulsa a través de transportadores especiales, configurando un microambiente tumoral ácido y rico en nutrientes que favorece el crecimiento y ayuda a los tumores a adaptarse al estrés, como la hipoxia o la quimioterapia.
El lactato como regulador de distintos tipos de muerte celular
La muerte celular en nuestro organismo suele estar estrechamente controlada, ayudando a eliminar células dañadas o peligrosas. Las células cancerosas con frecuencia eluden estos programas. Los autores describen cómo el lactato puede bloquear y también desencadenar varias vías de muerte regulada: apoptosis ("suicidio" celular), autofagia (autodigestión), ferroptosis (daño de membrana impulsado por hierro), piroptosis (estallido inflamatorio) y cuproptosis (colapso impulsado por cobre). Cuando las células tumorales generan o importan cantidades moderadas de lactato, tienden a usarlo como combustible y como señal de supervivencia, activando vías que las protegen frente a la quimioterapia, la escasez de nutrientes o fármacos dirigidos. Pero cuando el lactato se acumula dentro de las células, por ejemplo si se bloquea su exportación, el estrés ácido resultante y el daño mitocondrial pueden cambiar el sentido del interruptor y empujar a las células hacia la apoptosis o la ferroptosis.
Lactilación: cuando el lactato escribe sobre las proteínas
Un hallazgo reciente llamativo es que el lactato puede convertirse en una pequeña etiqueta química y unirse a residuos de lisina en proteínas, una modificación conocida como lactilación. Enzimas actúan como “escritores” y “borradores” de estas etiquetas, decorando tanto a las histonas asociadas al ADN como a muchas otras proteínas. Estas marcas cambian qué genes se activan, cómo se comportan las enzimas y la estabilidad de reguladores clave. En el cáncer, la lactilación ajusta finamente el equilibrio entre supervivencia y autodestrucción. Puede, por ejemplo, aumentar proteínas que bloquean la apoptosis, potenciar el reciclaje mediante autofagia, proteger a las células de la ferroptosis al reforzar el control del hierro y aumentar los antioxidantes, o alterar formas emergentes de muerte como la cuproptosis al modificar cómo las células manejan proteínas sensibles al cobre.
Una conversación bidireccional entre metabolismo y programas de muerte
La relación no es unilateral: las vías de muerte celular también remodelan cómo los tumores usan la glucosa y producen lactato. Cuando las mitocondrias se dañan durante una apoptosis temprana o la mitofagia (la eliminación selectiva de mitocondrias), las células a menudo recurren a la glucólisis rápida, elevando la producción de lactato. Las células de soporte circundantes, como los fibroblastos asociados al cáncer, pueden sufrir un reconectado similar y convertirse en fábricas de lactato que alimentan a las células tumorales próximas. Otros tipos de muerte, como la ferroptosis, tienden a suprimir la glucólisis y por tanto reducir los niveles de lactato. El resultado es un bucle de retroalimentación dinámico en el que metabolismo y mecanismos de muerte se ajustan continuamente entre sí a medida que el tumor evoluciona y responde al tratamiento.
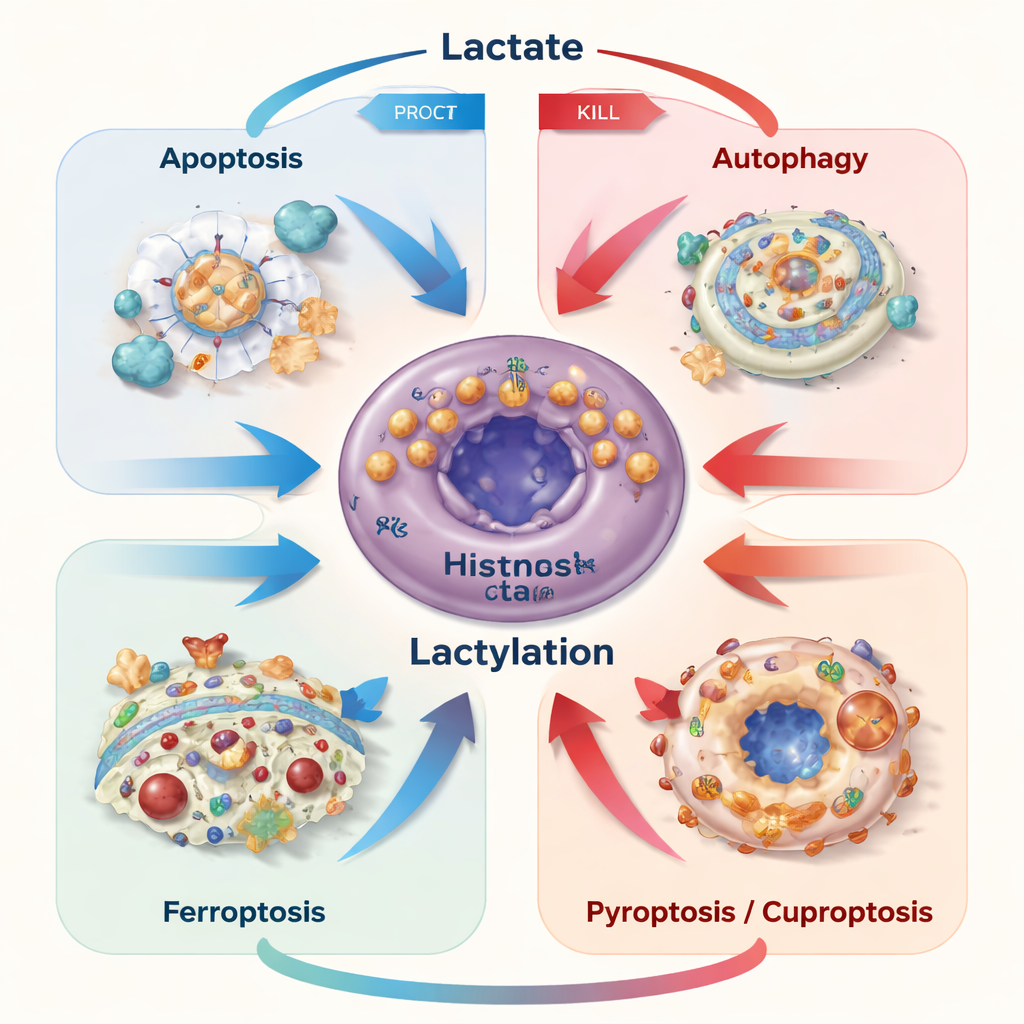
Convertir una debilidad en una estrategia terapéutica
Dado que el lactato y la lactilación pueden proteger o matar a las células cancerosas según el contexto, los autores sostienen que las terapias deben hacer más que simplemente bloquear la producción de lactato. En su lugar, los tratamientos futuros podrían redirigir selectivamente los flujos de lactato, ajustar sus transportadores o dirigirse a marcas específicas de lactilación para inclinar a las células cancerosas hacia la muerte mientras se reactivan las células inmunitarias antitumorales que actualmente están paralizadas por el ambiente ácido. Sistemas inteligentes de liberación de fármacos y nanomedicinas que responden a niveles locales de lactato o pH están surgiendo como formas de aplicar esta precisión. En términos sencillos, el mensaje del artículo es que lo que antes parecía basura metabólica es en realidad una potente perilla de control sobre el destino de las células cancerosas —y aprender a girar esa perilla correctamente podría hacer que las terapias existentes sean mucho más eficaces.
Cita: Chen, C., Lin, A., Zhao, J. et al. Beyond metabolism: exploring the regulatory and therapeutic implications of lactate and lactylation in cancer-regulated cell death. Cell Death Dis 17, 184 (2026). https://doi.org/10.1038/s41419-026-08410-z
Palabras clave: lactato, lactilación, muerte celular cancerosa, metabolismo tumoral, ferroptosis