Clear Sky Science · es
Huellas funcionales de la deficiencia de recombinación homóloga en el cáncer de próstata reveladas por la fragmentación del ctDNA y la accesibilidad de factores de transcripción
Por qué esto importa para los pacientes con cáncer
Muchos hombres con cáncer de próstata avanzado podrían beneficiarse de fármacos que explotan vulnerabilidades en la forma en que sus tumores reparan el ADN dañado. Sin embargo, hoy en día los médicos a menudo no identifican quién responderá porque las pruebas suelen requerir biopsias de tejido difíciles y se centran en solo un puñado de genes. Este estudio muestra cómo una extracción de sangre sencilla puede convertirse en una lectura rica y multilayer de estas debilidades en la reparación del ADN, guiando potencialmente decisiones de tratamiento más precisas y menos agresivas.
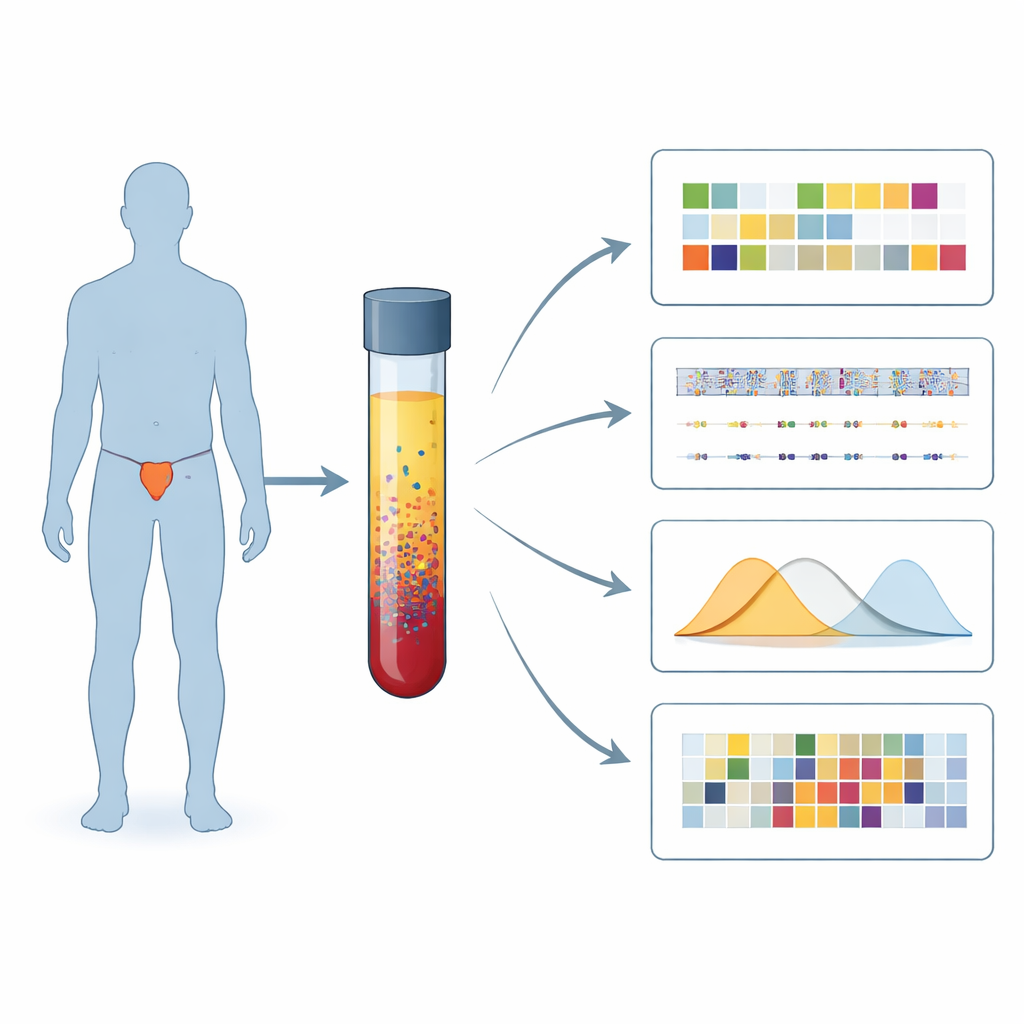
Una nueva forma de leer señales del cáncer en la sangre
Los investigadores se centraron en un problema concreto de reparación denominado deficiencia de recombinación homóloga, o HRD, que hace que los tumores sean especialmente vulnerables a fármacos como los inhibidores de PARP y a determinadas quimioterapias. En lugar de depender de muestras tumorales tomadas del hueso o de la próstata, analizaron fragmentos de ADN tumoral que circulan en el torrente sanguíneo, conocidos como ADN tumoral circulante. De 375 hombres con cáncer de próstata metastásico, seleccionaron a 106 cuyos sueros contenían suficiente ADN tumoral para un estudio en profundidad y aplicaron varias pruebas complementarias a las mismas muestras de plasma.
Más allá de las mutaciones en un solo gen
Primero, secuenciaron un panel de genes clave de reparación del ADN, incluidos actores bien conocidos como BRCA2, BRCA1 y PALB2, junto con otros genes que modulan la agresividad de los tumores prostáticos. BRCA2 emergió como el gen de reparación alterado con más frecuencia y a menudo apareció junto con la pérdida de otras salvaguardas importantes como PTEN y RB1. Pero el equipo también examinó cambios a gran escala en la estructura cromosómica en todo el genoma, empleando secuenciación de genoma completo a baja profundidad para calcular una puntuación de inestabilidad genómica. Los tumores con genes BRCA dañados, o con puntuaciones altas, presentaban genomas muy reordenados y se asociaban con una supervivencia global peor, lo que subraya que los grandes cambios estructurales pueden ser tan informativos como las mutaciones específicas.
Huellas de fallo de reparación en los patrones de mutación
En un subconjunto de pacientes, los científicos profundizaron aún más secuenciando todas las regiones codificantes de proteínas para leer el patrón detallado de mutaciones acumuladas con el tiempo. Ciertas combinaciones de cambios de bases y pequeñas inserciones o deleciones actúan como huellas dactilares de los procesos que las generaron. Encontraron que firmas clásicas vinculadas a HRD, como una denominada SBS3 y otro patrón de indels conocido como ID6, estaban enriquecidas en tumores con defectos en genes de reparación y alta inestabilidad genómica. Otras firmas apuntaron a problemas distintos, como fallos en la reparación por desajuste o un subtipo específico impulsado por CDK12, subrayando que diferentes fallos en la reparación del ADN dejan cicatrices reconocibles y distintas en el genoma.
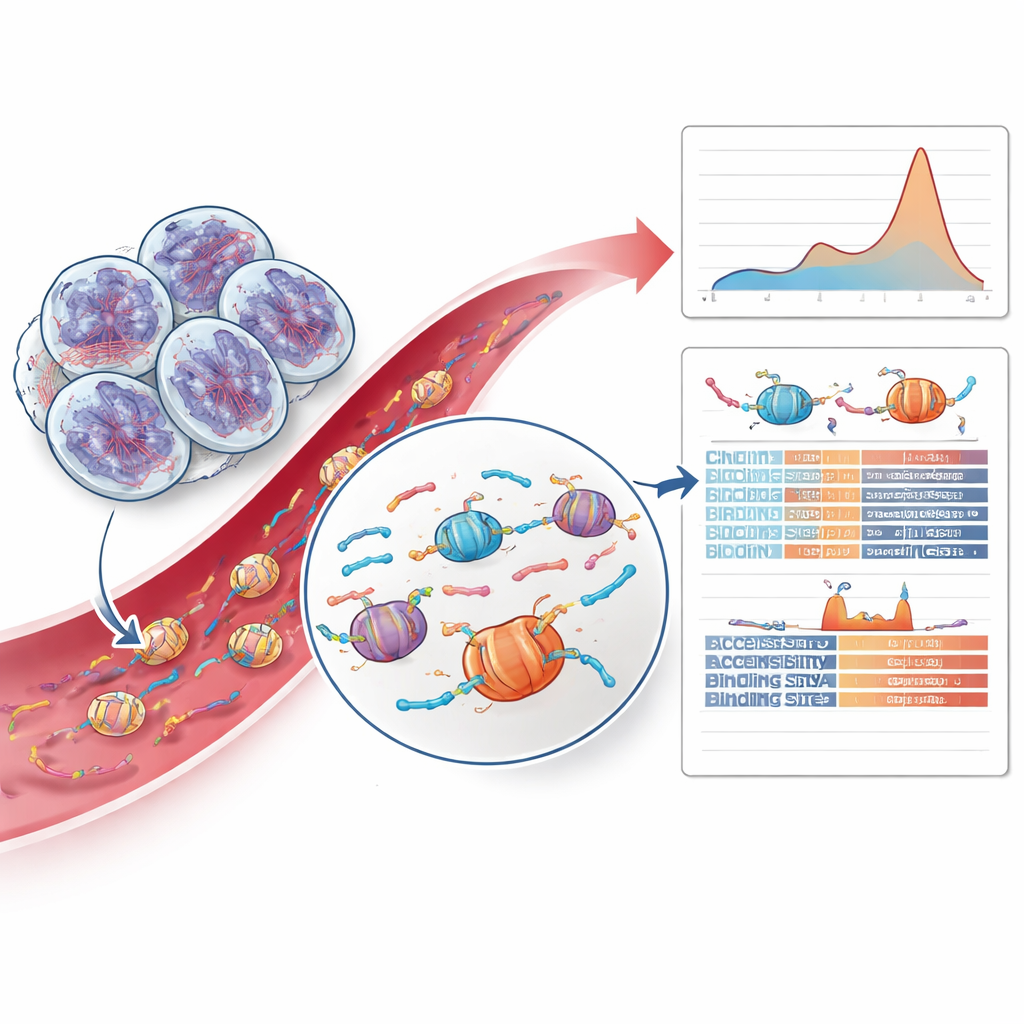
Decodificando patrones de fragmentos de ADN y pistas de cromatina
La parte más innovadora del trabajo fue más allá de las mutaciones y examinó cómo se fragmentaba el ADN tumoral. Cuando las células mueren, su ADN se corta alrededor de paquetes proteicos llamados nucleosomas, creando fragmentos con longitudes y patrones de extremos característicos. El equipo descubrió que los tumores con HRD mostraban un exceso relativo de fragmentos algo más largos correspondientes a dos nucleosomas, un cambio que no se observó en otros cánceres de próstata ni en controles sanos. Al entrenar un modelo de aprendizaje automático cauteloso con longitudes de fragmentos y características de los extremos de los fragmentos, pudieron detectar casos positivos para HRD a partir de la sangre con una precisión prometedora. También indagaron en la accesibilidad de distintas regiones del genoma alrededor de sitios de unión de factores de transcripción —proteínas que regulan la actividad génica— y encontraron que ciertos sitios de unión de dedos de zinc eran menos accesibles en tumores con HRD, lo que sugiere cambios más profundos relacionados con la reparación en la organización de la cromatina.
Qué podría significar esto para los pacientes
En conjunto, estas capas de información —desde mutaciones en genes específicos y grandes reordenamientos cromosómicos hasta cambios sutiles en el tamaño de los fragmentos de ADN y la accesibilidad de la cromatina— conforman una imagen más completa de la debilidad en la reparación del ADN en el cáncer de próstata. Para un lector no especialista, el mensaje clave es que una muestra de sangre analizada con rigor puede revelar no solo si un gen conocido como BRCA2 está mutado, sino si un tumor se comporta como si tuviera un defecto grave en la reparación, incluso cuando las pruebas habituales parecen normales. Si se valida en cohortes más grandes y diversas, este enfoque multimodal basado en sangre podría ayudar a los médicos a identificar con mayor fiabilidad quién puede beneficiarse de inhibidores de PARP o de fármacos con platino, monitorizar cambios a lo largo del tiempo y, en última instancia, personalizar la terapia mediante una prueba simple y repetible.
Cita: Vlachos, G., Moser, T., Lazzeri, I. et al. Functional footprints of homologous recombination deficiency in prostate cancer revealed by ctDNA fragmentation and transcription factor accessibility. Br J Cancer 134, 949–960 (2026). https://doi.org/10.1038/s41416-025-03301-0
Palabras clave: cáncer de próstata, biopsia líquida, reparación del ADN, ADN tumoral circulante, inhibidores de PARP