Clear Sky Science · es
Paisajes microambientales inmunosupresores en el cáncer gástrico con alta expresión de VISTA
Por qué las defensas del organismo a veces fallan frente al cáncer de estómago
Los tratamientos oncológicos modernos dependen cada vez más de reactivar el sistema inmunitario para que ataque los tumores. Sin embargo, en muchas personas con cáncer gástrico avanzado, estos potentes fármacos funcionan mal o dejan de hacerlo. Este estudio explora una razón importante: una molécula frenadora llamada VISTA que remodela el entorno local del tumor, transformando a las células inmunitarias de combatientes en espectadores o incluso en colaboradoras del cáncer. Comprender este interruptor oculto podría abrir la puerta a inmunoterapias más precisas y eficaces.
Un freno oculto en el vecindario tumoral
Los autores se centraron en VISTA, una proteína que se encuentra principalmente en ciertos glóbulos blancos que residen en y alrededor de los tumores. VISTA actúa como una señal de parada para las respuestas inmunitarias. Mientras que otros frenos como PD-1 y PD-L1 ya son diana de fármacos aprobados, el papel de VISTA en el cáncer gástrico no estaba claro. Para investigarlo, el equipo analizó tejido de 172 pacientes usando tinciones multicolores avanzadas para mapear muchos tipos celulares a la vez. También emplearon secuenciación de ARN unicelular y transcriptómica espacial en conjuntos de muestras más pequeños para examinar qué células presentan VISTA, qué están haciendo y exactamente dónde se ubican en el paisaje tumoral. 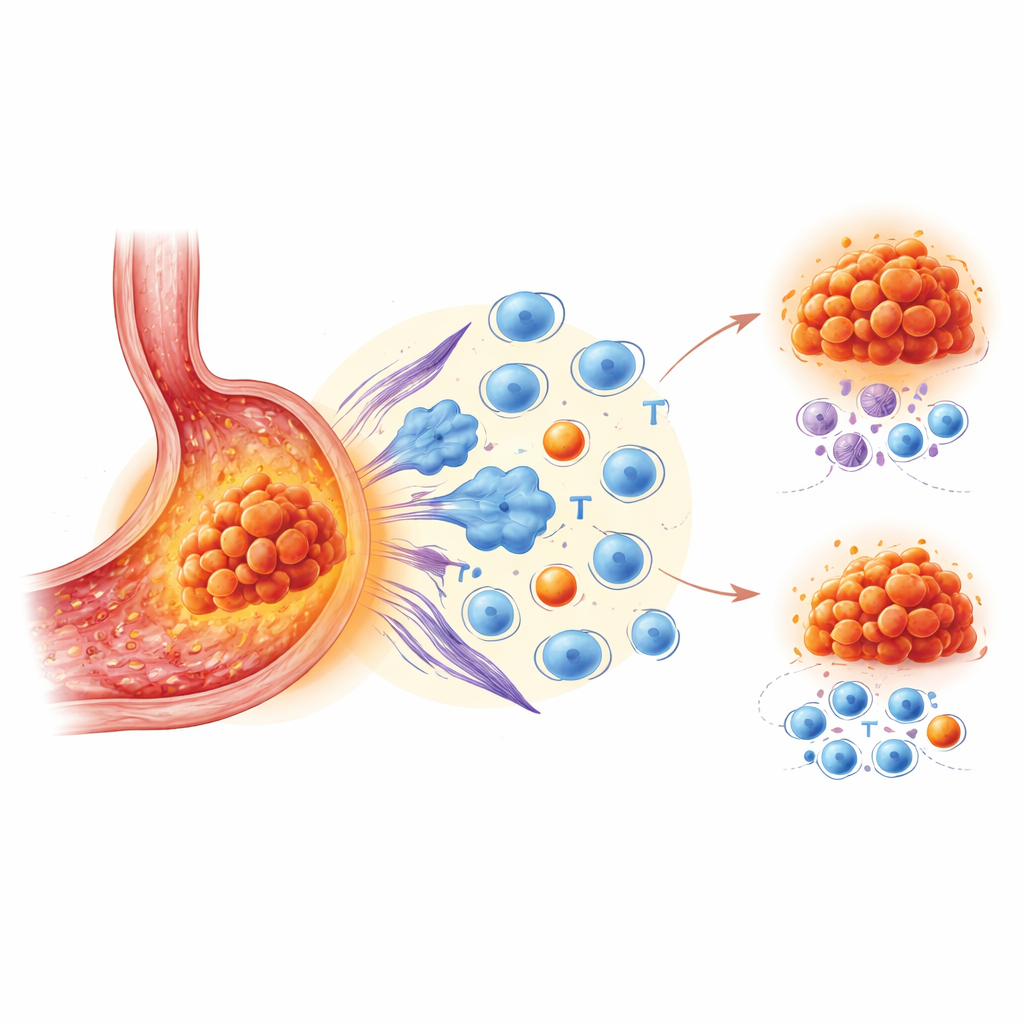
Cuando VISTA está alta, el sistema inmunitario se silencia
Al comparar tumores con niveles altos frente a bajos de VISTA, los investigadores hallaron un patrón consistente. Los cánceres ricos en VISTA estaban rodeados de células inmunitarias, pero no del tipo que monta un ataque potente. En su lugar, había una acumulación de células T citotóxicas agotadas que habían perdido su eficacia, células T reguladoras que frenan las respuestas inmunitarias, células de soporte formadoras de cicatriz llamadas fibroblastos y macrófagos inclinados hacia un estado que nutre al tumor. Los pacientes cuyos regiones tumorales contenían más VISTA tuvieron periodos más cortos antes del empeoramiento de la enfermedad tras la inmunoterapia, incluso al ajustar por otros factores clínicos. En otras palabras, un vecindario con alta VISTA parecía activo al microscopio pero funcionaba como una zona “inmune-silente” o supresora.
Macrófagos como intermediarios clave
Ahondando más, los científicos se centraron en monocitos y macrófagos, células inmunitarias que pueden devorar el cáncer o protegerlo. A nivel unicelular, el gen que codifica VISTA (llamado VSIR) estaba especialmente activo en varios subgrupos de macrófagos, en particular en aquellos que presentan fragmentos de proteínas tumorales en su superficie y en los que muestran rasgos de macrófagos tipo M2, o de reparación de heridas. Usando una línea temporal computacional del desarrollo celular, el equipo observó que VISTA se activaba a medida que las células pasaban de monocitos tempranos a macrófagos más maduros que se agrupaban alrededor de las células tumorales. El mapeo espacial confirmó que los macrófagos positivos para VISTA tendían a situarse cerca de las células cancerosas, y los pacientes cuyos tumores tenían más de estas células precisamente en esas ubicaciones evolucionaron peor tras el tratamiento con inhibidores de puntos de control inmunitario. 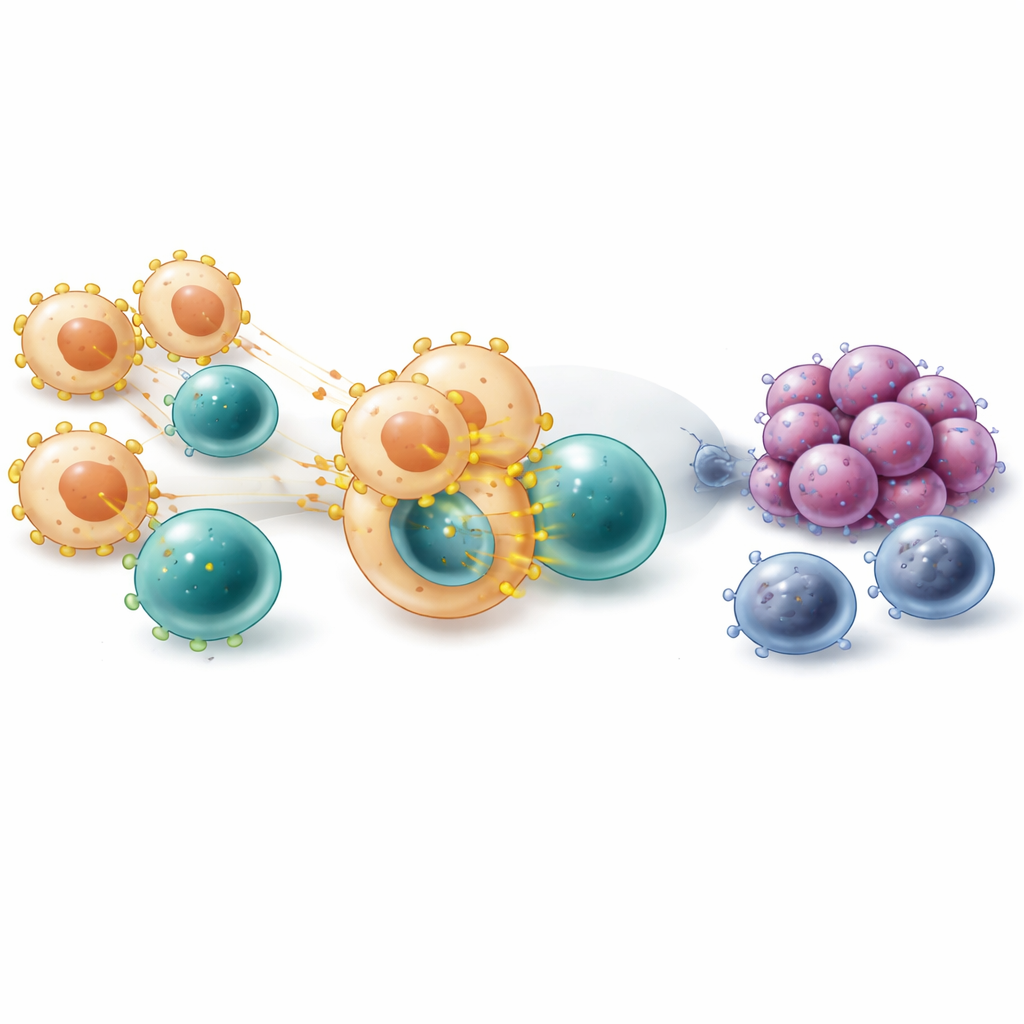
Cómo las células VISTA-positivas desgastan a las células T
El estudio también exploró cómo los macrófagos que portan VISTA se comunican con las células T. Los mapas de comunicación construidos a partir de datos de expresión génica sugirieron que estos macrófagos contactan frecuentemente a las células T mediante pares moleculares como LGALS9 y PTPRC, y a través de moléculas implicadas en la presentación de fragmentos tumorales a las células T. Esta presentación constante puede, con el tiempo, empujar a las células T desde un estado temprano y activo hacia un estado de estimulación crónica y agotamiento, marcado por múltiples señales inhibitorias en su superficie. En muestras donde los macrófagos mostraban mayor expresión de VSIR había más células T reguladoras y más células T citotóxicas agotadas, lo que refuerza la idea de que los macrófagos VISTA-positivos contribuyen al desgaste inmunitario en lugar de a un ataque eficaz y contundente.
Qué podría significar esto para tratamientos futuros
En conjunto, el trabajo sitúa a VISTA como un interruptor central que ayuda a los tumores gástricos a construir un nicho inmunosupresor, especialmente a través de macrófagos especializados que tanto presentan material tumoral como envían señales inhibitorias a las células T. Para los pacientes, esto sugiere que la alta expresión de VISTA marca una forma de resistencia a los fármacos inmunitarios actuales que sólo bloquean PD‑1 o PD‑L1. Bloquear VISTA —posiblemente en combinación con los inhibidores de puntos de control existentes— podría reactivar las células T y devolver el equilibrio hacia el control tumoral. Aunque se necesitan más estudios de laboratorio y ensayos clínicos, esta investigación ofrece una hoja de ruta para diseñar nuevas combinaciones terapéuticas e identificar qué pacientes tienen más probabilidades de beneficiarse.
Cita: Luo, Y., Peng, H., Yao, Q. et al. Immunosuppressive immune microenvironment landscapes in VISTA-high gastric cancer. Br J Cancer 134, 1066–1079 (2026). https://doi.org/10.1038/s41416-025-03290-0
Palabras clave: cáncer gástrico, microambiente tumoral, punto de control inmunitario, macrófagos, agotamiento de células T