Clear Sky Science · es
Espectro y funciones de canales iónicos y transportadores en osteoclastos
Por qué nuestros huesos necesitan pequeños guardianes
Nuestre esqueleto parece sólido e inmutable, pero está en constante destrucción y reconstrucción. Células especializadas llamadas osteoclastos actúan como la cuadrilla de demolición, disolviendo hueso antiguo para que pueda formarse hueso nuevo. Este artículo de revisión explora un reparto oculto de proteínas microscópicas “guardianas”: canales iónicos y transportadores que permiten que átomos cargados y nutrientes entren y salgan de los osteoclastos. Al comprender cómo estas pequeñas compuertas controlan la degradación ósea, los científicos esperan diseñar mejores tratamientos para la osteoporosis y otras enfermedades óseas.
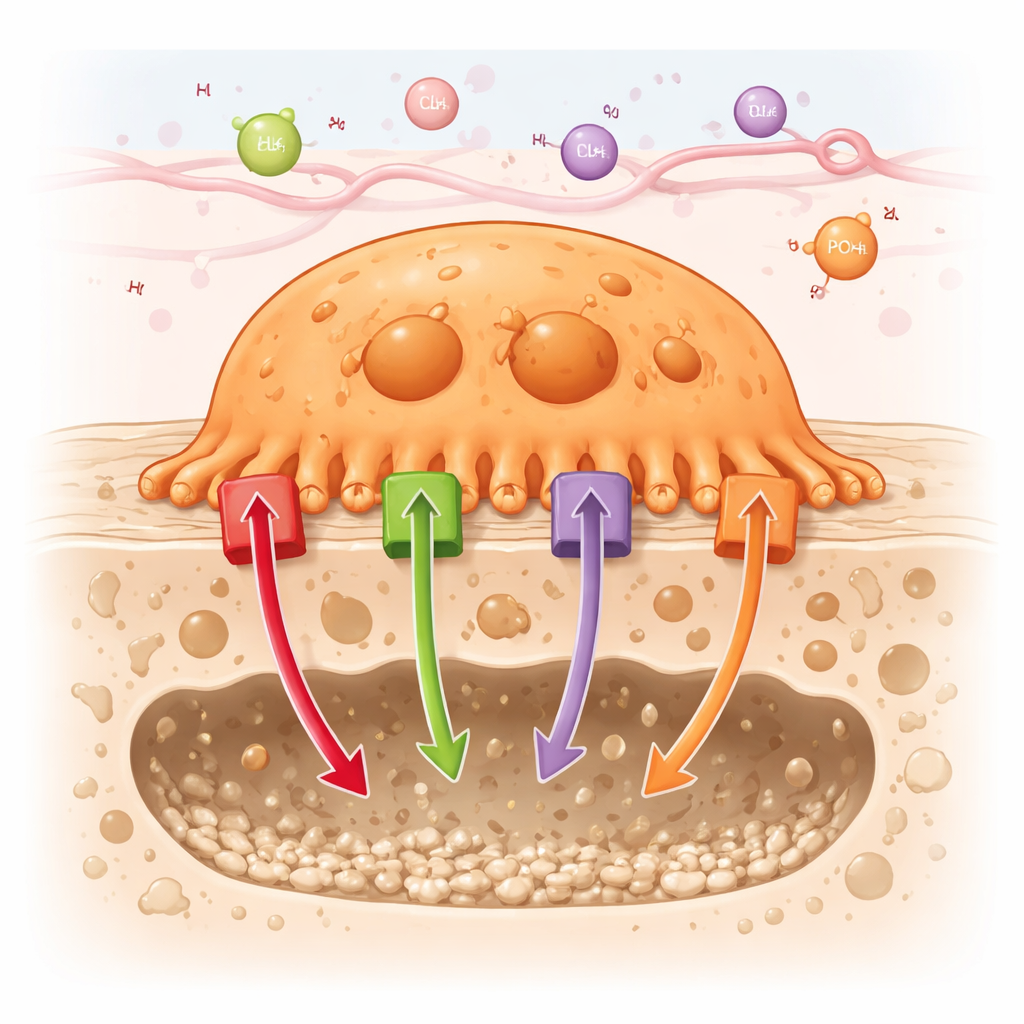
Cómo realizan su trabajo las células que devoran hueso
Los osteoclastos actúan fijándose firmemente a la superficie ósea y creando un bolsillo sellado donde pueden disolver minerales y digerir proteínas con seguridad. Para hacer que esta “cámara de digestión” en miniatura sea extremadamente ácida, los osteoclastos bombean un gran número de protones (iones de hidrógeno) hacia el interior del bolsillo. Al mismo tiempo, transportan otros iones —como cloruro, calcio y fosfato— a través de sus membranas y compartimentos internos. El artículo repasa unos 90 canales y transportadores distintos presentes en osteoclastos y los agrupa en seis familias, incluyendo bombas impulsadas por energía (ATPasas), canales de cationes y aniones, transportadores acoplados, transportadores de nutrientes y transportadores de la familia de las proteínas de unión a ATP (ABC).
Ácido, sal y energía: la maquinaria central
Dos sistemas proteicos destacan como centrales para la resorción ósea. Primero, las bombas vacuolares de protones conocidas como V-ATPasas empujan activamente protones hacia la cavidad de resorción, volviéndola lo bastante ácida como para disolver el mineral óseo y activar enzimas que degradan proteínas. Subunidades específicas de la V-ATPasa, como a3, d2 y varios componentes de V1, se enriquecen en el borde estriado del osteoclasto y en los lisosomas, y las anomalías genéticas en estas subunidades pueden debilitar el hueso o causar un engrosamiento óseo anómalo. Segundo, un intercambiador cloruro–protón llamado ClC-7, que forma pareja con una proteína denominada OSTM1, introduce iones cloruro en la misma región. Esto balancea la carga eléctrica y permite un bombeo continuo de protones. Cuando ClC-7 está mutado, humanos y ratones desarrollan osteopetrosis, una condición caracterizada por huesos demasiado densos pero frágiles, lo que ilustra lo esencial que es un flujo iónico adecuado para la salud esquelética normal.
Calcio, fosfato y otros actores auxiliares
Más allá de la producción de ácido, los osteoclastos dependen de un manejo fino del calcio y del fosfato. Una red de canales y bombas de calcio en la membrana celular, el retículo endoplásmico, los lisosomas y las mitocondrias genera “oscilaciones” rítmicas de calcio que activan genes clave para la formación y fusión de osteoclastos. Transportadores en el borde estriado y en el lado opuesto de la célula desplazan calcio y fosfato procedentes del hueso disuelto, ya sea reciclando estos iones dentro de la célula o devolviéndolos al torrente sanguíneo. Otros metales y minerales —como manganeso, magnesio, zinc, cobre y hierro— también son regulados por transportadores especializados y modulan la agresividad de la resorción osteoclástica. Por ejemplo, el hierro y ciertas formas de muerte celular relacionadas con el hierro pueden aumentar o reducir la actividad de los osteoclastos, mientras que los transportadores de zinc tienden a contener la pérdida ósea excesiva.
Control del tráfico dentro de la célula
Los canales iónicos no se limitan a la membrana exterior. Muchos se localizan en compartimentos internos como lisosomas, endosomas, el aparato de Golgi y las mitocondrias, creando una red de transporte por capas. Estas compuertas internas contribuyen a fijar el pH en las vesículas digestivas, la producción de energía en las mitocondrias y el movimiento de enzimas y restos. La revisión destaca cómo múltiples sistemas de canales cooperan: los intercambiadores sodio–hidrógeno regulan la acidez interna, los cotransportadores potasio–cloruro ayudan a mantener el potencial de membrana y el balance de cloruro, y los canales purinérgicos y mecanosensibles traducen señales químicas o mecánicas en cambios en la resorción ósea. Transportadores de nutrientes para glucosa, aminoácidos, nucleósidos y vitamina C sostienen además las elevadas demandas energéticas y biosintéticas de los osteoclastos activos en resorción.
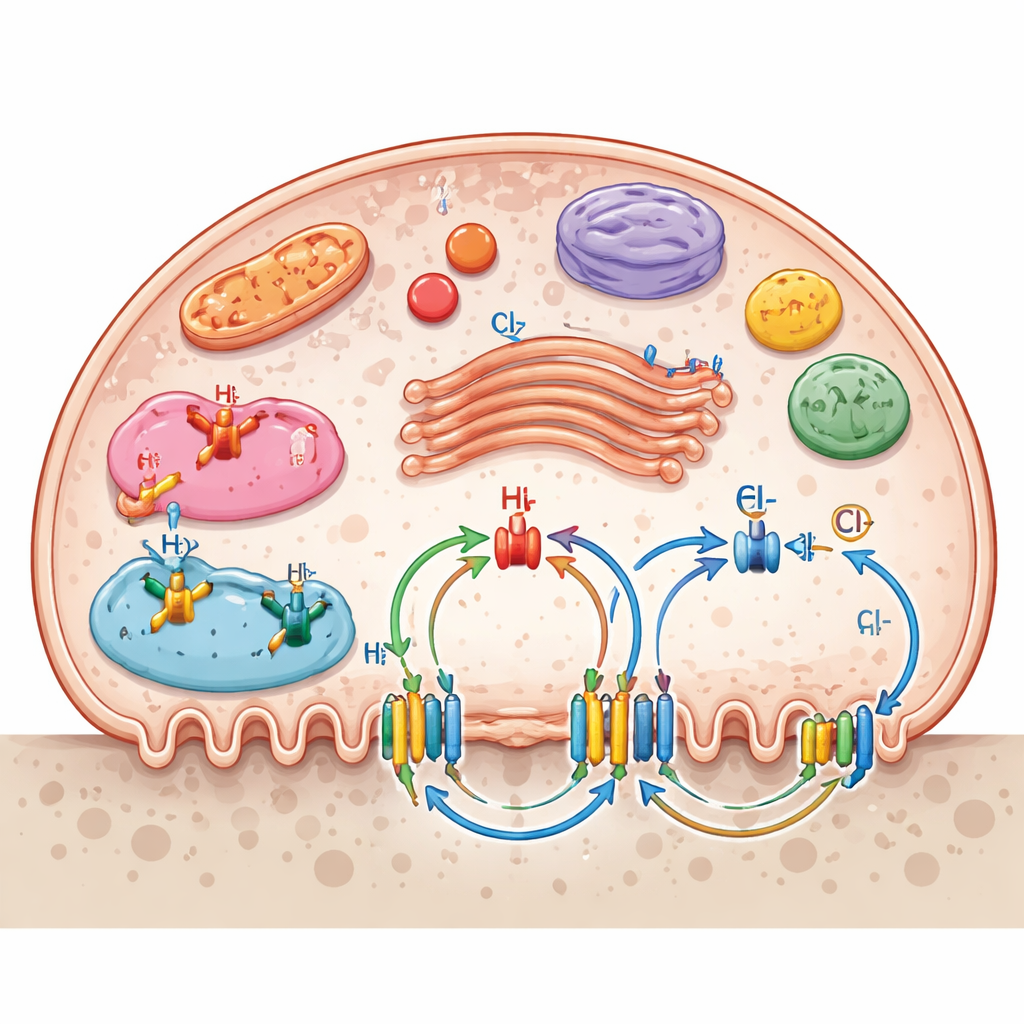
De la biología básica a nuevos tratamientos
Dado que numerosos trastornos óseos surgen cuando los osteoclastos están sobreactivos o poco activos, los canales y transportadores que guían su comportamiento son blancos farmacológicos atractivos. Los autores revisan compuestos existentes y experimentales que bloquean V-ATPasas, canales TRP de calcio, intercambiadores de cloruro, receptores purinérgicos y otros transportadores, así como ideas más recientes como interrumpir interacciones específicas entre subunidades o usar nanopartículas dirigidas para entregar fármacos directamente al hueso. Enfatizan que muchas de estas proteínas también se expresan en otros tejidos, por lo que alcanzar una verdadera especificidad osteoclástica sigue siendo un desafío. Aun así, a medida que las herramientas genómicas e imagenológicas revelan más sobre la localización y las interacciones de estos canales, el creciente “mapa iónico” de los osteoclastos probablemente producirá terapias más precisas para la osteoporosis, la pérdida ósea inflamatoria y enfermedades óseas genéticas raras.
Cita: Chen, H., Zhang, Y., Zhu, Y. et al. Spectrum and functions of ion channels and transporters in osteoclasts. Bone Res 14, 35 (2026). https://doi.org/10.1038/s41413-026-00513-9
Palabras clave: osteoclastos, canales iónicos, resorción ósea, V-ATPasa, osteoporosis