Clear Sky Science · es
PRMT6 es necesario para iniciar y amplificar la inflamación inducida por macrófagos en la osificación heterotópica al aumentar la expresión de CCL2
Cuando la curación se pasa de la raya
A veces, tras una lesión grave o una cirugía, el cuerpo intenta sanar con tanta intensidad que genera hueso nuevo donde no debería formarse. Esta condición dolorosa, denominada crecimiento óseo no deseado en tejidos blandos, puede inmovilizar articulaciones, complicar amputaciones y dificultar el movimiento cotidiano. Los tratamientos actuales son limitados y a menudo no evitan que el problema reaparezca. Este estudio descubre un interruptor temprano clave del sistema inmunitario que conecta el traumatismo con esta formación ósea anómala —y señala una ventana crítica y breve en la que un tratamiento dirigido podría detener el proceso antes de que comience. 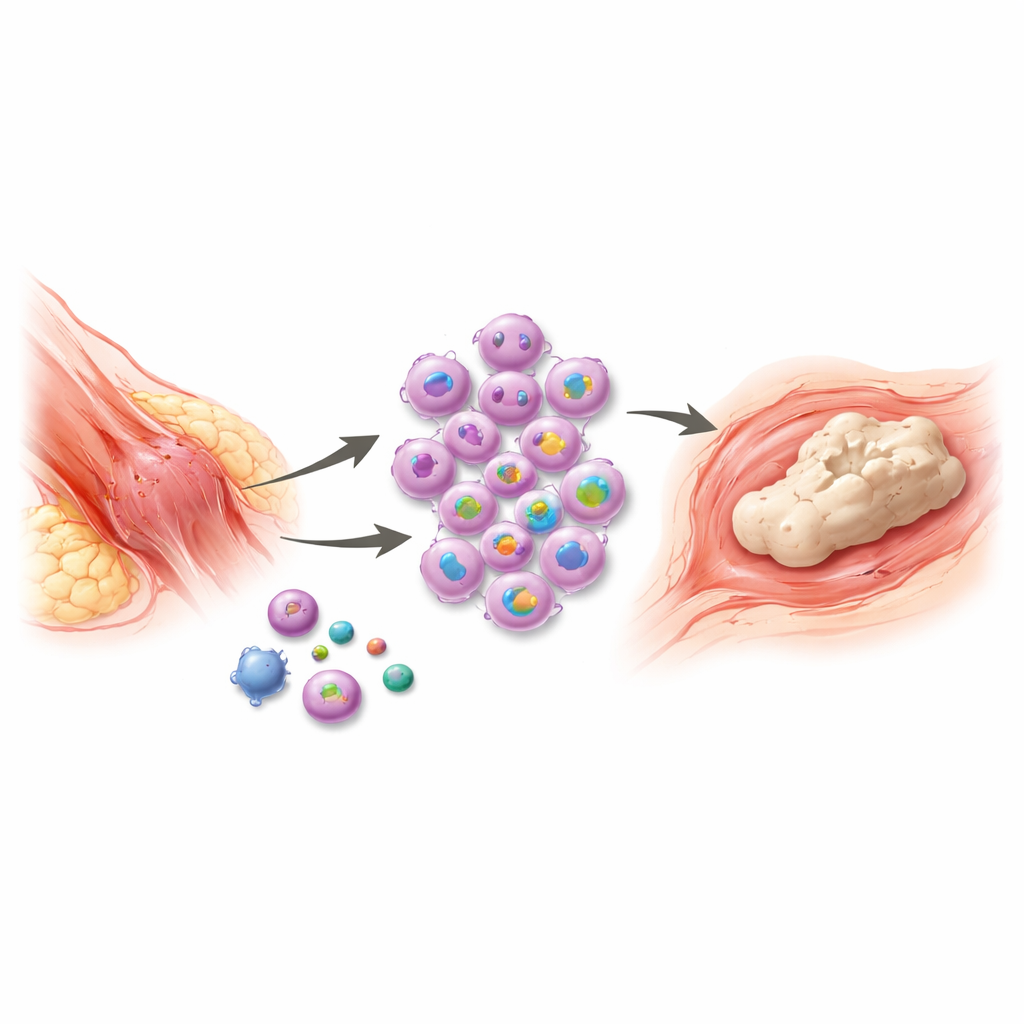
El problema del hueso en el lugar equivocado
Tras traumatismos importantes, como quemaduras, fracturas o cirugías ortopédicas, algunos pacientes desarrollan islotes de hueso dentro de músculos, tendones y otros tejidos blandos. El hueso nuevo se forma mediante un proceso similar al desarrollo óseo normal, que comienza con inflamación y termina con tejido maduro y mineralizado. Aunque los médicos saben que las células inmunitarias llamadas macrófagos son centrales en esta respuesta, el control paso a paso de cómo inician y mantienen la inflamación no estaba claro. Sin ese conocimiento, terapias como antiinflamatorios, radioterapia o la resección quirúrgica tardía tratan en su mayoría las consecuencias y no la causa, y la recurrencia es común.
El intermediario clave de la inflamación
Usando un modelo de ratón que combina lesión del tendón con una quemadura —que imita de forma cercana el trauma severo en humanos— los investigadores siguieron lo que ocurre en el sitio de la lesión a lo largo del tiempo. Observóse una acumulación rápida de macrófagos durante los primeros días tras la lesión, que luego persistió a medida que se formaba el hueso anómalo. Cuando eliminaron estas células, el hueso extra prácticamente desapareció y el tejido circundante mostró mucha menos alteración de vasos sanguíneos y células de sostén. Un análisis genético más profundo del tejido lesionado destacó una molécula en estos macrófagos que sobresalía: PRMT6, una enzima que modifica proteínas y ayuda a controlar qué genes se activan.
Un regulador molecular del volumen de la inflamación
El equipo encontró que los niveles de PRMT6 en macrófagos aumentaban rápidamente tras la lesión y en respuesta a señales de peligro y componentes bacterianos en el laboratorio. Ratones sin PRMT6, o ratones en los que PRMT6 se redujo selectivamente solo en macrófagos, presentaron muchos menos macrófagos en el sitio de la lesión y desarrollaron notablemente menos hueso anómalo. De manera importante, los tendones lesionados en estos animales cicatrizaron mejor, con tejido más ordenado y menos formación de cicatriz. Esto indica que PRMT6 no es necesario para la reparación saludable, sino que actúa como un control de volumen que amplifica una inflamación perjudicial. Cuando los investigadores bloquearon PRMT6 con un fármaco, solo funcionó si se administraba pronto —durante las primeras semanas tras la lesión. Comenzar el tratamiento más tarde tuvo poco efecto, revelando una ventana terapéutica estrecha pero potente. 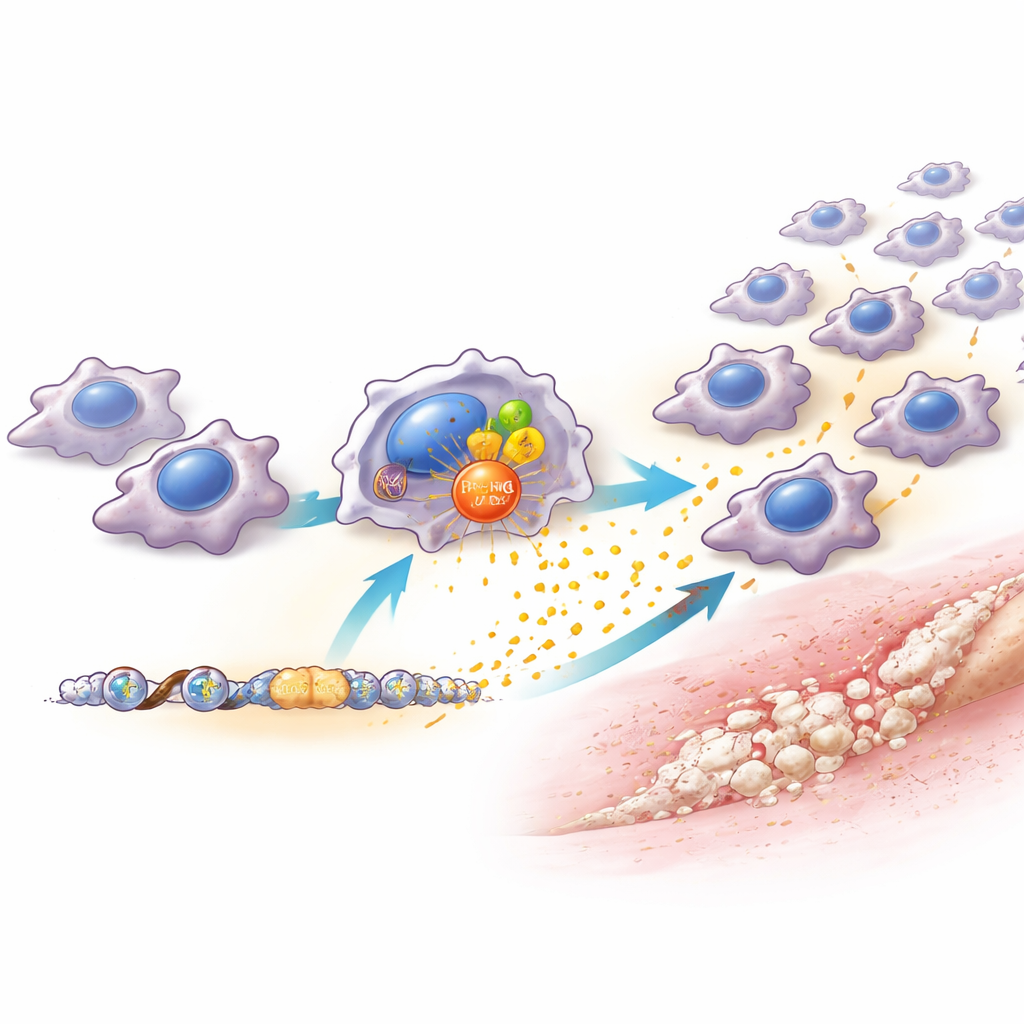
Cómo una señal atrae a muchas células inmunitarias
Para entender cómo ejerce PRMT6 este efecto, los científicos estudiaron los macrófagos en detalle. Sin PRMT6, estas células produjeron cantidades mucho menores de varios atractantes químicos, especialmente uno llamado CCL2, que normalmente recluta más monocitos y macrófagos desde el torrente sanguíneo hacia el tejido lesionado. PRMT6 ayuda a activar el gen de CCL2 de dos maneras: se asocia con el conocido regulador de la inflamación NF-κB y marca químicamente las proteínas que empaquetan el ADN cercanas para que ese gen sea más fácil de leer. Como resultado, los macrófagos con altos niveles de PRMT6 producen más CCL2, lo que atrae a macrófagos adicionales y crea un “centro inflamatorio” que favorece los vasos sanguíneos y las células progenitoras formadoras de hueso. Cuando CCL2 se redujo específicamente solo en macrófagos, el resultado imitó de cerca la pérdida de PRMT6: menos macrófagos, nichos inflamatorios más débiles y menos hueso adicional. Reponer CCL2 restauró parcialmente tanto la afluencia de macrófagos como el crecimiento óseo anómalo.
Una oportunidad dirigida para prevenir el hueso no deseado
En conjunto, el estudio muestra que PRMT6 en macrófagos actúa como un amplificador epigenético temprano: aumenta una señal química clave que recluta más células inmunitarias, las cuales a su vez impulsan la formación de hueso donde no corresponde. Dado que bloquear PRMT6 solo durante la fase inflamatoria temprana redujo drásticamente el hueso no deseado mientras dejaba intacta la cicatrización normal del tendón —e incluso mejoró la organización del tejido— esta vía ofrece una estrategia prometedora. En principio, un curso corto y bien cronometrado de terapia dirigida a PRMT6 tras un traumatismo o una cirugía mayor podría prevenir la discapacidad a largo plazo por hueso ectópico, sin comprometer la capacidad natural del cuerpo para repararse.
Cita: Chu, W., Peng, W., Wu, Z. et al. PRMT6 is required for initiating and amplifying macrophage-induced inflammation in heterotopic ossification by increasing CCL2 expression. Bone Res 14, 29 (2026). https://doi.org/10.1038/s41413-026-00512-w
Palabras clave: osificación heterotópica, macrófagos, inflamación, regulación epigenética, señalización CCL2