Clear Sky Science · es
C/EBPβ dicta la transcripción de FSHβ posmenopáusica y el bloqueo de la vía AEP/C/EBPβ alivia la osteoporosis
Por qué esta investigación importa para la vida después de la menopausia
A muchas mujeres se les dice que la caída del estrógeno es la principal causa de la fragilidad ósea tras la menopausia. Este estudio añade una pieza nueva al rompecabezas: otra hormona, la hormona folículoestimulante (FSH), y una pareja proteica en el cerebro y el hueso—C/EBPβ y AEP—trabajan en conjunto para acelerar la pérdida ósea. Más intrigante aún, los investigadores muestran en ratones que bloquear esta vía con una píldora experimental puede proteger los huesos con la misma eficacia que un fármaco para la osteoporosis aprobado.
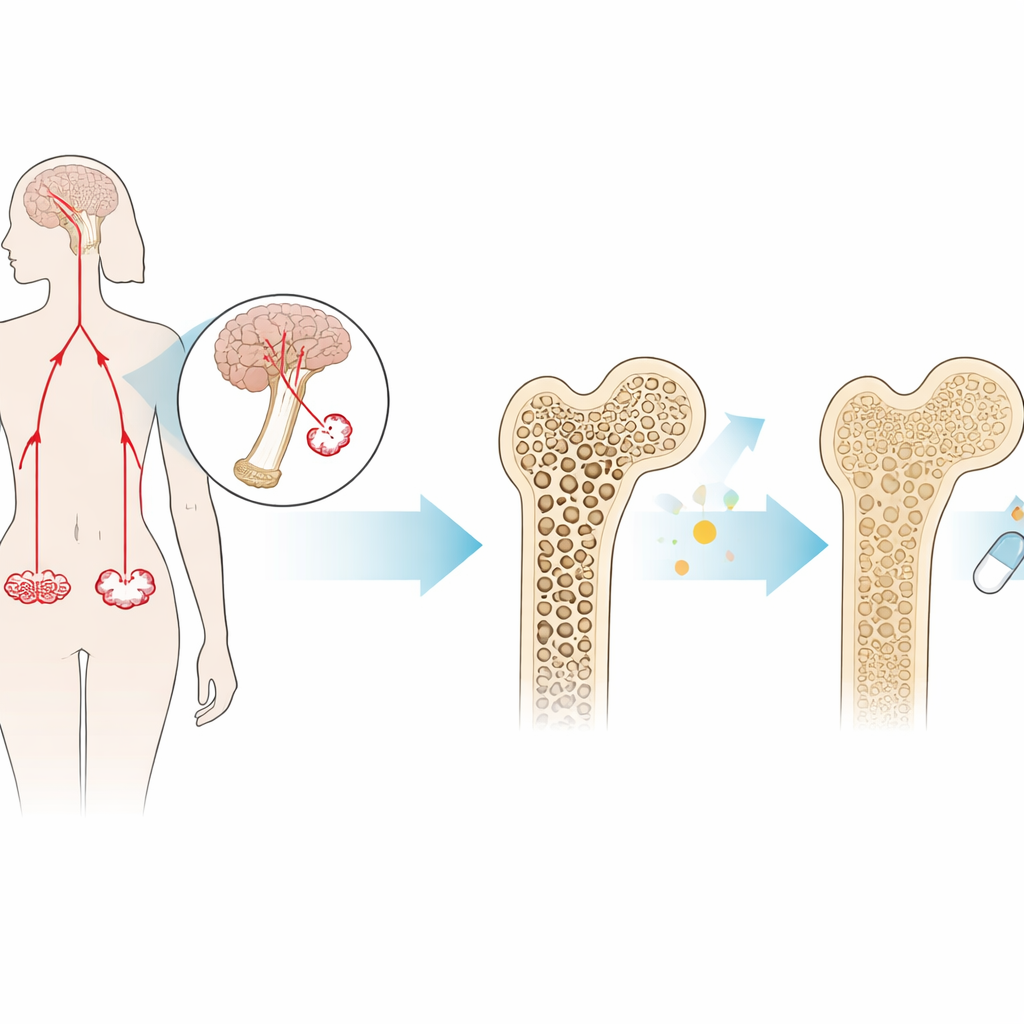
Una hormona poco conocida con gran impacto en el hueso
La FSH se produce en la glándula pituitaria y es más conocida por su papel en la fertilidad. En las mujeres que se acercan a la menopausia, los niveles de FSH aumentan bruscamente varios años antes del último periodo menstrual. Más allá de su papel reproductivo, la FSH puede actuar directamente sobre el hueso: se une a receptores en las células que reabsorben hueso (osteoclastos), estimulándolas a eliminar hueso más rápido de lo que se reconstruye. Estudios anteriores mostraron que los ratones que carecen de FSH o de su receptor están protegidos de la pérdida ósea, incluso cuando sus niveles de estrógeno son bajos. Esto sugirió que la propia FSH, y no solo la deficiencia de estrógeno, puede impulsar la osteoporosis posmenopáusica.
El interruptor de control en la pituitaria
El nuevo estudio se centra en C/EBPβ, una proteína que se une al ADN y activa o desactiva genes. Los autores descubrieron que C/EBPβ se une directamente a la región de control del gen de la subunidad beta de la FSH—la parte de la hormona que define su identidad—y aumenta su producción en la pituitaria. En células pituitarias en cultivo, aumentar C/EBPβ incrementó la FSH, mientras que silenciar C/EBPβ redujo la FSH, especialmente cuando las células eran estimuladas por la señal reproductiva cerebral, GnRH. En ratones ovariectomizados, que imitan la menopausia al eliminar los ovarios productores de estrógeno, los animales con C/EBPβ reducido produjeron mucha menos FSH en sus glándulas pituitarias y en sangre. Estos experimentos revelan a C/EBPβ como un interruptor clave que determina cuánto aumenta la FSH tras la caída del estrógeno.
Un circuito autorreforzante y un nuevo objetivo farmacológico
C/EBPβ también regula otra proteína llamada AEP, una enzima cortadora que puede activar o desactivar otras moléculas. En el cerebro, la cadena C/EBPβ–AEP se ha vinculado a daños similares a los del Alzheimer. Aquí, el equipo preguntó si esta misma cadena retroalimenta la FSH y el hueso. En ratones carentes de AEP, los niveles de C/EBPβ y de FSH cayeron en la pituitaria, y la pérdida ósea tras la extirpación de los ovarios se redujo. Bloquear AEP con una droga de pequeña molécula, denominada #11a, produjo un efecto similar: tras meses de tratamiento, los ratones ovariectomizados mostraron menos FSH, huesos más fuertes en escáneres de alta resolución y menos células reabsorbentes óseas hiperactivas. Otra clase de compuestos—activadores de TrkB que amortiguan indirectamente AEP—ayudaron a las células óseas en cultivos pero no pudieron reducir la FSH en animales, en gran parte porque su receptor objetivo es escaso en la pituitaria. Este contraste reforzó la conclusión de que inhibir AEP directamente es una forma más potente de apagar el eje C/EBPβ–FSH en su fuente.
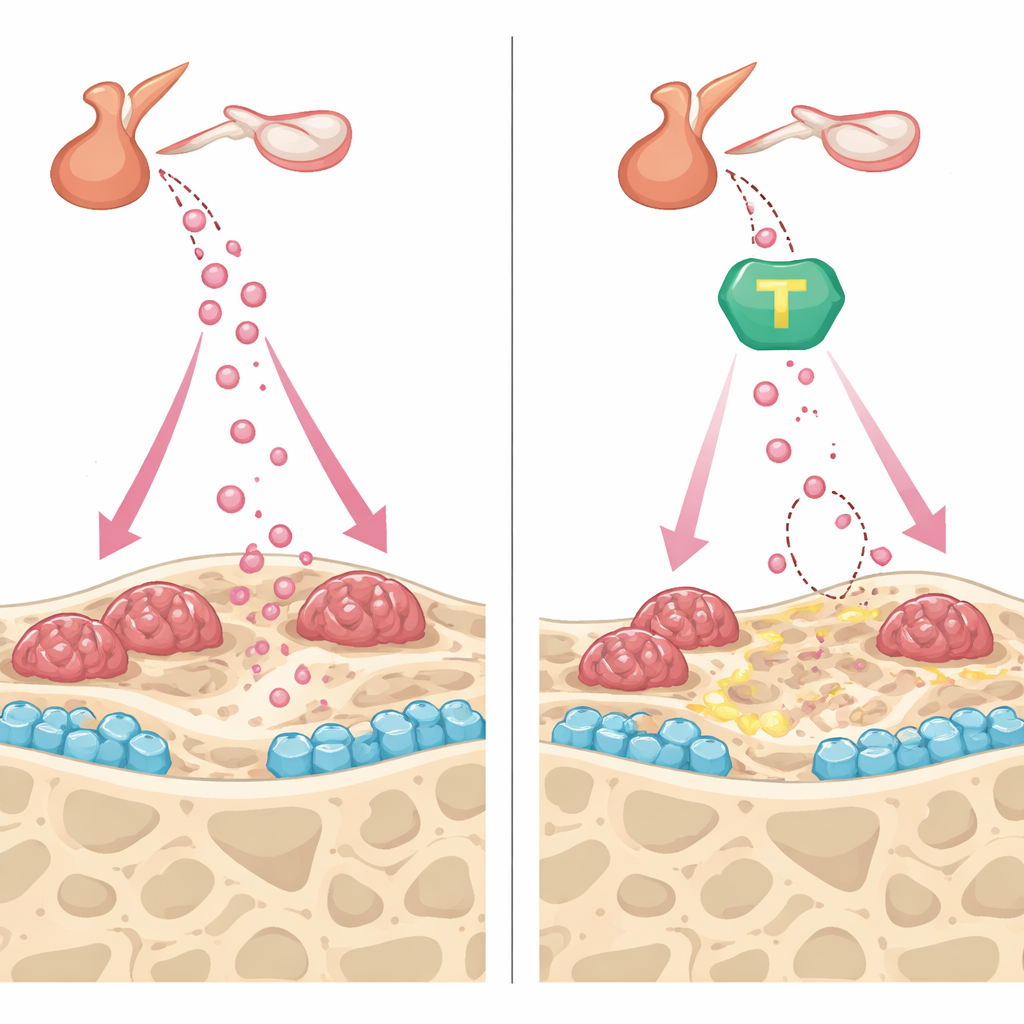
Protegiendo el hueso desde dos frentes
Más allá de bajar la FSH, #11a y el activador de TrkB CF3CN mostraron beneficios complementarios dentro del propio hueso. En cultivos de células formadoras de hueso, ambos compuestos aceleraron la maduración y la deposición mineral, en parte preservando la fibronectina, una proteína estructural que AEP normalmente corta, y potenciando señales pro-óseas como la osteoprotegerina. En las células reabsorbentes de hueso, los fármacos atenuaron los efectos de una señal clave de resorción, reduciendo el número de células grandes y multinucleadas y su capacidad para excavar hoyos en cortes de hueso. En ratones vivos, tanto #11a como CF3CN frenaron la rápida remodelación ósea desencadenada por la extirpación de ovarios, estabilizando la densidad y la microarquitectura ósea. De manera llamativa, cuando #11a se comparó directamente con teriparatida, un inyectable aprobado por la FDA que construye hueso, la píldora experimental igualó la capacidad de la teriparatida para restaurar el volumen y la resistencia ósea en este modelo.
Lo que esto podría significar para la atención futura de la osteoporosis
Para un público no especialista, la conclusión es que este trabajo identifica una vía con doble función que conecta la inflamación relacionada con la menopausia con el aumento de la FSH y el daño óseo, y muestra que dirigirse a AEP puede interrumpir esta cadena. En ratones, un inhibidor oral de AEP no solo reduce el exceso de FSH que alimenta la pérdida ósea, sino que también desplaza directamente el equilibrio dentro del hueso hacia la formación en lugar de la degradación. Aunque estos hallazgos deben probarse aún en personas, sugieren que los tratamientos futuros para la osteoporosis podrían ir más allá de simplemente reemplazar estrógeno o estimular la formación ósea, y en su lugar silenciar este circuito hormonal y enzimático recientemente mapeado que impulsa la fragilidad ósea posmenopáusica.
Cita: Xie, Z., Liao, J., Xiong, J. et al. C/EBPβ dictates postmenopausal FSHβ transcription and blockade of AEP/C/EBPβ pathway alleviates osteoporosis. Bone Res 14, 31 (2026). https://doi.org/10.1038/s41413-026-00510-y
Palabras clave: osteoporosis posmenopáusica, hormona folículoestimulante, vía C/EBPβ AEP, remodelado óseo, terapia dirigida a hormonas