Clear Sky Science · es
La formación de cicatrices fibróticas inducida por TGF-β limita la recuperación tras lesión de la médula espinal
Por qué importan las cicatrices en la médula espinal
Cuando la médula espinal sufre una lesión grave, muchas personas quedan con parálisis permanente o pérdida de sensibilidad porque las fibras nerviosas dañadas no vuelven a crecer. Este estudio plantea una pregunta simple pero crucial: ¿qué es exactamente lo que bloquea ese rebrote —y podemos eliminar esa barrera de forma segura? Al desvelar cómo se forma un tipo particular de cicatriz dentro de la médula lesionada, los autores señalan una nueva vía para ayudar al sistema nervioso a repararse.
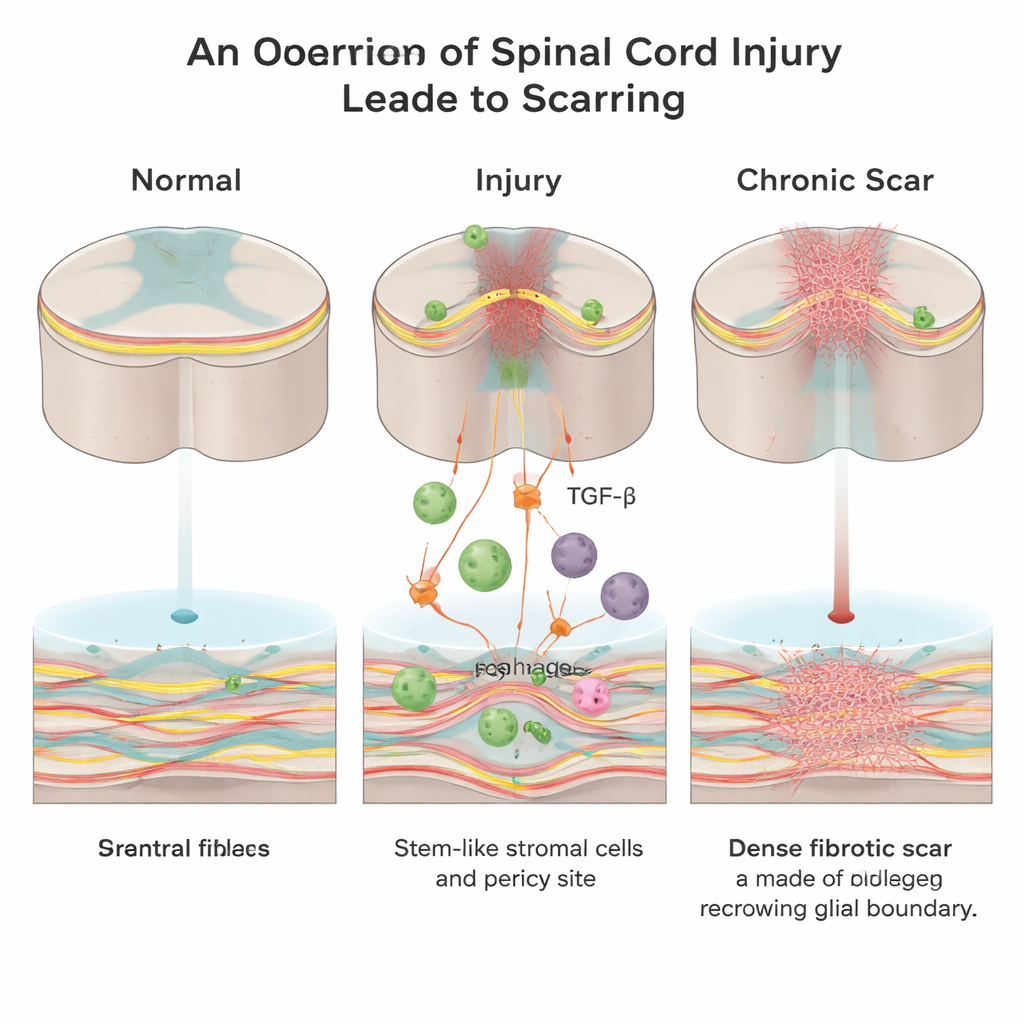
Un muro oculto dentro de la lesión
Tras una lesión medular, el organismo se apresura a sellar la herida. Se forman dos tipos principales de tejido cicatricial: una cicatriz “glial” creada por células de soporte llamadas astrocitos, y una cicatriz “fibrótica” rica en colágeno, fibronectina y células fibroblásticas. Mientras que la cicatriz glial puede tener funciones protectoras, la cicatriz fibrótica crea un muro físico y químico denso que las fibras nerviosas en crecimiento no pueden cruzar fácilmente. Hasta ahora, los científicos sabían mucho menos sobre cómo aparece este núcleo fibrótico y qué señales impulsan su formación.
El papel de las células inmunitarias y una señal poderosa
Trabajando en ratones adultos, los investigadores se centraron en una molécula señalizadora llamada factor de crecimiento transformante beta (TGF‑β), que ayuda a coordinar la reparación de heridas en todo el organismo y suele estar sobreactivada en enfermedades fibróticas. Descubrieron que, tras la lesión medular, las células inmunitarias invasoras conocidas como macrófagos se convierten en una fuente importante de TGF‑β1 activo en el sitio de la lesión. Este aumento de TGF‑β1 recluta células estromales/mesenquimales locales y células asociadas a los vasos llamadas pericitos y las empuja a transformarse en fibroblastos—las mismas células que depositan la cicatriz fibrótica rica en colágeno.
Reducir la señal para abrir un camino
Para comprobar si esta vía causa realmente la formación de una cicatriz dañina, el equipo empleó varios trucos genéticos en ratones. Cuando eliminaron los macrófagos, o suprimieron el gen de TGF‑β1 solo en células de la línea macrófaga, la cantidad de tejido fibrótico en la médula lesionada disminuyó drásticamente y más fibras nerviosas y vías que contienen serotonina pudieron atravesar la zona lesionada. Del mismo modo, eliminar el receptor de TGF‑β específicamente en pericitos redujo su respuesta a TGF‑β, condujo a una menor acumulación de colágeno y mejoró el movimiento y la sensibilidad en pruebas conductuales. Importante: los pericitos y las células relacionadas con carácter similar a células madre seguían existiendo, pero eran menos propensos a convertirse en fibroblastos formadores de cicatriz.
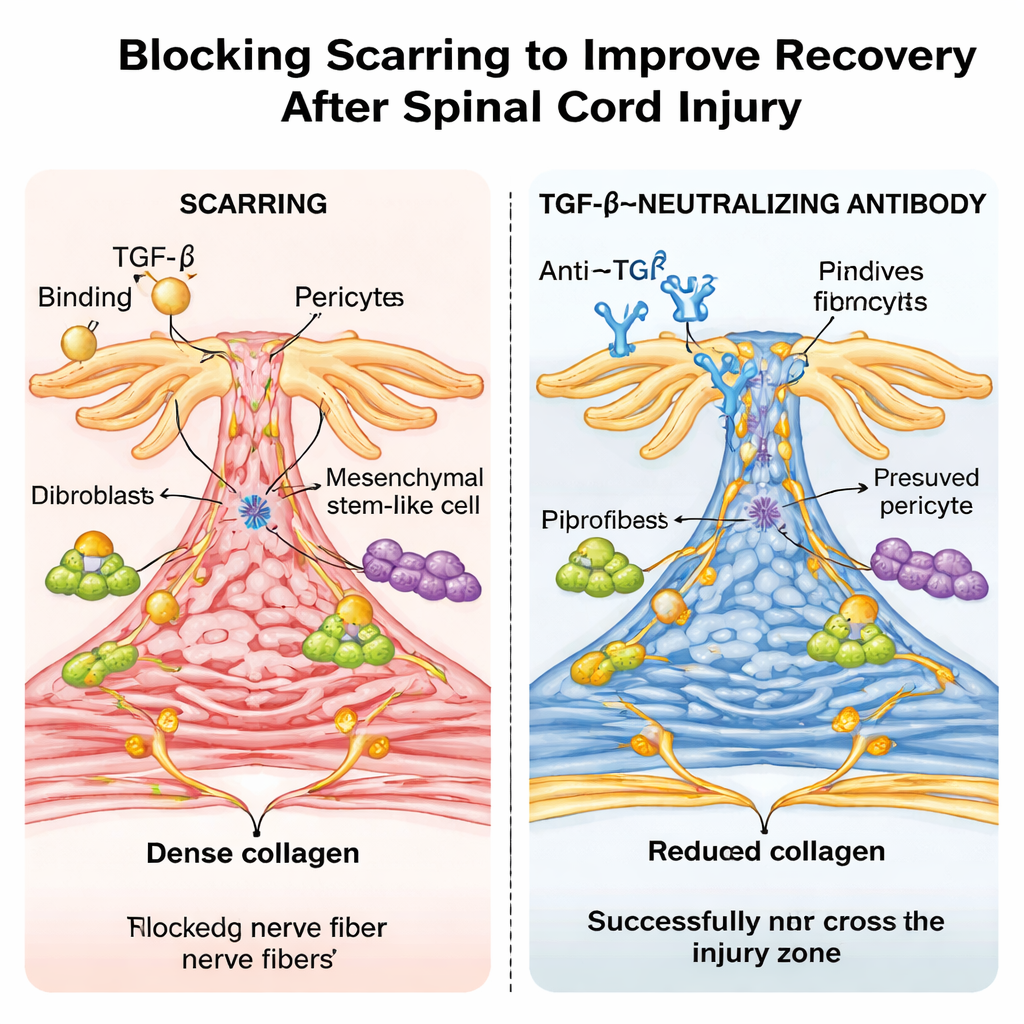
Un anticuerpo tipo fármaco y un sorprendente efecto edad
Los investigadores probaron luego un enfoque más clínicamente relevante: tratar ratones normales con un anticuerpo de laboratorio que neutraliza TGF‑β. Dosis repetidas tras la lesión redujeron los niveles de TGF‑β activo en sangre y médula espinal, encogieron la cicatriz fibrótica y permitieron que las fibras nerviosas puentearan la lesión con mayor eficacia, con ganancias notables en la marcha y la función sensorial. El secuenciamiento de ARN de una sola célula confirmó que los genes sensibles a TGF‑β estaban muy activos en los tipos celulares formadores de cicatriz en ratones no tratados y se vieron atenuados por el anticuerpo. De forma llamativa, cuando se realizó el mismo tipo de aplastamiento medular en ratones recién nacidos, los animales sanaron casi sin cicatrización fibrótica, no mostraron activación detectable de TGF‑β en el lugar de la lesión y recuperaron un movimiento casi normal —semblante de la reparación sin cicatriz observada en algunos animales no mamíferos.
Qué podría significar para tratamientos futuros
En conjunto, los hallazgos sugieren que la activación excesiva de TGF‑β tras la lesión de la médula espinal desvía a células reparadoras útiles hacia la construcción de un muro fibrótico rígido que bloquea el rebrote nervioso y la recuperación funcional. Evitando esta sobreactivación —ya sea dirigiéndose a la producción de TGF‑β en macrófagos, bloqueando su receptor en pericitos y células estromales, o usando un anticuerpo neutralizante— puede ser posible reducir la cicatriz perjudicial preservando o incluso potenciando tipos de respuesta tisular más beneficiosos. Aunque traducir estas estrategias a humanos requerirá estudios cuidadosos para evitar efectos adversos, este trabajo destaca a la cicatrización fibrótica impulsada por TGF‑β como una barrera central y potencialmente tratable para la reparación de la médula espinal.
Cita: Pan, D., Wu, P., Noller, K. et al. TGF-β-induced fibrotic scar formation limits recovery of spinal cord injury. Bone Res 14, 27 (2026). https://doi.org/10.1038/s41413-026-00507-7
Palabras clave: lesión de la médula espinal, cicatriz fibrótica, TGF-beta, macrófagos, regeneración nerviosa