Clear Sky Science · es
HIF-1α y BMAL1 en la regeneración ósea: diálogo entre la respuesta a la hipoxia y el ritmo circadiano
Por qué los huesos rotos se curan mejor de lo que piensas
Cuando nos rompemos un hueso o nos extraen una muela, nuestro cuerpo inicia en silencio un proyecto de reparación notablemente bien orquestado. En lo profundo de la zona lesionada, los niveles de oxígeno caen bruscamente y nuestro reloj interno día‑noche sigue marcando el ritmo. Este artículo explora cómo dos interruptores maestros—HIF‑1α, que detecta el bajo oxígeno, y BMAL1, una proteína central del reloj—trabajan juntos para guiar a las células óseas durante la inflamación, el crecimiento de nuevo tejido y la restauración final de la resistencia. Comprender esta asociación podría mejorar los tratamientos para fracturas, osteoporosis, artritis e incluso implantes dentales.
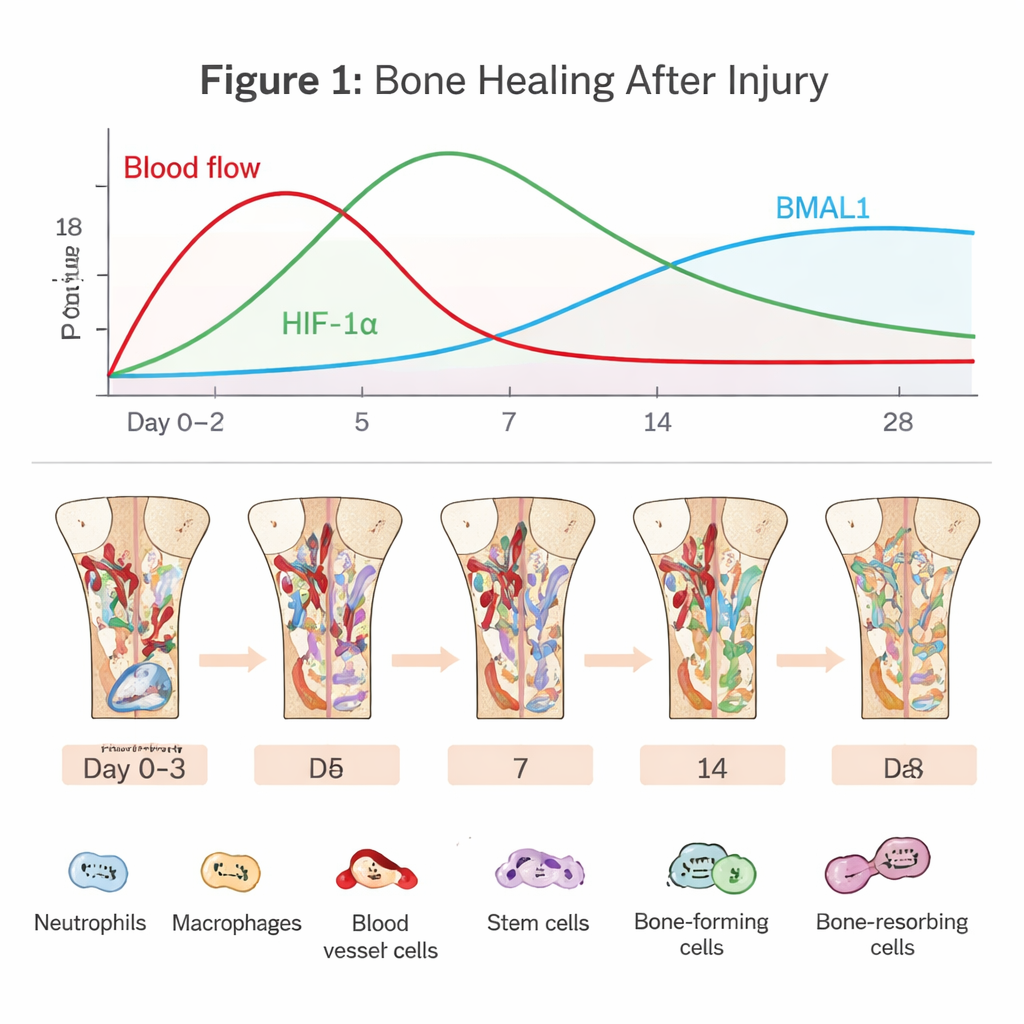
El drama oculto dentro de un hueso en curación
La regeneración ósea comienza en el momento en que se rompen los vasos sanguíneos. Se forma un coágulo que corta gran parte del suministro de oxígeno y crea un nicho hostil y pobre en oxígeno. Células inmunitarias como neutrófilos y macrófagos acuden rápidamente para limpiar los desechos y defender frente a microbios. Al mismo tiempo, se reclutan células madre de la médula ósea y células vasculares para reconstruir la zona. Esta primera “fase inflamatoria” es una espada de doble filo: una ráfaga breve y bien sincronizada de inflamación pone en marcha la reparación, pero si dura demasiado o es demasiado intensa, la curación puede estancarse o fallar. El artículo subraya que recorrer este estrecho camino depende en gran medida de cómo las células perciben el oxígeno y el tiempo.
Cómo las células usan la baja disponibilidad de oxígeno a su favor
En la zona fracturada, pobre en oxígeno, la proteína HIF‑1α se estabiliza y activa genes que ayudan a las células a adaptarse. Impulsa a las células endoteliales a brotar nuevos vasos sanguíneos, asegurando que oxígeno y nutrientes frescos lleguen al defecto. También reprogrma el metabolismo celular hacia la glucólisis, una vía de generación de energía que funciona incluso cuando el oxígeno escasea. Para las células madre y los osteoblastos formadores de hueso, una activación moderada de HIF‑1α puede aumentar la proliferación, la migración y el crecimiento óseo, en parte elevando factores como VEGF que vinculan la formación vascular con el hueso nuevo. Pero si la hipoxia es demasiado severa o prolongada, se acumulan moléculas de estrés y especies reactivas de oxígeno, lo que inclina a los osteoblastos hacia la muerte y estimula a los osteoclastos, que reabsorben hueso. La misma señal hipóxica puede por tanto apoyar o sabotear la curación, según su intensidad y duración.
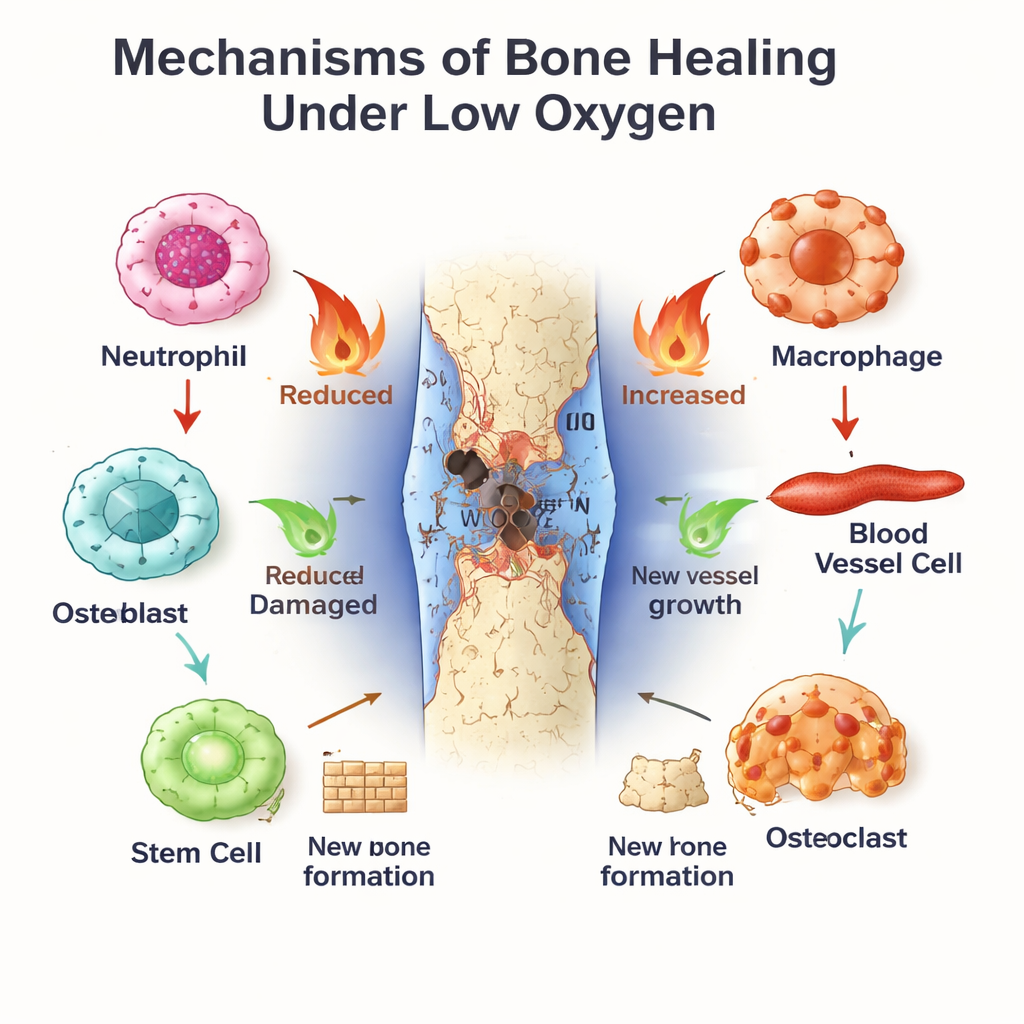
El reloj interno del cuerpo como gestor de la reparación ósea
En paralelo funciona el reloj circadiano, un cronómetro molecular presente en casi todas las células. BMAL1, uno de sus componentes centrales, ayuda a establecer ritmos diarios en la actividad inmunitaria, el comportamiento vascular y la diferenciación de las células madre. Neutrófilos y macrófagos muestran diferencias según la hora del día en la intensidad de su respuesta a la lesión y en la rapidez con que envejecen o pasan de estados inflamatorios (tipo M1) a estados reparadores (tipo M2). En las células vasculares y las células madre de la médula ósea, BMAL1 promueve una proliferación sana y una formación ósea ordenada, en parte afinando vías de crecimiento como Wnt y TGF‑β/SMAD. Cuando BMAL1 se ve alterado—por defectos genéticos, trabajo por turnos o enfermedad metabólica—los huesos tienden a perder masa, las células madre se agotan y el equilibrio entre formación y degradación ósea se desplaza hacia la pérdida.
Una conversación entre la detección de oxígeno y el reloj biológico
El núcleo de la revisión es el emergente “diálogo” entre HIF‑1α y BMAL1. Estas dos proteínas comparten estructuras similares y pueden interactuar físicamente, incluso formando pares mixtos que se unen al ADN y controlan conjuntos de genes superpuestos. Cada una puede influir en la producción y estabilidad de la otra, creando circuitos de retroalimentación que vinculan el ritmo día‑noche con la forma en que las células responden a la hipoxia. Juntas también regulan el balance redox celular—la producción de especies reactivas dañinas frente a la capacidad antioxidante disponible—y co‑regulan enzimas clave que deciden si las células dependen más de la respiración dependiente de oxígeno o de la glucólisis anaerobia. Este control conjunto ayuda a determinar si el entorno de la fractura favorece la reconstrucción constructiva o la inflamación excesiva y la reabsorción ósea.
Qué significa esto para la enfermedad y el tratamiento
La misma asociación HIF‑1α–BMAL1 aparece en muchas condiciones relacionadas con el hueso. En trabajadores por turnos, el sueño alterado y la exposición a la luz probablemente modifican BMAL1, aumentan el estrés oxidativo e interfieren con la reparación guiada por HIF‑1α, contribuyendo a la osteoporosis. En la diabetes, el azúcar sanguíneo elevado debilita tanto la función del reloj como la señalización hipóxica, socavando el crecimiento vascular y la formación ósea dirigida por células madre. En la osteoartritis, la pérdida de BMAL1 en las células del cartílago desordena su ritmo y su relación protectora con HIF‑1α, acelerando la degradación del cartílago. Alrededor de implantes de titanio, la hipoxia controlada y un ritmo circadiano saludable parecen favorecer una mejor oseointegración, lo que sugiere que las futuras recubrimientos de implantes podrían diseñarse para activar suave y conjuntamente HIF‑1α y BMAL1. En conjunto, el artículo concluye que la regeneración ósea exitosa depende no solo de qué células están presentes, sino de cómo interpretan el oxígeno y el tiempo—y que dirigirse a este diálogo podría abrir nuevas vías para una curación más rápida y resistente.
Cita: Weng, Y., Xiong, J., Zhao, Q. et al. HIF-1α and BMAL1 in bone regeneration: crosstalk between hypoxia response and circadian rhythm. Bone Res 14, 25 (2026). https://doi.org/10.1038/s41413-026-00506-8
Palabras clave: regeneración ósea, ritmo circadiano, hipoxia, osteoporosis, curación de fracturas