Clear Sky Science · es
MicroARN-132/212 modula negativamente la recompensa por opioides al dirigirse al transportador de dopamina en el área tegmental ventral
Por qué esta investigación importa en la vida cotidiana
Los analgésicos opioides y fármacos relacionados pueden proporcionar alivio pero también conllevan un riesgo grave de adicción. Este estudio inspecciona el funcionamiento interno del sistema de recompensa del cerebro para identificar pequeños interruptores genéticos que influyen en la intensidad con la que los opioides resultan gratificantes. Al comprender estos interruptores, los científicos esperan diseñar tratamientos más inteligentes que alivien el dolor o reduzcan la dependencia sin secuestrar los circuitos placenteros del cerebro.
Moléculas pequeñas con gran influencia
Nuestros cerebros dependen de una sustancia química llamada dopamina para señalar el placer y motivarnos a buscar experiencias gratificantes, desde comida sabrosa hasta drogas adictivas. La intensidad y la duración de esta señal se controlan en parte por una proteína llamada transportador de dopamina, que actúa como una aspiradora, reabsorbiendo la dopamina hacia las neuronas. Los autores se centraron en dos fragmentos muy pequeños de material genético, microARN-132 y microARN-212, que pueden reducir la producción de proteínas específicas. Trabajos anteriores vincularon estos microARN con el consumo de cocaína y el estrés. Aquí, el equipo preguntó si también influyen en la respuesta cerebral a los opioides, en particular a la morfina.
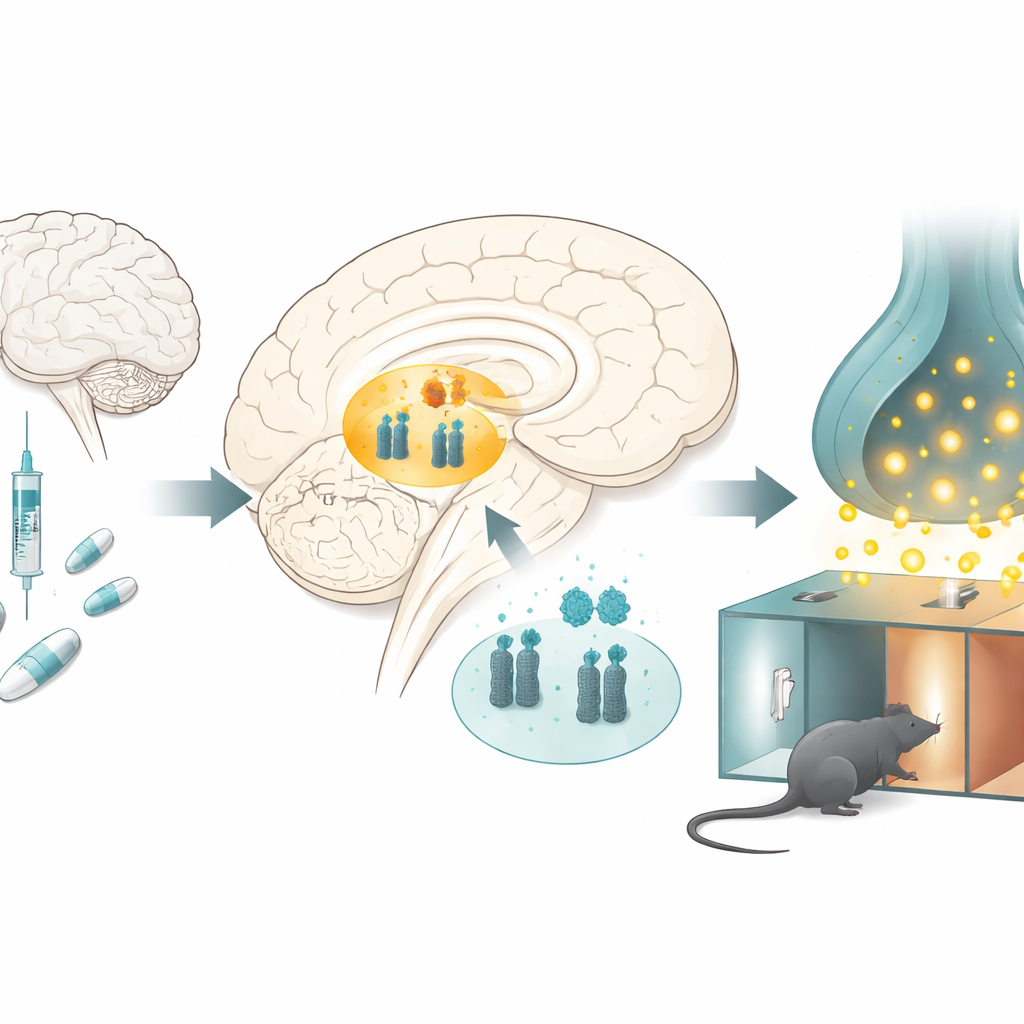
Cómo los opioides cambian el centro de recompensa del cerebro
Los investigadores estudiaron ratas que recibían dosis repetidas de morfina en una prueba clásica de recompensa por drogas, en la que los animales aprenden a preferir una sala asociada con el fármaco. Tras varios días, las ratas tratadas con morfina pasaron más tiempo en la cámara emparejada con la droga, mostrando que el fármaco se había vuelto gratificante. Cuando los científicos examinaron una región clave de recompensa en lo profundo del cerebro llamada área tegmental ventral, hallaron un patrón llamativo: los niveles de microARN-132 y microARN-212 disminuyeron, mientras que los niveles del transportador de dopamina aumentaron. Cambios similares aparecieron cuando las ratas recibieron morfina sin la tarea de aprendizaje de lugar, lo que sugiere que la exposición crónica a la droga por sí sola desplaza este equilibrio molecular.
Señalando un vínculo molecular directo
Para comprobar si estos microARN realmente controlan el transportador de dopamina, el equipo recurrió a células humanas con aspecto nervioso en el laboratorio. Al aumentar artificialmente microARN-132 o microARN-212, observaron una caída tanto en el mensaje genético como en la proteína del transportador. Bloquear los microARN produjo el efecto opuesto. Luego diseñaron un constructo reportero en el que una enzima productora de luz estaba vinculada a la región reguladora del transportador. Añadir los microARN atenuó la señal luminosa, pero este efecto desapareció cuando se mutaron unas pocas bases clave en el sitio de unión. En conjunto, estos experimentos mostraron que microARN-132 y microARN-212 se unen directamente al mensaje del transportador y suprimen su producción.
De las moléculas a los niveles de dopamina y el comportamiento
A continuación, los investigadores preguntaron cómo se manifiesta este control molecular en neuronas vivas. En neuronas cultivadas, aumentar los microARN redujo la captación de dopamina, mientras que bloquearlos potenció la eliminación de dopamina. Cuando aumentaron o disminuyeron artificialmente los niveles del transportador de dopamina, la influencia de los microARN subió o bajó en consecuencia, confirmando que el transportador es el mediador principal. En ratas vivas, elevar microARN-132 en el área tegmental ventral incrementó los niveles de dopamina que se derraman en regiones conectadas, reflejando una actividad del transportador más débil. A nivel conductual, usar herramientas virales para absorber («esponjar») microARN-132 o microARN-212 en esta región cerebral hizo que las ratas aprendieran una preferencia más fuerte por la morfina, junto con niveles más altos del transportador. Por el contrario, forzar la expresión extra de microARN-132 en la misma área redujo los niveles del transportador y atenuó la preferencia por la morfina en animales machos, hembras y adolescentes, sin afectar el movimiento ni el disfrute de recompensas naturales como el agua azucarada.
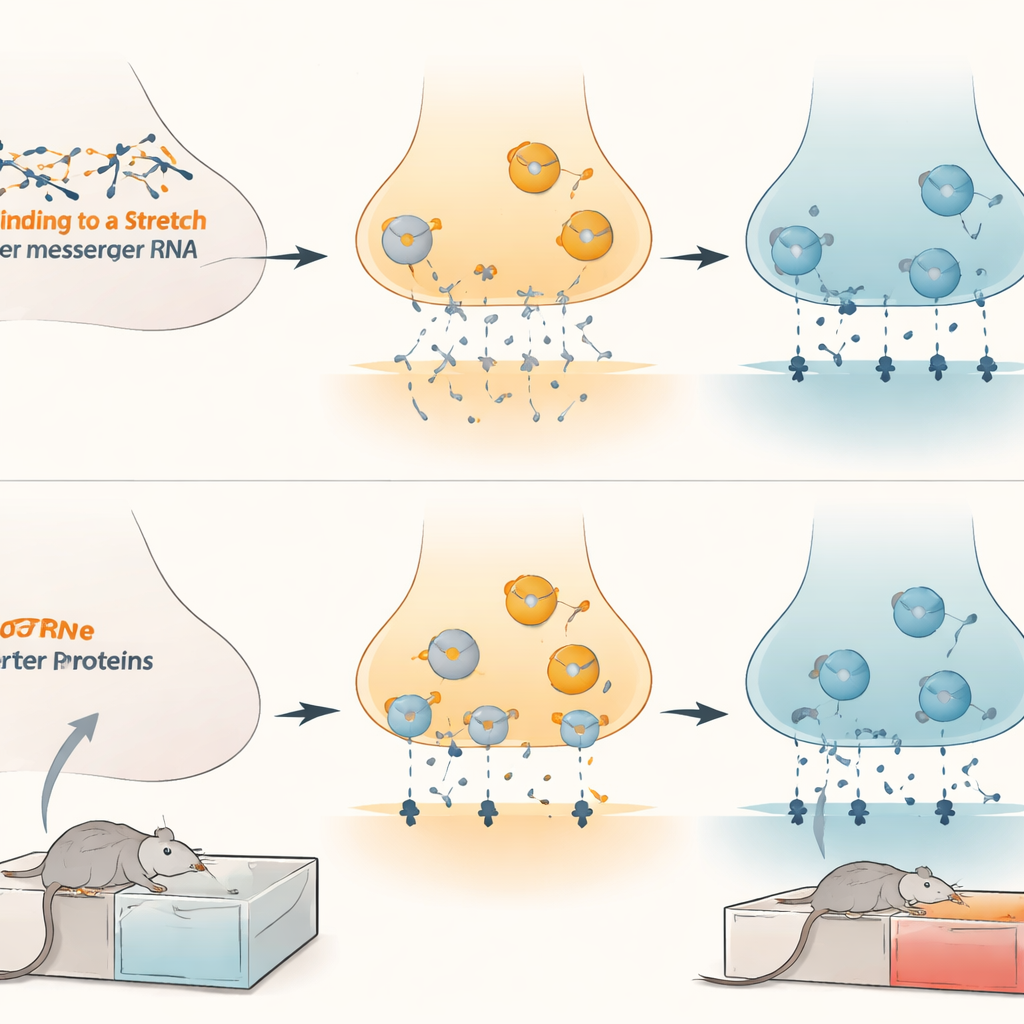
Implicaciones para el tratamiento de la adicción a opioides
Estos hallazgos revelan un sistema de freno finamente ajustado dentro del circuito de recompensa del cerebro: microARN-132 y microARN-212 mantienen controlado al transportador de dopamina, modulando la potencia con que los opioides se experimentan como gratificantes. La morfina crónica parece levantar este freno al reducir los microARN, permitiendo que aumenten los niveles del transportador y contribuyendo a consolidar las señales de recompensa relacionadas con la droga. Restaurar o imitar la acción de estos microARN específicamente en el área tegmental ventral podría suavizar el agarre de la recompensa por opioides sin amortiguar de forma general el placer o el movimiento. Aunque queda mucho trabajo antes de que tales estrategias puedan probarse en personas, este estudio apunta a una vía nueva y muy específica para futuros tratamientos que aborden la adicción a nivel de los propios diales moleculares del cerebro.
Cita: Meng, J., Li, Z., Zhang, Y. et al. MicroRNA-132/212 negatively modulates opioid reward by targeting dopamine transporter in the ventral tegmental area. Transl Psychiatry 16, 152 (2026). https://doi.org/10.1038/s41398-026-03915-9
Palabras clave: adicción a opioides, transportador de dopamina, microARN-132, área tegmental ventral, recompensa por morfina