Clear Sky Science · es
Efectos prenatales y postnatales de la activación inmune gestacional en vías sinápticas y de neurodesarrollo mediante mecanismos epigenéticos
Cómo el sistema inmunitario de la madre moldea el cerebro del niño
Las infecciones durante el embarazo se han vinculado desde hace tiempo con un mayor riesgo de condiciones como la esquizofrenia, el autismo y el TDAH en la descendencia, pero el “puente” biológico entre una madre enferma y un cerebro adulto vulnerable no estaba claro. Este estudio, realizado en ratones, muestra cómo la respuesta inmune materna ante la gripe durante la gestación puede dejar marcas químicas duraderas en el cerebro en desarrollo, alterando la comunicación entre las células cerebrales y aumentando potencialmente el riesgo de problemas neurológicos y de salud mental más adelante.
Enfermedad durante el embarazo y riesgo cerebral a lo largo de la vida
Estudios epidemiológicos en humanos han demostrado que cuando las mujeres embarazadas sufren infecciones, sus hijos tienen mayor probabilidad de desarrollar una serie de trastornos psiquiátricos y del neurodesarrollo en la edad adulta. Los autores se centran en la activación inmune materna, la cascada de señales inmunitarias liberadas cuando el organismo combate una infección. Estas señales pueden atravesar o influir la placenta e interactuar con el cerebro en desarrollo justo cuando se están formando los circuitos. La corteza frontal —crucial para la planificación, la toma de decisiones y el control emocional— se desarrolla durante un largo período y es especialmente sensible a las perturbaciones tempranas.
Disecando los efectos antes y después del nacimiento
Para separar lo que ocurre en el útero de lo que sucede después del nacimiento, los investigadores infectaron a ratonas gestantes con un virus de la influenza leve y no letal durante una etapa temprana de la gestación equivalente al final del primer trimestre en humanos. Algunas crías se quedaron con sus madres biológicas, mientras que otras fueron cruzadas a madres sustitutas en las primeras 24 horas tras el parto. Esto generó cuatro grupos: descendencia sin exposición antes ni después del nacimiento, expuesta solo antes del nacimiento, solo después del nacimiento, o en ambos periodos. Cuando las crías alcanzaron la edad adulta, el equipo examinó neuronas de la corteza frontal, analizando tanto la actividad génica como las marcas “epigenéticas”: etiquetas químicas en las proteínas que empaquetan el ADN que ayudan a controlar qué genes se activan o se silencian. 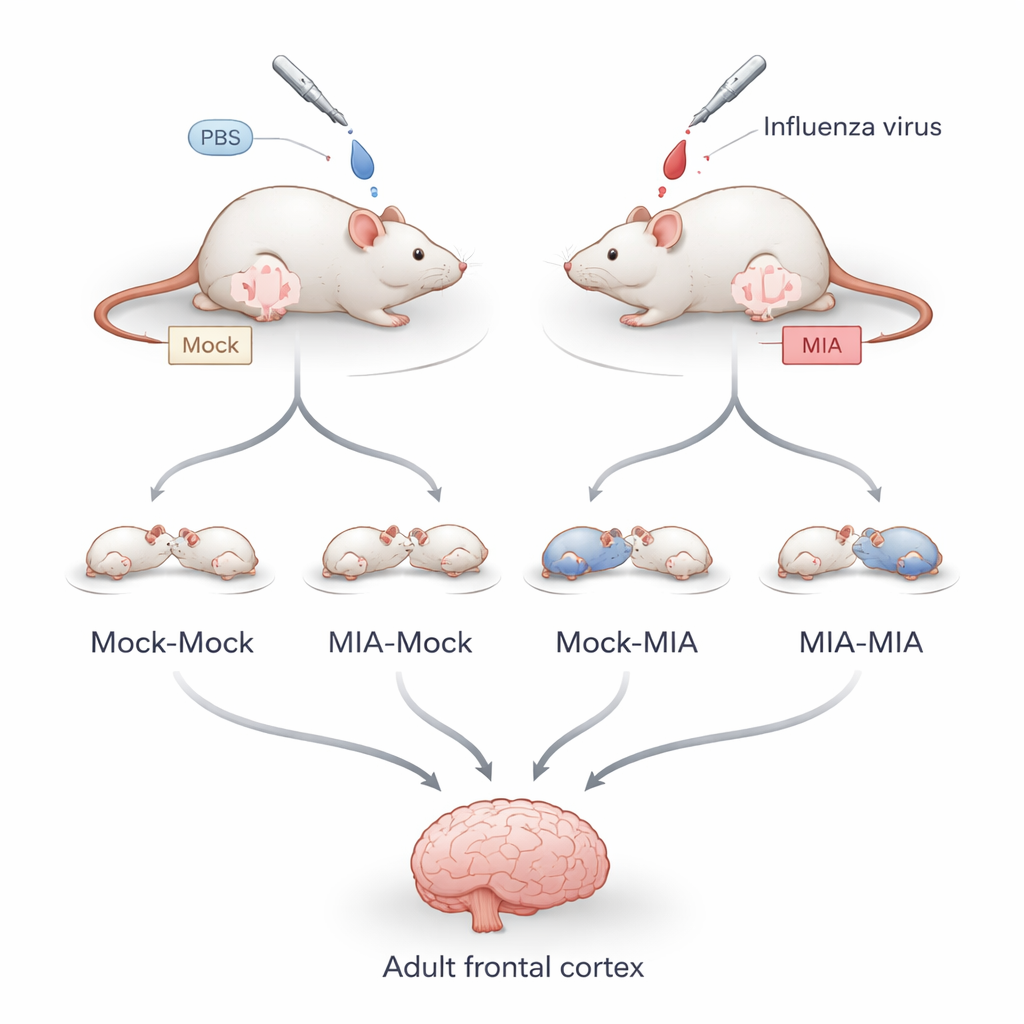
Marcas químicas duraderas en el ADN cerebral
El estudio se centró en dos marcas de histonas, H3K27ac y H3K4me3, que señalan interruptores activos y puntos de inicio de genes. Utilizando métodos de secuenciación sensibles, los autores mapearon decenas de miles de estas regiones regulatorias y midieron qué genes estaban más o menos activos en cada grupo. Encontraron que la activación inmune materna antes del nacimiento produjo cambios extensos y duraderos en las regiones potenciadoras (enhancers): tramos de ADN que actúan como diales de control de la actividad génica. Estos cambios se enriquecieron especialmente en genes implicados en la construcción del prosencéfalo, la orientación del crecimiento axonal y el establecimiento de los primeros puntos de comunicación entre neuronas. Muchos de los mismos genes también mostraron actividad alterada tras el nacimiento cuando las crías fueron criadas por madres con activación inmune, lo que indica una trayectoria regulatoria sostenida a lo largo del desarrollo más que un impacto transitorio.
De los cambios epigenéticos a las alteraciones sinápticas y de circuitos
Tanto la exposición prenatal como la postnatal influyeron en vías moleculares que gobiernan cómo las neuronas se comunican entre sí. Genes relacionados con el glutamato (el principal transmisor excitatorio), el GABA (el principal transmisor inhibitor) y la dopamina (importante para la motivación y la recompensa) mostraron cambios coordinados en sus elementos regulatorios y en sus niveles de expresión. Estos sistemas se implican repetidamente en la esquizofrenia, la depresión, el autismo y la adicción. Los autores hallaron además que genes involucrados en la organización de sinapsis, el crecimiento axonal y la refinación de circuitos cerebrales se vieron afectados, especialmente por la exposición postnatal, lo que sugiere que la conducta materna y los cambios inmunitarios continuos tras el nacimiento contribuyen a moldear cómo se cablean y ajustan las redes neuronales. Los análisis de redes destacaron un conjunto central de factores de transcripción —reguladores maestros de la actividad génica— que se vieron alterados en ambas ventanas temporales.
Vínculos con el riesgo psiquiátrico humano
Para evaluar la relevancia de estos cambios en ratones para la enfermedad humana, el equipo convirtió las ubicaciones de enhancers y promotores del ratón a sus contrapartes humanas más cercanas y las comparó con grandes estudios genéticos de trastornos psiquiátricos. Las regiones alteradas por la activación inmune materna se enriquecieron de forma notable en loci de riesgo humano para esquizofrenia, trastorno bipolar, depresión, neuroticismo y TDAH, pero no en la mayoría de las condiciones no psiquiátricas. Este patrón sugiere que los mismos tipos de regiones regulatorias del ADN que portan riesgo genético heredado para enfermedades mentales también son sensibles a desafíos inmunitarios durante el embarazo y la primera infancia, constituyendo un punto de convergencia entre genes y ambiente.
Qué significa esto para la salud humana
Para un lector no especializado, el mensaje clave es que la respuesta inmune de la madre —no solo la infección en sí— puede dejar “notas en los márgenes” duraderas en el manual de instrucciones del cerebro en desarrollo. Estas notas epigenéticas, escritas antes y poco después del nacimiento, pueden alterar sutilmente cómo las células cerebrales crecen y se comunican en circuitos que controlan el pensamiento, el estado de ánimo y el comportamiento. Aunque la mayoría de los hijos de madres enfermas no desarrollarán trastornos psiquiátricos, este trabajo ayuda a explicar por qué algunos pueden ser más vulnerables y subraya la importancia de prevenir y manejar infecciones e inflamación durante el embarazo y la primera infancia como parte de la salud cerebral a largo plazo.
Cita: Zhu, B., Li, G., Saunders, J.M. et al. Prenatal and postnatal effects of gestational immune activation on synaptic and neurodevelopmental pathways via epigenetic mechanisms. Transl Psychiatry 16, 82 (2026). https://doi.org/10.1038/s41398-026-03884-z
Palabras clave: activación inmune materna, epigenética, neurodesarrollo, señalización sináptica, riesgo psiquiátrico