Clear Sky Science · es
Neuroimagen funcional de la inhibición de la hidrolasa de amidas de ácidos grasos en el trastorno de estrés postraumático: un ensayo clínico aleatorizado
Por qué la química cerebral importa para la recuperación del trauma
Muchas personas que viven un trauma desarrollan trastorno de estrés postraumático (TEPT), una condición caracterizada por pesadillas, recuerdos intrusivos y una tensión constante. Los tratamientos con mayor respaldo son formas de psicoterapia que exponen con cuidado a las personas a los recuerdos traumáticos en un entorno seguro, ayudando al cerebro a aprender que el peligro pasado ya no está presente. Los científicos han esperado que añadir un medicamento que potencie las propias sustancias calmantes del cerebro, similares al cannabis, pudiera facilitar ese aprendizaje y hacer la terapia más eficaz. Este estudio puso esa idea a prueba rigurosa y además examinó el interior del cerebro para ver qué ocurría realmente.
Una idea prometedora del sistema cerebral similar al cannabis
El cuerpo produce sus propias sustancias parecidas al cannabis, llamadas endocannabinoides, que ayudan a regular el estrés, el miedo y el aprendizaje emocional. Una de ellas, la anandamida, parece especialmente importante para la “extinción del miedo”: el proceso de aprender que una señal que antes era amenazante ahora es segura. En animales y en voluntarios sanos, elevar los niveles de anandamida mejora ese aprendizaje de seguridad y atenúa las respuestas al estrés. Una enzima clave, la hidrolasa de amidas de ácidos grasos (FAAH), descompone la anandamida. Bloquear la FAAH con un fármaco eleva la anandamida en el organismo y, según la hipótesis de los investigadores, en las regiones cerebrales que controlan el miedo y las emociones.
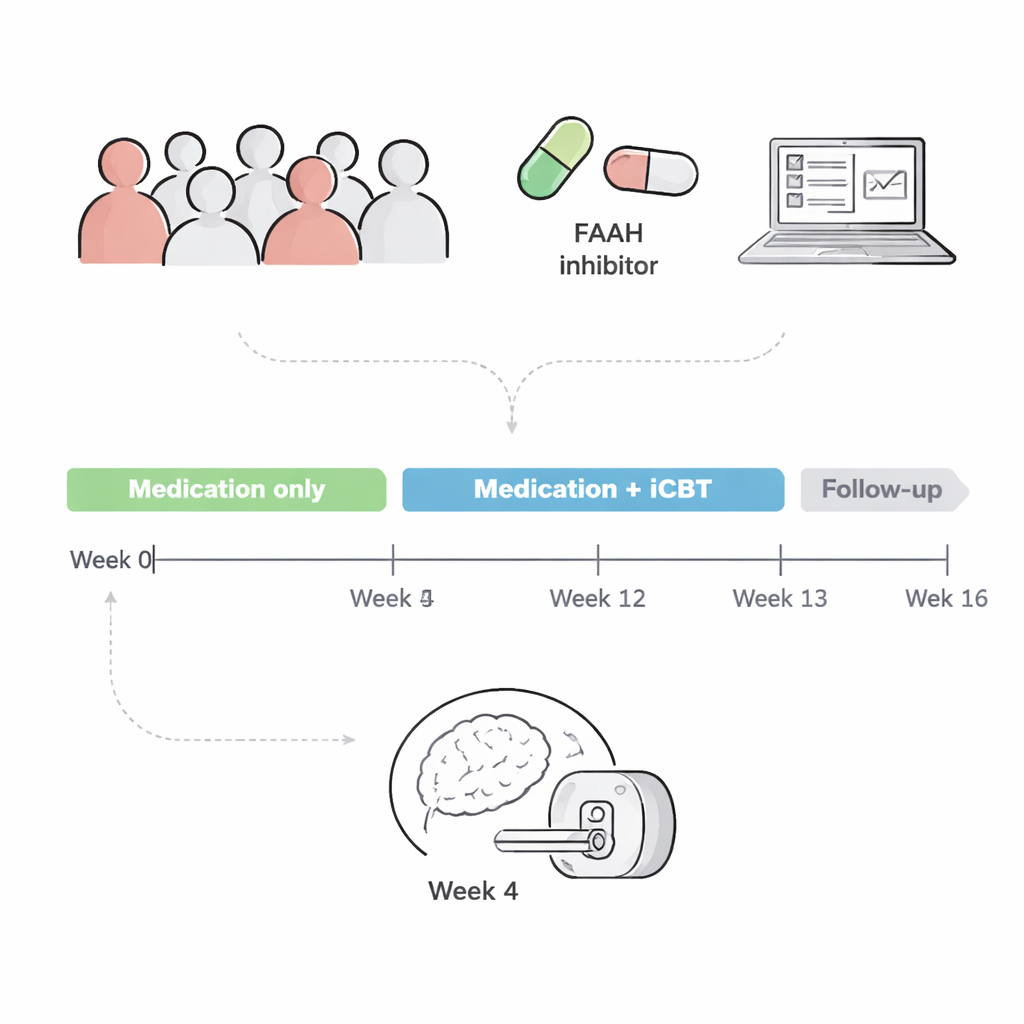
Con base en esto, el equipo realizó un ensayo clínico aleatorizado doble ciego en 100 adultos con TEPT. Durante 12 semanas, los participantes tomaron o bien un fármaco que bloquea la FAAH o un placebo, y tras 4 semanas todos comenzaron un programa de terapia cognitivo-conductual por internet (iCBT) centrado en el trauma. Informes anteriores de este ensayo mostraron que, contrariamente a lo esperado, el inhibidor de FAAH no redujo los síntomas del TEPT más que el placebo a lo largo del tratamiento. El presente artículo indaga en las exploraciones cerebrales para preguntar: ¿al menos cambió el fármaco la actividad cerebral o la comunicación entre áreas clave emocionales, aun cuando los síntomas no mejoraron?
Mirando cerebros en reposo y en tareas emocionales
Setenta y seis participantes se sometieron a resonancia magnética funcional tras 4 semanas con el fármaco o el placebo, justo antes de iniciar la terapia. Los investigadores recopilaron dos tipos de datos cerebrales. Primero, una exploración en “estado de reposo” midió con qué intensidad distintas regiones cerebrales aumentaban y disminuían su actividad de forma conjunta, señal de que están conectadas funcionalmente. Segundo, durante una tarea de “conflicto emocional”, los participantes vieron caras y palabras emocionales que a veces coincidían y otras veces chocaban, una especie de versión emocional de la prueba Stroop. Esta tarea se ha vinculado anteriormente con la respuesta a la terapia del TEPT.
El equipo se centró en una red largamente implicada en el TEPT: la amígdala, que detecta amenazas y la importancia emocional; la corteza prefrontal ventromedial (vmPFC), implicada en el aprendizaje de seguridad y la regulación emocional; y la corteza prefrontal dorsolateral (dlPFC), relacionada con el control esforzado y el afrontamiento. También examinaron una zona llamada ínsula anterior, que ayuda a integrar las sensaciones corporales con los estados emocionales. Al relacionar las medidas cerebrales con los síntomas del TEPT evaluados por clínicos y autoinformados, los investigadores buscaron patrones que pudieran distinguir a las personas que mejoraron más durante el ensayo.
Qué cambió en el cerebro —y qué no
El fármaco bloqueador de la FAAH cumplió claramente su función bioquímica: los niveles sanguíneos de anandamida fueron más altos en las personas que lo recibieron. Sin embargo, al comparar los grupos de fármaco y placebo, no hallaron diferencias significativas en la conectividad en reposo ni en la activación cerebral relacionada con la tarea. El esperado impulso en los circuitos vinculados al miedo y a la emoción simplemente no apareció en las exploraciones. En su lugar, surgieron otros patrones ligados a la gravedad de los síntomas y al grado de mejoría a lo largo del tiempo, independientemente de la píldora que tomaran.
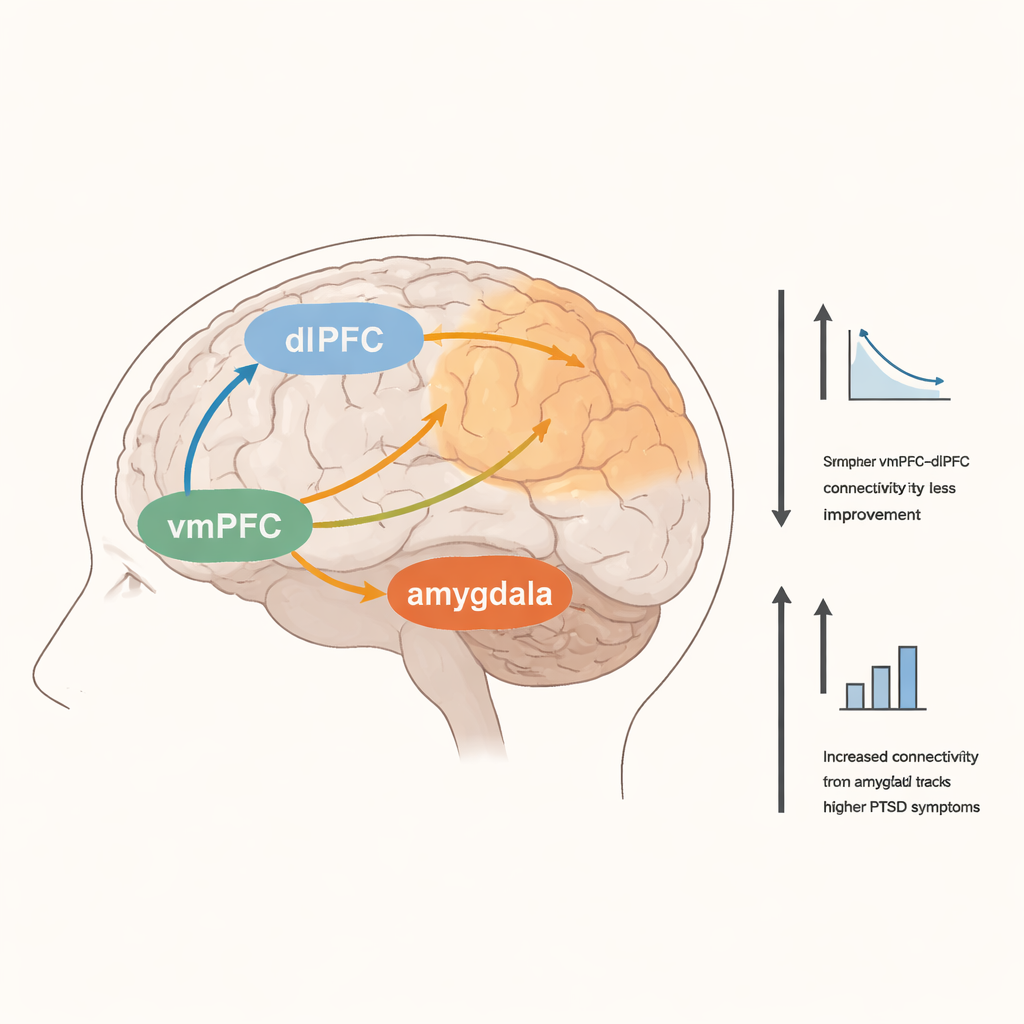
Las personas que informaron síntomas más graves de TEPT en el momento del escaneo mostraron conexiones funcionales más fuertes entre la vmPFC y amplias regiones cerebrales relacionadas con la atención, y entre la amígdala y áreas implicadas en la percepción y el movimiento del cuerpo. Enlaces más fuertes entre la vmPFC y la ínsula anterior también se asociaron con síntomas autoinformados más altos. De forma interesante, una mayor mejoría clínica a lo largo del ensayo de 12 semanas se relacionó con una activación menor en la dlPFC derecha durante la tarea de conflicto emocional, y con una conectividad en reposo más débil entre la vmPFC y esa misma región de la dlPFC. Esto sugiere que los pacientes que finalmente mejoraron podrían haber dependido menos del control esforzado y de alto nivel y más de otras formas, quizás más automáticas, de procesamiento emocional.
Qué significa esto para futuros tratamientos del TEPT
La conclusión central en términos cotidianos es que simplemente aumentar una de las sustancias cerebrales parecidas al cannabis, la anandamida, no fue suficiente para potenciar la terapia ni para remodelar los circuitos clave de miedo y emoción en personas con TEPT, al menos en esta muestra mayoritariamente femenina y no combatiente. No obstante, el estudio destaca a la dlPFC como un posible marcador de quién tiene más probabilidades de beneficiarse de la terapia basada en la exposición, y subraya que el TEPT implica cambios amplios en la forma en que las redes de emoción y atención se comunican entre sí. Para pacientes y clínicos, estos resultados recuerdan que ideas prometedoras procedentes de estudios en animales y en fases tempranas en humanos no siempre se traducen directamente en tratamientos efectivos, y que comprender la compleja respuesta del cerebro al trauma requerirá mirar más allá de un solo químico y hacia patrones cerebrales completos y diferencias individuales.
Cita: Tansey, R., Perini, I., Petrie, G.N. et al. Functional neuroimaging of fatty acid amide hydrolase inhibition in posttraumatic stress disorder: a randomized clinical trial. Transl Psychiatry 16, 95 (2026). https://doi.org/10.1038/s41398-026-03864-3
Palabras clave: TEPT, endocannabinoide, inhibidor de FAAH, fMRI funcional, extinción del miedo