Clear Sky Science · es
La modificación m6A mediada por METTL3 regula CDKN1A para atenuar el deterioro cognitivo y la apoptosis neuronal inducidos por privación crónica de sueño en ratas
Por qué las noches sin dormir pueden dañar tu memoria
Mucha gente minimiza la pérdida crónica de sueño como parte normal de la vida moderna, pero la ciencia está mostrando que la falta de sueño puede dañar silenciosamente las zonas cerebrales que sostienen el aprendizaje y la memoria. Este estudio en ratas examina hasta el nivel de moléculas individuales dentro de las neuronas del hipocampo e identifica un interruptor químico específico—llamado METTL3—que parece proteger a las células cerebrales de los efectos nocivos de la privación crónica de sueño. Entender este interruptor podría apuntar, eventualmente, a nuevas maneras de preservar la memoria en personas que no pueden evitar la pérdida de sueño, como trabajadores por turnos, cuidadores y pacientes con trastornos del sueño.
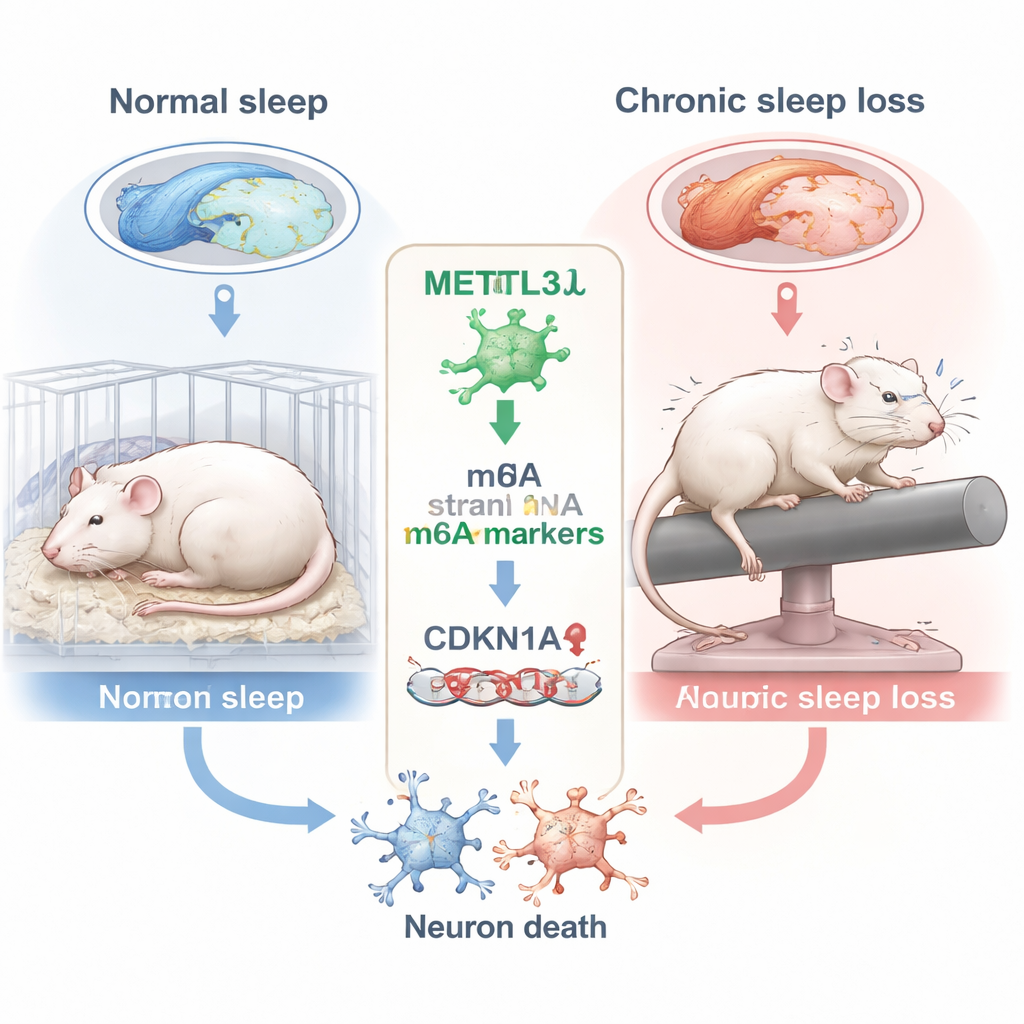
Cómo el déficit prolongado de sueño daña el centro de la memoria
Los investigadores se centraron en el hipocampo, una región cerebral con forma de caballito de mar esencial para formar recuerdos nuevos. Dentro del hipocampo se enfocaron en una subregión llamada CA3, que ayuda a codificar y recuperar información espacial—habilidades que se evalúan con tareas como encontrar una plataforma oculta en el agua. Las ratas se mantuvieron despiertas 10 horas al día durante seis semanas mediante un rodillo giratorio suave que las despertaba repetidamente. Cuando se evaluó su memoria en el conocido laberinto acuático de Morris, las ratas privadas de sueño trazaron rutas menos directas, cruzaron menos veces la ubicación previa de la plataforma y pasaron menos tiempo en el cuadrante objetivo, todos signos de un deterioro de la memoria espacial en comparación con animales bien descansados.
Una marca química en el ARN que desaparece
Para comprender qué ocurría dentro de las neuronas CA3, el equipo analizó una etiqueta química en el ARN llamada m6A, una de las marcas internas más comunes del ARN mensajero. Estas marcas ayudan a controlar cuánto duran las moléculas de ARN y cuán eficientemente se usan para fabricar proteínas. Una enzima clave que añade marcas m6A es METTL3. Usando secuenciación m6A de alto rendimiento y análisis de expresión génica, los científicos hallaron que la privación crónica de sueño redujo significativamente METTL3 en la región CA3. Esta caída se confirmó tanto a nivel de ARN como de proteína. El patrón de genes afectados sugirió alteraciones en el control del ciclo celular y las respuestas al estrés, insinuando que la pérdida de sueño podría estar empujando a las neuronas hacia estados perjudiciales.
Del cambio molecular a la muerte neuronal
Para ver cómo una menor cantidad de METTL3 podría afectar directamente a las neuronas, los investigadores recurrieron a células del hipocampo de ratón cultivadas en placa. Cuando utilizaron ARN interferente pequeño para silenciar METTL3, las células se volvieron mucho más vulnerables a un tratamiento dañino con rapamicina, un fármaco que estresa a las neuronas. Estas células con METTL3 reducido mostraron niveles más altos de proteínas clásicas de “suicidio celular” como Bax y caspasa-3 clivada, y un mayor número de células fue marcado como apoptótico mediante citometría de flujo. Análisis de ARN más profundos apuntaron a un único gen, CDKN1A (que codifica la proteína p21), como un actor clave: cuando METTL3 se redujo, los niveles de CDKN1A aumentaron notablemente.
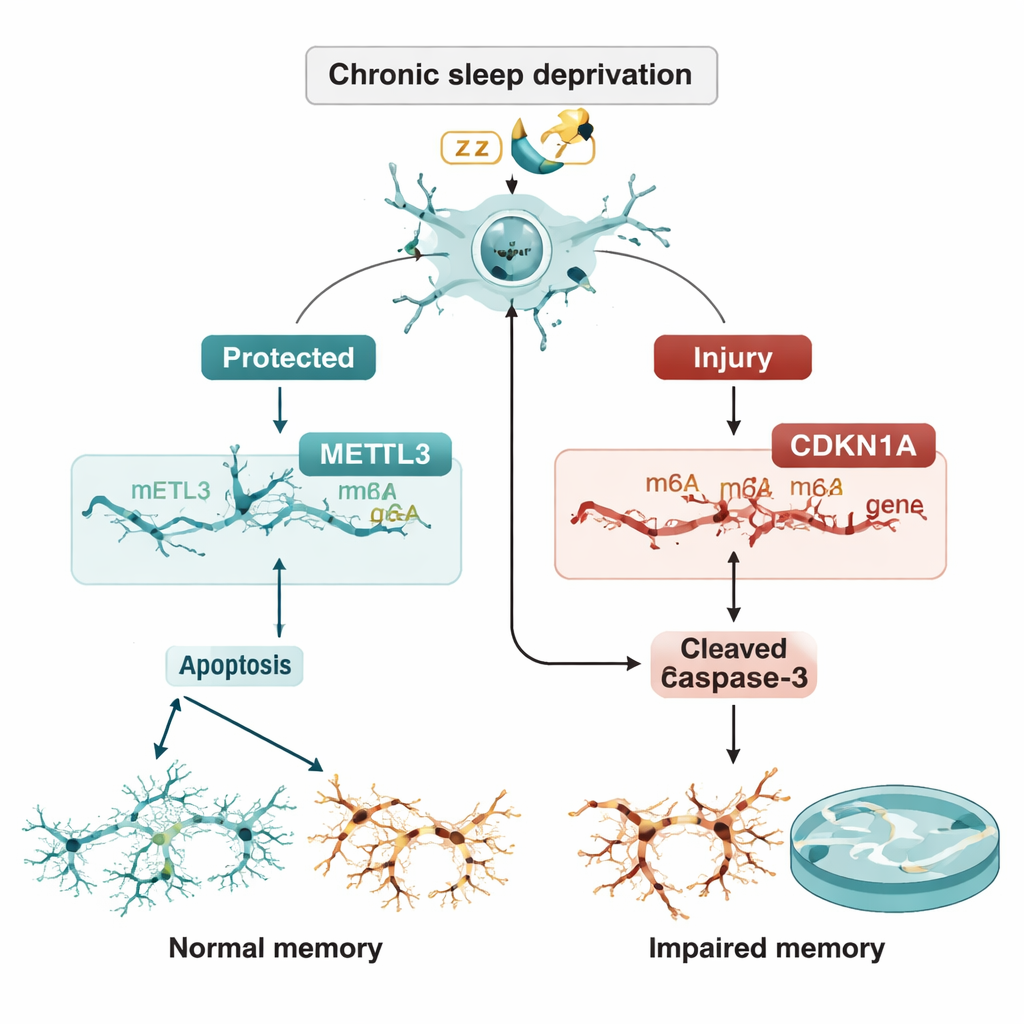
Un equilibrio frágil entre protección y autodestrucción
El equipo preguntó entonces si METTL3 controla CDKN1A a través del marcado m6A. Mostraron que reducir METTL3 disminuía las marcas m6A en el ARN de CDKN1A y hacía ese ARN más estable, de modo que sus niveles se acumulaban en lugar de degradarse. El aumento de CDKN1A, a su vez, impulsó a las neuronas hacia la apoptosis. De manera crucial, cuando CDKN1A se redujo, la muerte celular adicional provocada por la pérdida de METTL3 se revirtió en gran medida. En ratas vivas, la entrega de METTL3 extra directamente en la región CA3 mediante un vector viral redujo los niveles de CDKN1A, disminuyó la abundancia de proteínas apoptóticas, preservó la estructura neuronal en tinciones de tejido y mejoró el rendimiento en el laberinto acuático a pesar de la continua privación de sueño.
Qué significa esto para las personas que no pueden dormir lo suficiente
En pocas palabras, la privación crónica de sueño parece disminuir una enzima protectora, METTL3, en un circuito cerebral crítico para la memoria. Cuando METTL3 baja, deja de etiquetar adecuadamente ciertos ARNs, especialmente el que codifica CDKN1A. Ese ARN se acumula, empujando a las neuronas hacia la muerte programada y contribuyendo a los problemas de memoria. Restaurando METTL3, los investigadores pudieron reducir CDKN1A, limitar la pérdida neuronal y rescatar la memoria en ratas privadas de sueño. Aunque este trabajo aún está en etapa animal, identifica la vía METTL3–CDKN1A como un objetivo prometedor para futuros fármacos destinados a proteger el cerebro del impacto cognitivo de la pérdida crónica de sueño.
Cita: Xing, F., Shi, XS., Gu, HW. et al. METTL3-mediated m6A modification regulates CDKN1A to attenuate chronic sleep deprivation-induced cognitive impairment and neuronal apoptosis in rats. Transl Psychiatry 16, 96 (2026). https://doi.org/10.1038/s41398-026-03855-4
Palabras clave: privación crónica de sueño, hipocampo, metilación del ARN, apoptosis neuronal, deterioro de la memoria