Clear Sky Science · es
La disfunción de las interneuronas GABAérgicas subyace a las oscilaciones cerebrales alteradas asociadas con actividad epileptiforme en ratones deficientes en PPT1
Cuando los ritmos cerebrales fallan
Las convulsiones no son solo tormentas repentinas de actividad cerebral; a menudo emergen de cambios sutiles en cómo se comunican las neuronas. Este estudio examina un trastorno cerebral infantil raro, la enfermedad CLN1, y plantea una pregunta sencilla con implicaciones amplias: ¿qué ocurre con los “guardianes del ritmo” del cerebro cuando falta una sola enzima, llamada PPT1? Al seguir estos cambios en ratones a lo largo del tiempo, los investigadores revelan cómo pequeñas fallas tempranas en la inhibición pueden convertirse en convulsiones y en un daño cerebral generalizado.
Los guardianes del equilibrio cerebral
Nuestros cerebros dependen de dos tipos generales de neuronas. Las neuronas excitadoras, como las piramidales del hipocampo, impulsan la actividad. Las neuronas inhibitorias, llamadas interneuronas, actúan como frenos, manteniendo el control de esa actividad y dando forma a los ritmos eléctricos cerebrales. Entre ellas, dos grupos importantes son las interneuronas positivas para parvalbúmina (PV+) y las positivas para somatostatina (SST+). Estas células contribuyen a generar y coordinar ondas rítmicas cerebrales, como las oscilaciones theta y gamma, que sostienen funciones como el aprendizaje y la memoria. En la enfermedad CLN1, los niños pierden la enzima PPT1, que normalmente elimina grupos grasos de las proteínas. Los autores usaron un modelo de ratón con la misma mutación encontrada en pacientes para ver cómo esta pérdida afecta a las interneuronas y a los ritmos cerebrales que ayudan a controlar.
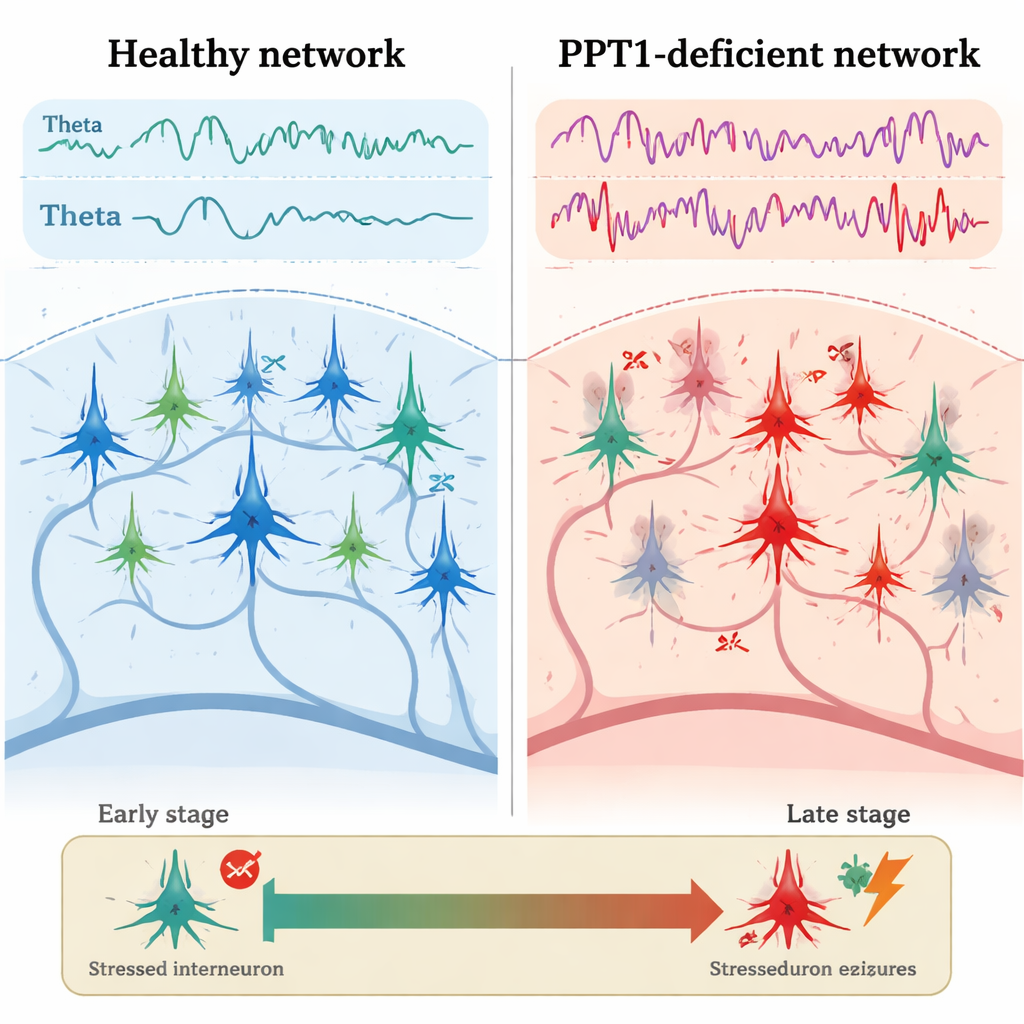
Fisuras tempranas en el sistema inhibitorio
En ratones jóvenes adultos mutantes, de aproximadamente tres a cuatro meses, apareció el primer problema claro en las interneuronas PV+. Registros eléctricos del hipocampo mostraron que estas células inhibitorias disparaban con menos frecuencia que en ratones sanos, mientras que las neuronas piramidales cercanas disparaban más rápido y con pausas más cortas entre picos. La microscopía reveló que muchas interneuronas PV+ tenían caspasa-3 activada, un ejecutor clave de la muerte celular programada, aunque sus números totales aún no habían disminuido. Al mismo tiempo, la potencia de las ondas theta y gamma aumentó, y la imagen de calcio mostró una actividad más intensa en neuronas hipocámpicas mientras los animales se movían. De forma crucial, el “diálogo” normal entre las ritmos theta y gamma —donde las ondas más lentas ayudan a organizar las más rápidas— se debilitó, lo que sugiere un fallo temprano en la temporización fina de la actividad en red.
De ritmos alterados a estallidos epilépticos
A los seis o siete meses de edad, el panorama había empeorado. Muchas interneuronas PV+ se habían perdido, y ahora las interneuronas SST+ también mostraban señales de activación de caspasa-3. Los registros del hipocampo revelaron descargas epileptiformes espontáneas: breves estallidos anormales de actividad asociados con convulsiones. El equipo se centró en los “ripples” de alta frecuencia, oscilaciones rápidas que normalmente ayudan a consolidar recuerdos. En los ratones mutantes, los ripples fisiológicos (alrededor de 140–200 hertz) se volvieron menos frecuentes pero de mayor amplitud, mientras que ripples aún más rápidos “patológicos” (200–500 hertz), estrechamente ligados a la epilepsia, se hicieron más fuertes y comunes. En conjunto, estos cambios sugieren un desplazamiento desde ritmos organizados relacionados con la memoria hacia patrones caóticos y propensos a convulsiones a medida que falla el control inhibitor.
Las neuronas se deterioran y el diazepam interviene
A medida que la enfermedad avanzó, el propio hipocampo empezó a degenerarse. Las señales de calcio en las neuronas disminuyeron, la tinción de Golgi mostró árboles dendríticos más delgados y menos ramificados, y hubo menos espinas diminutas donde se forman las sinapsis. Los recuentos de neuronas en regiones clave del hipocampo (CA1 y CA3) confirmaron una pérdida celular generalizada, y en los registros eléctricos se detectaron menos unidades activas. Los investigadores probaron entonces diazepam, un fármaco antiepiléptico común que potencia la acción del neurotransmisor inhibidor GABA. En ratones mutantes más viejos, el diazepam redujo la frecuencia de las descargas epilépticas y restauró parcialmente patrones oscilatorios más normales, incluido el comportamiento de los ripples, aunque no reparó la pérdida subyacente de receptores. Esto sugiere que reforzar las señales inhibitorias restantes puede calmar la red, al menos de forma temporal.
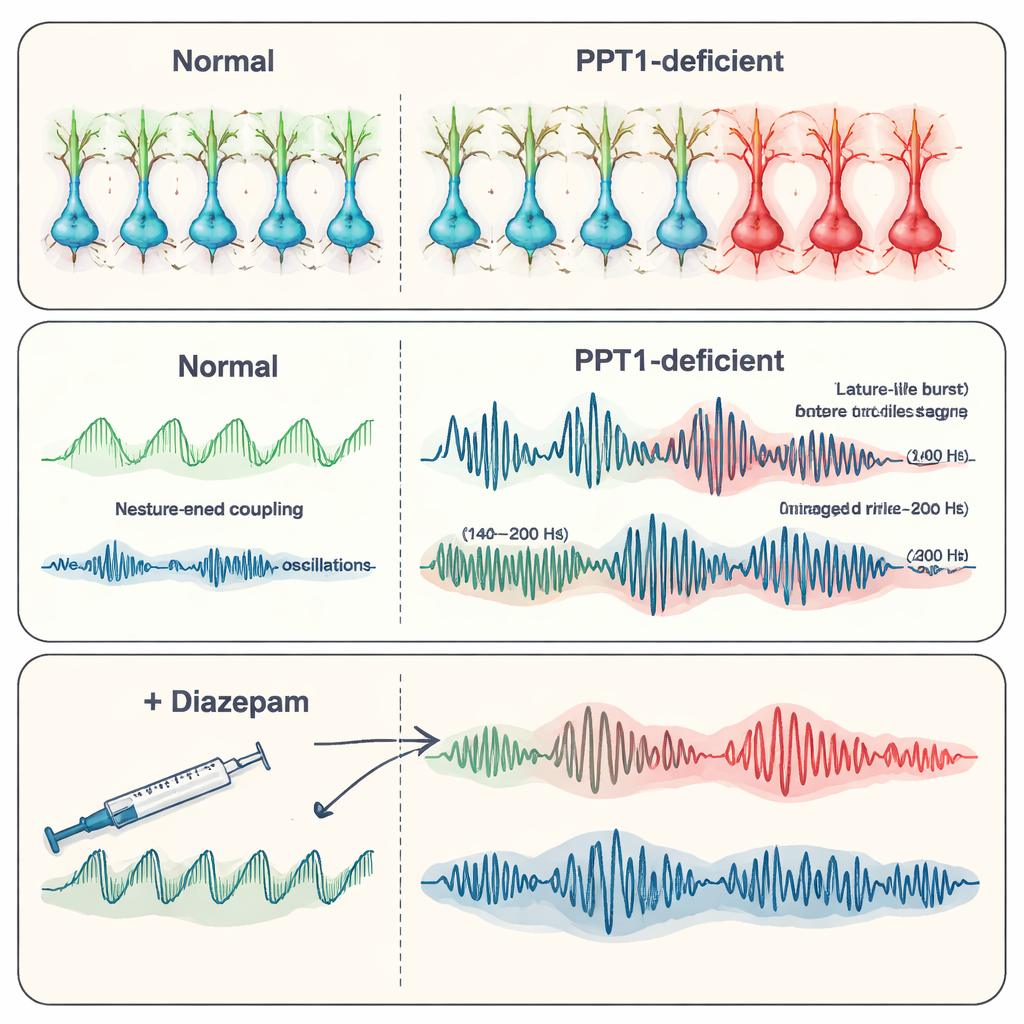
Por qué importan estos hallazgos
Para un lector no especializado, el mensaje clave es que la enfermedad CLN1 no es solo una cuestión de acumulación de desechos en las células cerebrales. La pérdida de PPT1 desencadena una reacción en cadena: primero, interneuronas inhibitorias especializadas se estresan y empiezan a fallar, lo que libera a las neuronas piramidales y distorsiona los ritmos cerebrales. Con el tiempo, este desequilibrio conduce a convulsiones y, finalmente, a una pérdida masiva de neuronas y conexiones. El estudio señala una ventana de oportunidad temprana en la enfermedad, cuando proteger o rescatar a las interneuronas PV+ —quizá bloqueando la activación de caspasas— podría prevenir convulsiones y degeneración posterior. Aunque el diazepam no cura la CLN1, su capacidad para amortiguar los ritmos anormales en este modelo subraya la idea más amplia de que restaurar la inhibición podría ser una estrategia potente en la epilepsia y trastornos cerebrales relacionados.
Cita: Tong, J., Liu, W., Wang, Q. et al. Dysfunction of GABAergic interneurons underlies altered neural network oscillations associated with epileptiform activity in PPT1-deficient mice. Transl Psychiatry 16, 106 (2026). https://doi.org/10.1038/s41398-026-03843-8
Palabras clave: epilepsia, interneuronas, hipocampo, oscilaciones cerebrales, enfermedad por almacenamiento lisosomal