Clear Sky Science · es
Cambios funcionales tempranos y GFAP plasmático en familias suecas con mutaciones de la enfermedad de Alzheimer autosómica dominante
Por qué este estudio importa a las familias
La enfermedad de Alzheimer a menudo parece aparecer de forma repentina, pero en realidad los cambios cerebrales dañinos se acumulan silenciosamente durante muchos años. En familias poco frecuentes que portan mutaciones hereditarias (“autosómicas dominantes”) de Alzheimer, los científicos pueden estimar cuándo es probable que aparezcan los síntomas y observar cómo se desarrollan estos cambios tempranos. Este estudio siguió a familias suecas con dichas mutaciones para entender cómo el uso de energía cerebral, las capacidades cognitivas y un marcador sanguíneo de las células de soporte del cerebro (GFAP) cambian mucho antes de que aparezcan los problemas de memoria, y cómo difieren estos cambios según el gen implicado.
Siguiendo el reloj de la enfermedad en familias de alto riesgo
Como las personas con enfermedad de Alzheimer autosómica dominante (ADAD) suelen desarrollar síntomas a una edad relativamente predecible, los investigadores pueden calcular los “años estimados hasta la aparición de síntomas” (EYA), es decir, cuántos años tiene alguien antes o después de sus primeros signos esperados de la enfermedad. El equipo estudió a 45 adultos de familias suecas con mutaciones en los genes APP o PSEN1, así como a familiares sin mutaciones. A lo largo de más de siete años de media, los participantes se sometieron a escáneres cerebrales que miden cuánto azúcar usa el cerebro (FDG PET), a pruebas detalladas de memoria y funciones cognitivas y, para un subconjunto, a análisis de sangre de GFAP, una proteína que se libera cuando las células de soporte cerebral llamadas astrocitos se activan. Este diseño permitió a los científicos ordenar los distintos cambios biológicos a lo largo de una línea temporal compartida de la enfermedad en lugar de comparar a las personas en un único momento.
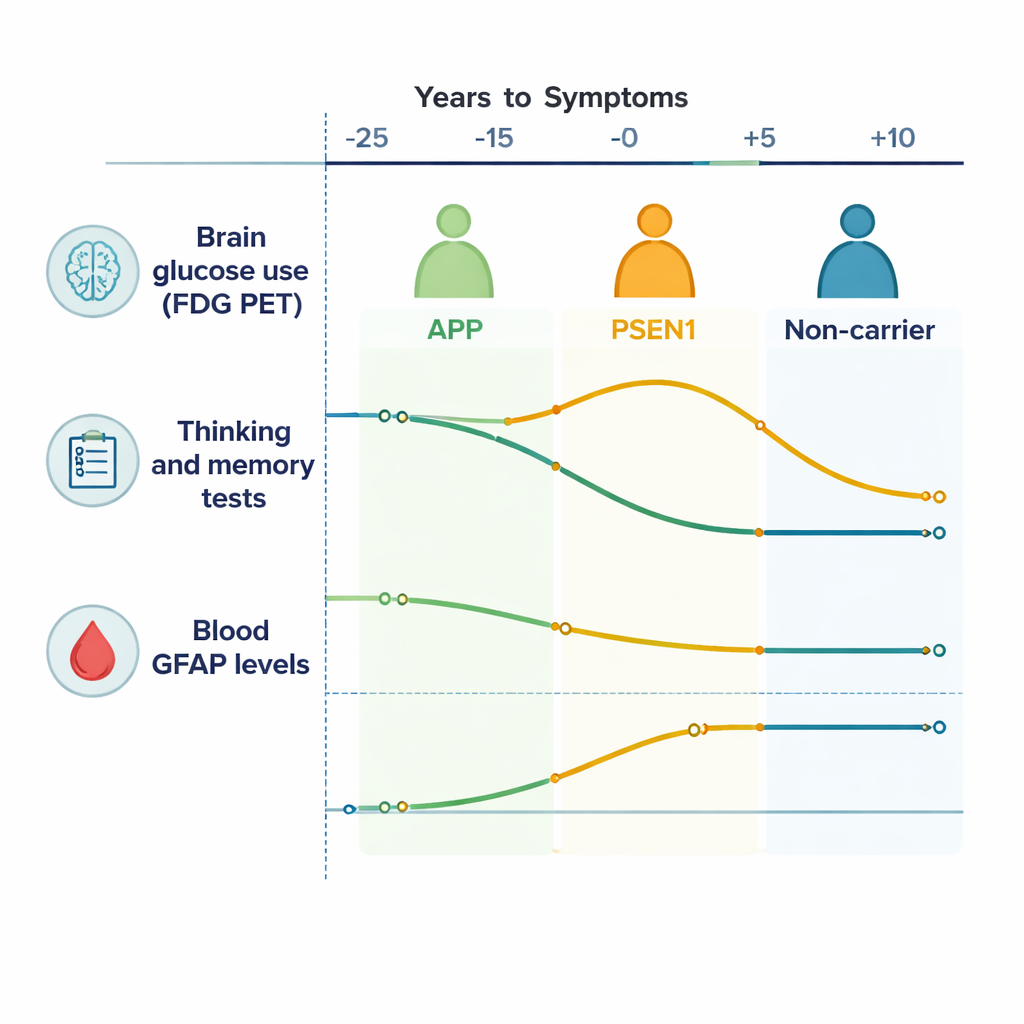
Rastreando la energía cerebral y el pensamiento a lo largo del tiempo
En la superficie cortical del cerebro, las personas con mutaciones de Alzheimer mostraron una disminución gradual en la señal de FDG PET en comparación con los familiares sin mutación, lo que indica que sus cerebros usaban menos glucosa con el tiempo—una señal de fallo de las células cerebrales. Las regiones subcorticales profundas, especialmente el caudado y el tálamo, también mostraron una disminución de la actividad, impulsada sobre todo por quienes portaban mutaciones en APP. Las pruebas de memoria y de funciones cognitivas empeoraron en varios dominios, incluida la memoria episódica y la flexibilidad mental, comenzando aproximadamente entre 10 y 15 años antes de la aparición esperada de los síntomas. En otras palabras, incluso cuando las personas todavía se sentían y funcionaban con normalidad en la vida diaria, pruebas sensibles y escáneres revelaron que sus cerebros ya estaban trabajando de forma más costosa y menos eficiente.
Diferentes patrones según el gen de Alzheimer
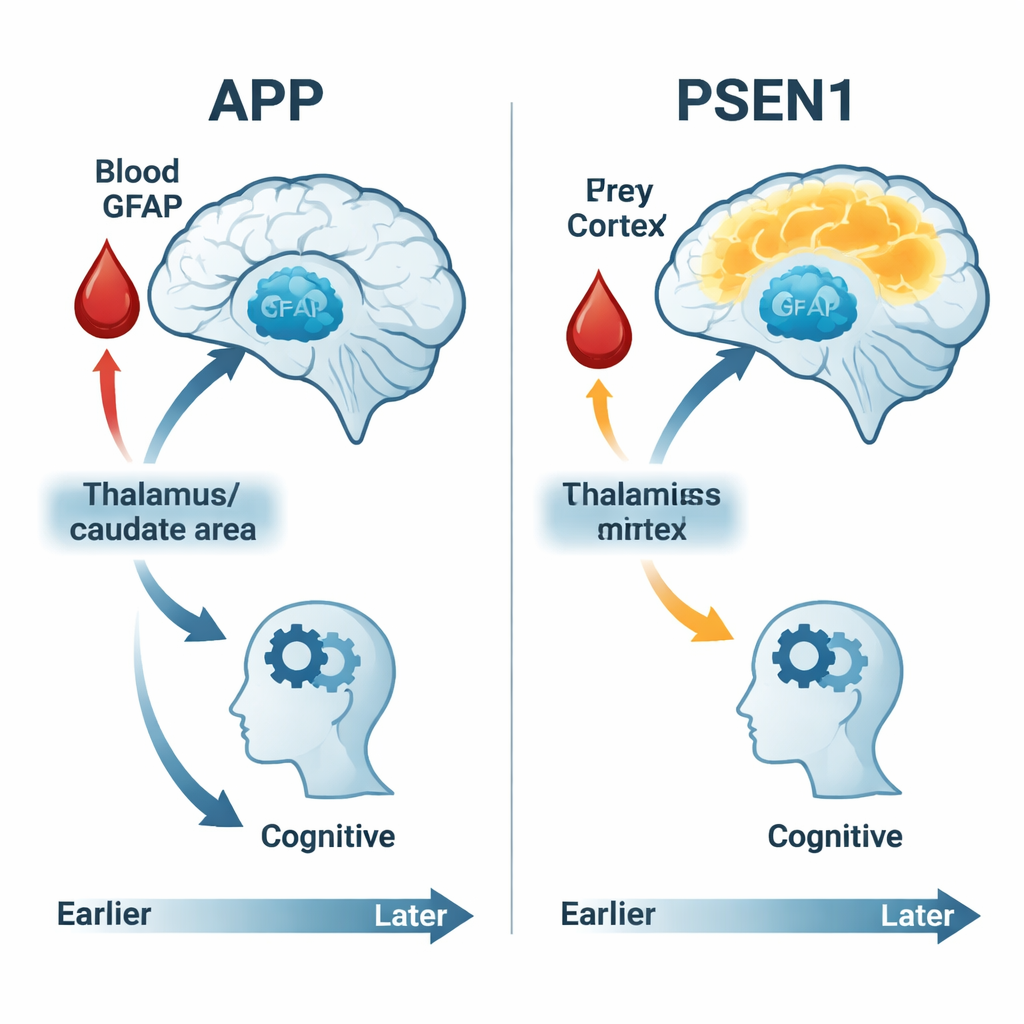
Una idea clave fue que los dos grupos principales de mutación—APP y PSEN1—no siguieron trayectorias idénticas. En los portadores de PSEN1, los investigadores observaron un periodo temprano, de unos 20 a 10 años antes de los síntomas esperados, en el que partes del cerebro mostraron en realidad un uso de glucosa inusualmente alto (“hipermetabolismo”), junto con un mejor rendimiento en las pruebas, antes de declinar más adelante. Esto probablemente refleja una fase temporal de compensación, donde el cerebro y sus células de soporte aumentan la actividad para hacer frente al daño creciente. Los portadores de APP, por el contrario, mostraron una caída más directa y gradual en el metabolismo cerebral sin ese pico temprano. Estos patrones específicos del gen sugieren que la “enfermedad de Alzheimer” no es una sola historia biológica, incluso en sus formas hereditarias, sino una familia de procesos relacionados que se desarrollan de forma distinta según la mutación subyacente.
Qué revela un análisis de sangre sobre el estrés cerebral temprano
GFAP, medido a partir de una muestra de sangre simple, proporcionó una ventana sobre cómo los astrocitos responden a los cambios tempranos del Alzheimer. Los niveles de GFAP tendieron a aumentar de forma sostenida a medida que las personas se acercaban a la edad esperada de aparición de los síntomas tanto en portadores de mutación como en no portadores, pero las relaciones entre GFAP, el metabolismo cerebral y la cognición fueron específicas del gen. En los portadores de APP, niveles más altos de GFAP se asociaron con una caída del uso de glucosa en regiones profundas del cerebro y con un empeoramiento del rendimiento en la mayoría de las pruebas cognitivas, lo que sugiere que la activación de los astrocitos está estrechamente ligada al daño temprano y la pérdida de función. En los portadores de PSEN1, estos vínculos fueron más débiles o ausentes, lo que apunta nuevamente a rutas biológicas diferentes hacia el mismo desenlace clínico de demencia.
Lo que esto significa para la detección temprana y el tratamiento
Para un lector no especialista, el mensaje principal es que en estas familias de alto riesgo los cambios relacionados con el Alzheimer comienzan décadas antes de la pérdida de memoria evidente—y no son iguales para todos. Los escáneres de consumo de glucosa cerebral, las pruebas cognitivas de alta sensibilidad y un marcador sanguíneo como GFAP pueden, en conjunto, revelar cuándo el cerebro empieza a tener dificultades y con qué rapidez progresa esa dificultad. Es importante destacar que las personas con distintas formas genéticas de Alzheimer muestran secuencias de cambio diferentes: algunos presentan una fase temprana de sobreactividad, otros muestran un descenso sostenido, y el marcador sanguíneo del estrés de los astrocitos se asocia con el daño con mayor fuerza en algunos grupos que en otros. Reconocer estas vías distintas puede ayudar a adaptar futuros fármacos y ensayos a las personas adecuadas en el momento oportuno, y respalda la promesa de pruebas sanguíneas como GFAP para detectar el Alzheimer antes—de que los síntomas priven a las personas de su independencia.
Cita: Luckett, E.S., Zapater-Fajari, M., Almkvist, O. et al. Early functional changes and plasma GFAP in Swedish families with Autosomal Dominant Alzheimer’s disease mutations. Transl Psychiatry 16, 67 (2026). https://doi.org/10.1038/s41398-026-03829-6
Palabras clave: enfermedad de Alzheimer autosómica dominante, biomarcador sanguíneo GFAP, metabolismo cerebral de la glucosa, astrocitos y neurodegeneración, detección temprana del Alzheimer