Clear Sky Science · es
Convergencia y divergencia de genes informadas por variantes comunes y raras del trastorno del espectro autista en vías y redes genéticas específicas de tejido
Por qué importa el rompecabezas genético del autismo
Familias y clínicos saben desde hace tiempo que el trastorno del espectro autista (TEA) es muy variable: algunas personas requieren apoyo de por vida, mientras que otras viven de forma independiente pero tienen dificultades sociales. Gran parte de esta diversidad parece proceder de la genética, aunque el riesgo está repartido entre miles de cambios en el ADN, cada uno inclinando el cerebro y el cuerpo de maneras sutiles. Este estudio plantea una pregunta simple pero importante: ¿cómo interactúan en distintos tejidos las mutaciones raras y potentes con las muchas variantes comunes y débiles para configurar el autismo, y qué implicaciones tiene eso para comprender y tratar la condición?
Dos tipos de pistas genéticas
Los investigadores distinguen entre variantes raras, que pueden alterar fuertemente un gen pero se hallan en relativamente pocas personas, y variantes comunes, que son frecuentes en la población pero suelen tener efectos pequeños. Las variantes raras han sido más fáciles de conectar con el autismo en familias concretas, pero solo explican una pequeña fracción del riesgo genético global. Las variantes comunes, consideradas en conjunto, representan mucho más del componente hereditario del autismo, aunque el efecto de cada una es diminuto y fácil de pasar por alto. Los autores de este trabajo se propusieron integrar señales tanto raras como comunes para averiguar si convergen en los mismos sistemas biológicos o apuntan a diferentes partes del cuerpo y mecanismos de enfermedad distintos.
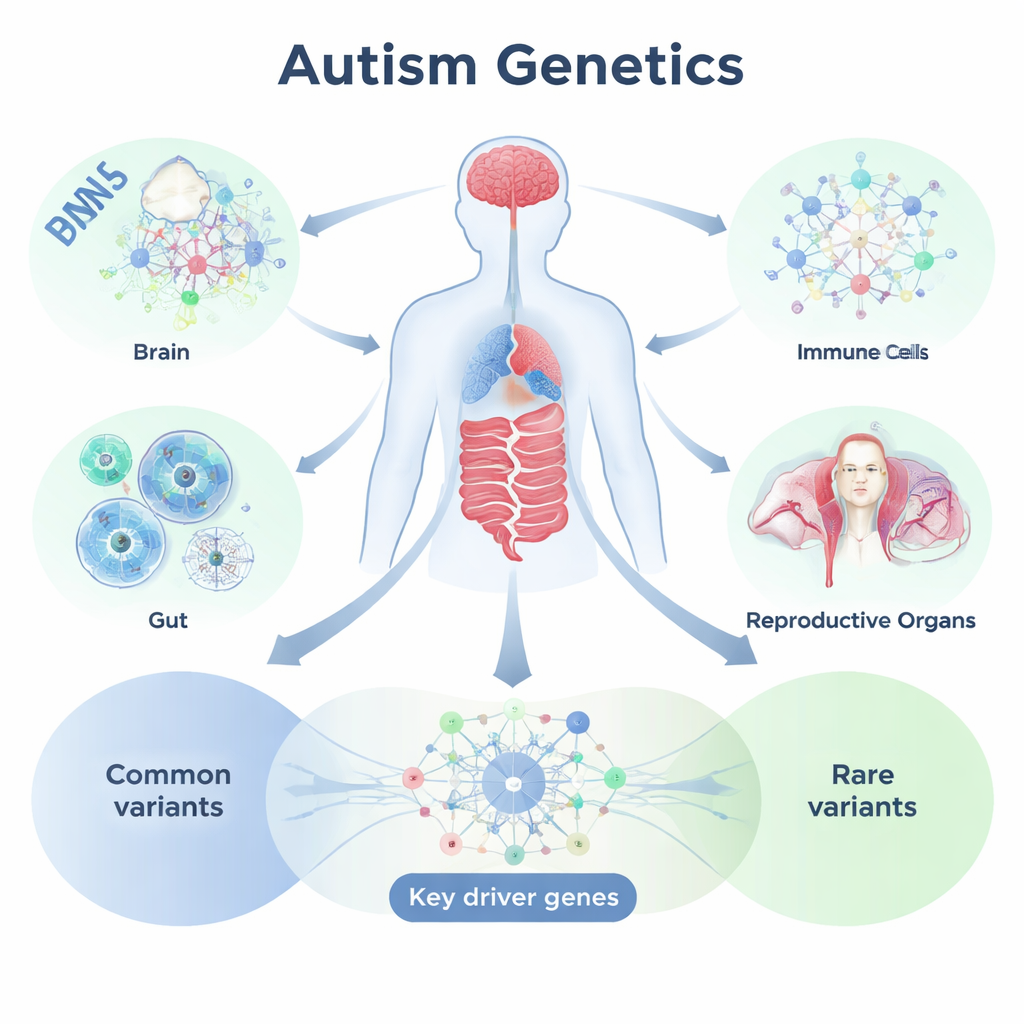
Mapear las señales del ADN en tejidos y redes
Para abordar esto, el equipo empleó un marco de análisis llamado Mergeomics, que combina estudios genéticos a gran escala con información sobre cómo se activan los genes en tejidos específicos. Partieron de datos de asociación a nivel genómico sobre más de nueve millones de variantes comunes del ADN procedentes de más de 18.000 personas con autismo y unos 28.000 controles sin autismo. A continuación, asignaron esas variantes a genes usando datos de referencia detallados sobre la actividad génica en casi 50 tejidos, incluidas muchas regiones cerebrales, así como órganos periféricos digestivos, inmunitarios, reproductivos y otros. Agrupando genes que se encienden conjuntamente en el mismo tejido y examinando hasta qué punto esos grupos se alinean con variantes asociadas al autismo, los investigadores identificaron “módulos” específicos por tejido y redes regulatorias que parecen ser importantes para el TEA.
Tanto el cerebro como el cuerpo contribuyen
El análisis confirmó un papel central del cerebro, especialmente regiones como la corteza cingulada anterior, la amígdala, la corteza frontal, el cerebelo y áreas corticales más amplias, que están implicadas en la emoción, el comportamiento social, el pensamiento y la coordinación. Las redes génicas en estas regiones cerebrales estaban enriquecidas tanto en variantes comunes como raras relacionadas con el autismo y se asociaban con señalización sináptica, neurodesarrollo y control inmunológico dentro del cerebro. Sin embargo, la imagen no se limitó al cráneo. De manera sorprendente, muchos tejidos periféricos, particularmente del sistema digestivo, inmunitario, endocrino y reproductivo, también contenían módulos génicos fuertemente informados por variantes comunes vinculadas al autismo. Esos módulos se relacionaban con procesos como respuestas inmunitarias, crecimiento y división celular, producción de energía, empalme del ARNm y una vía de control importante conocida como mTOR, todos implicados en el desarrollo cerebral y el comportamiento.
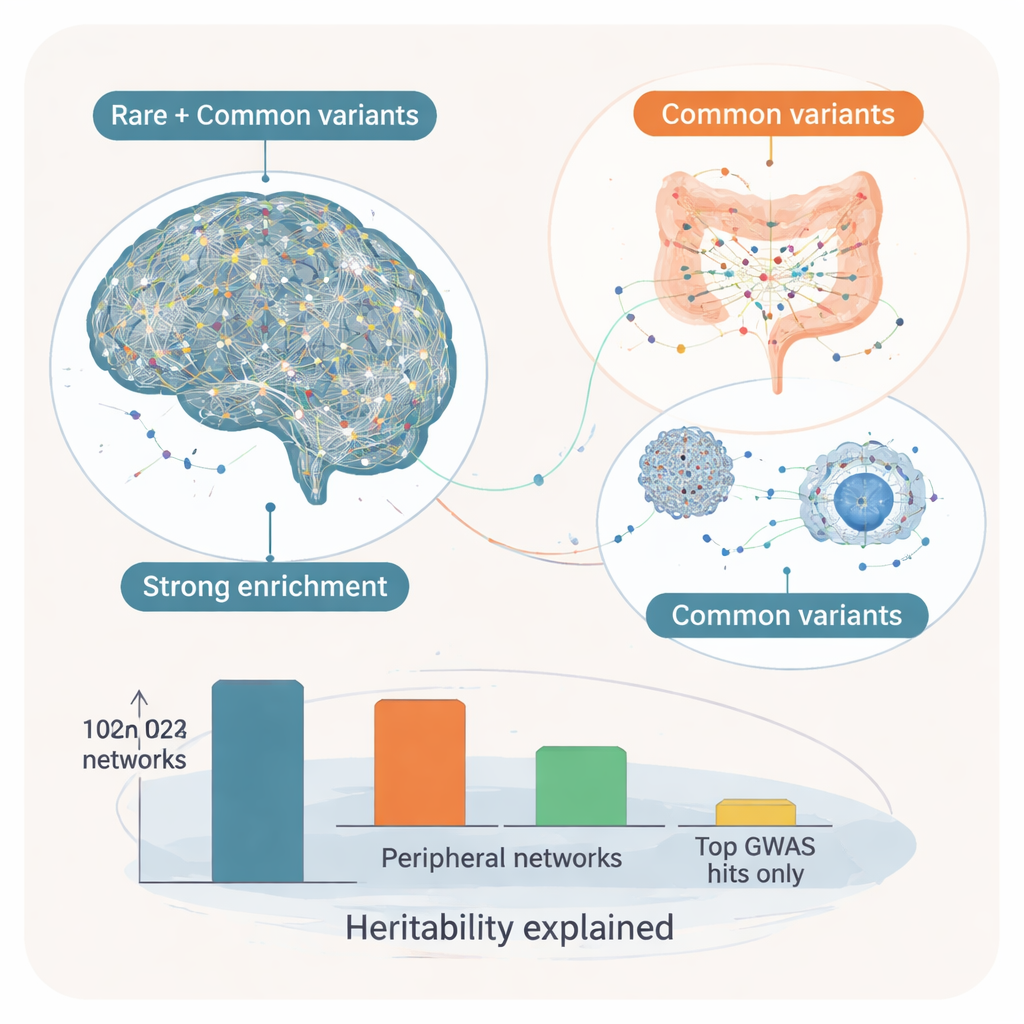
Genes clave y la idea núcleo‑modificador
Al situar estos módulos en redes regulatorias génicas direccionales, los investigadores preguntaron a continuación qué genes ocupan los nodos centrales —los llamados “conductores clave” que influyen en muchos otros genes. En las redes cerebrales, estos conductores clave mostraron un fuerte enriquecimiento tanto de variantes raras de gran impacto como de variantes comunes, lo que sugiere que forman un conjunto “núcleo” de genes donde convergen ambos tipos de riesgo. Ejemplos incluyen SYT1, que ayuda a controlar la liberación de neurotransmisores en las sinapsis, y ADD2, implicado en la configuración de la estructura y conectividad neuronal. Sus redes circundantes contenían una mezcla de genes de autismo raros conocidos y dianas de variantes comunes implicadas en la comunicación sináptica y la excitabilidad neuronal. En contraste, los conductores clave en tejidos periféricos, sobre todo en órganos digestivos y endocrinos, estaban más influidos por variantes comunes por sí solas. Estos actúan como “modificadores”, ajustando vías inmunitarias, metabólicas y de señalización que pueden moldear cómo las vulnerabilidades cerebrales centrales se traducen en síntomas.
Qué significa esto para las personas y el tratamiento futuro
Cuando los autores estimaron cuánto del riesgo hereditario del autismo podía atribuirse a estas redes, los módulos cerebrales explicaron alrededor del 7% del componente hereditario y los módulos periféricos otro 3%, capturando conjuntamente casi toda la heredabilidad atribuible a variantes comunes observada en el estudio original —y mucho más que la pequeña fracción explicada solo por los pocos impactos únicos más fuertes del ADN. Para un público no especializado, la conclusión es que la genética del autismo sigue un patrón en capas: variantes raras y comunes convergen en un conjunto central de redes centradas en el cerebro que son cruciales para el neurodesarrollo, mientras que las variantes comunes extendidas en tejidos intestinales, inmunitarios y hormonales probablemente modifiquen el curso y las características de la condición. Este marco núcleo‑modificador ayuda a explicar por qué el autismo se ve tan distinto entre unas personas y otras y sugiere que las terapias futuras podrían necesitar abordar no solo el cerebro, sino también los sistemas corporales más amplios que interactúan con él.
Cita: Gill, C., Zuo, Y., Ha, D.Sm. et al. Convergence and divergence of genes informed by common and rare variants of autism spectrum disorders in tissue-specific pathways and gene networks. Transl Psychiatry 16, 98 (2026). https://doi.org/10.1038/s41398-026-03824-x
Palabras clave: genética del autismo, variantes raras, variantes comunes, redes cerebrales, eje intestino‑cerebro