Clear Sky Science · es
Estimulación asociativa pareada con un componente cortical de alta intensidad y un componente periférico de alta frecuencia en el tratamiento del dolor neuropático tras lesión medular incompleta – un ensayo piloto
Por qué importa el dolor nervioso crónico tras una lesión medular
Para muchas personas con lesión de la médula espinal, el daño no termina con debilidad o entumecimiento. Más de la mitad desarrolla dolor ardiente, hormigueo o sensaciones tipo descarga eléctrica en brazos o piernas que pueden persistir durante años y resistir los analgésicos habituales. Este estudio examinó si una prometedora técnica de estimulación cerebro–nervio, llamada estimulación asociativa pareada, podría aliviar el dolor neuropático difícil en las manos y los brazos de personas con lesiones medulares no traumáticas de larga evolución.
Una nueva manera de influir en el sistema nervioso
En lugar de depender de fármacos, la estimulación asociativa pareada intenta reentrenar suavemente las vías nerviosas estimulándolas desde dos direcciones a la vez. Una bobina magnética situada sobre el cuero cabelludo administra pulsos fuertes pero breves a la zona del cerebro que controla la mano, mientras que pequeñas pulsaciones eléctricas se aplican a los nervios de la muñeca y el antebrazo. Cuando se sincronizan con precisión, estas señales están diseñadas para encontrarse en la médula espinal, animando a las neuronas a fortalecer conexiones útiles. Estudios previos, mayormente no controlados, sugerían que este método podría no solo mejorar el movimiento de la mano tras una lesión medular, sino también reducir el dolor neuropático leve a moderado como un efecto secundario beneficioso. 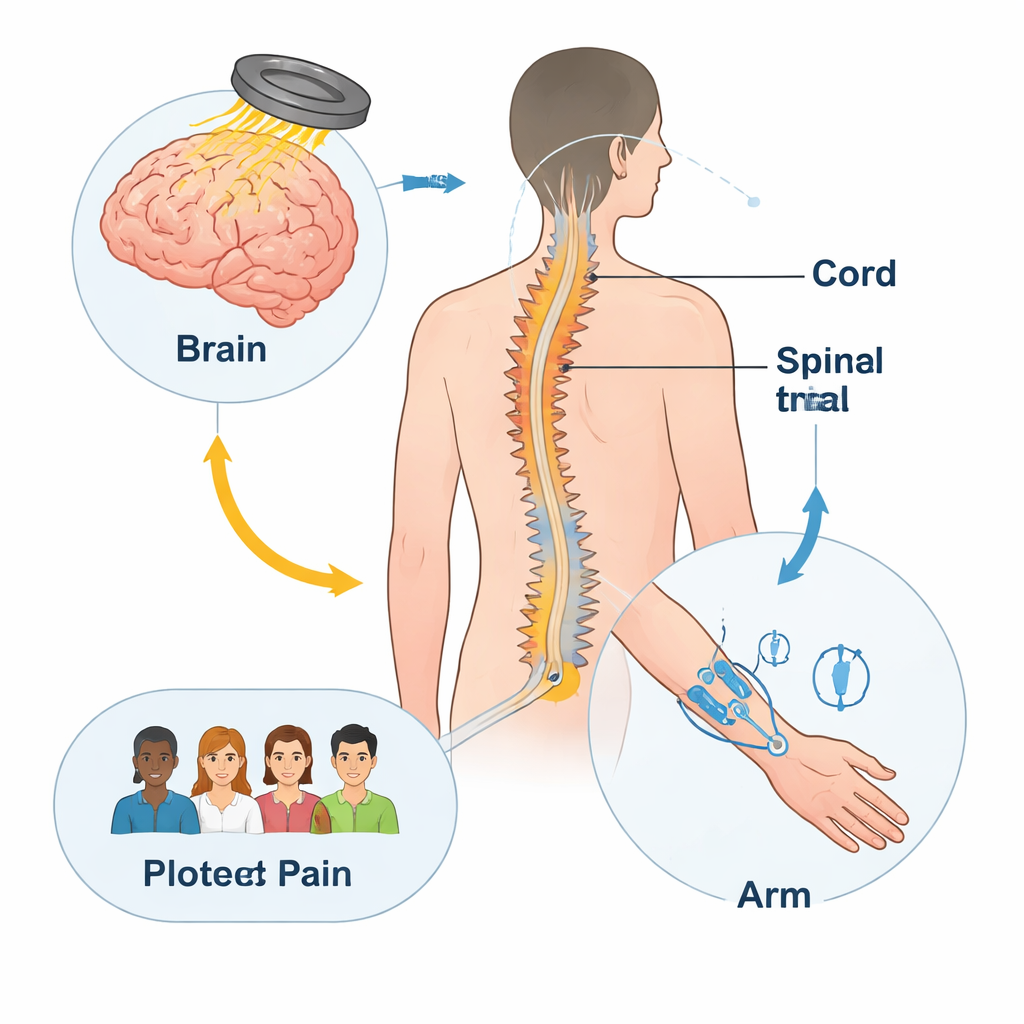
Evaluando el tratamiento de forma rigurosa
Los investigadores llevaron a cabo un ensayo piloto pequeño pero cuidadosamente controlado en cinco adultos con lesiones medulares incompletas en la región cervical y dolor neuropático unilateral en una mano o brazo, de moderado a severo y de larga duración. Cada persona pasó por dos periodos separados de cuatro semanas: uno con la estimulación pareada completa y otro con una versión simulada (similar a un placebo), en orden aleatorio. En el tratamiento real, pulsos magnéticos de alta intensidad activaban el área de la mano en el cerebro mientras trenes rápidos de pulsos eléctricos se dirigían a tres nervios principales de la mano más dolorosa. En la condición simulada, el equipo presentaba apariencia y sonidos similares, pero el campo magnético que llegaba al cerebro estaba bloqueado y los electrodos cutáneos se desplazaban alejándolos de los nervios y se ajustaban a una intensidad apenas perceptible sin activar los músculos.
Cómo se midieron el dolor y la función
Durante ambos periodos de tratamiento y en el seguimiento, los pacientes puntuaron el dolor medio en la mano tratada en una escala verbal de 0–10 cada semana y cumplimentaron un cuestionario detallado que registraba tanto la intensidad del dolor como cuánto interfería en actividades diarias como el sueño, el estado de ánimo y el trabajo. El equipo también midió la fuerza de la mano, la destreza, la fuerza de agarre y pinza, la espasticidad y la independencia en tareas cotidianas. Para sondear cómo el sistema nervioso procesaba la temperatura y la vibración en la zona dolorosa, usaron pruebas sensoriales cuantitativas que determinan los umbrales a los que el frío o el calor se vuelven incómodos o dolorosos. Todas las evaluaciones las realizaron clínicos que desconocían si el paciente había recibido estimulación real o simulada.
Qué mostraron (y no mostraron) los resultados
Las puntuaciones de dolor fluctuaron ligeramente con el tiempo en ambas condiciones, pero los cambios se mantuvieron dentro de aproximadamente tres puntos en la escala de 0–10 y variaron entre personas. En promedio, el dolor descendió alrededor de un punto (aproximadamente una reducción del 20–30 %) tras tanto la estimulación real como la simulada, pero esto no alcanzó el umbral que generalmente se considera una mejora claramente significativa, y no hubo una ventaja consistente para el tratamiento real. Las medidas de cuánto el dolor afectaba la vida diaria, los niveles de ansiedad relacionada con el dolor, la fuerza de la mano, las habilidades motoras finas y la calidad de vida general también mostraron cambios pequeños y similares entre ambas condiciones. Las pruebas sensoriales sugirieron cierta normalización de los umbrales de dolor por frío en la mano tratada tras sesiones reales y simuladas, nuevamente sin una diferencia clara entre ellas. Es importante subrayar que los pacientes toleraron bien la estimulación, incluso con dolor severo, y no se observaron efectos adversos graves. 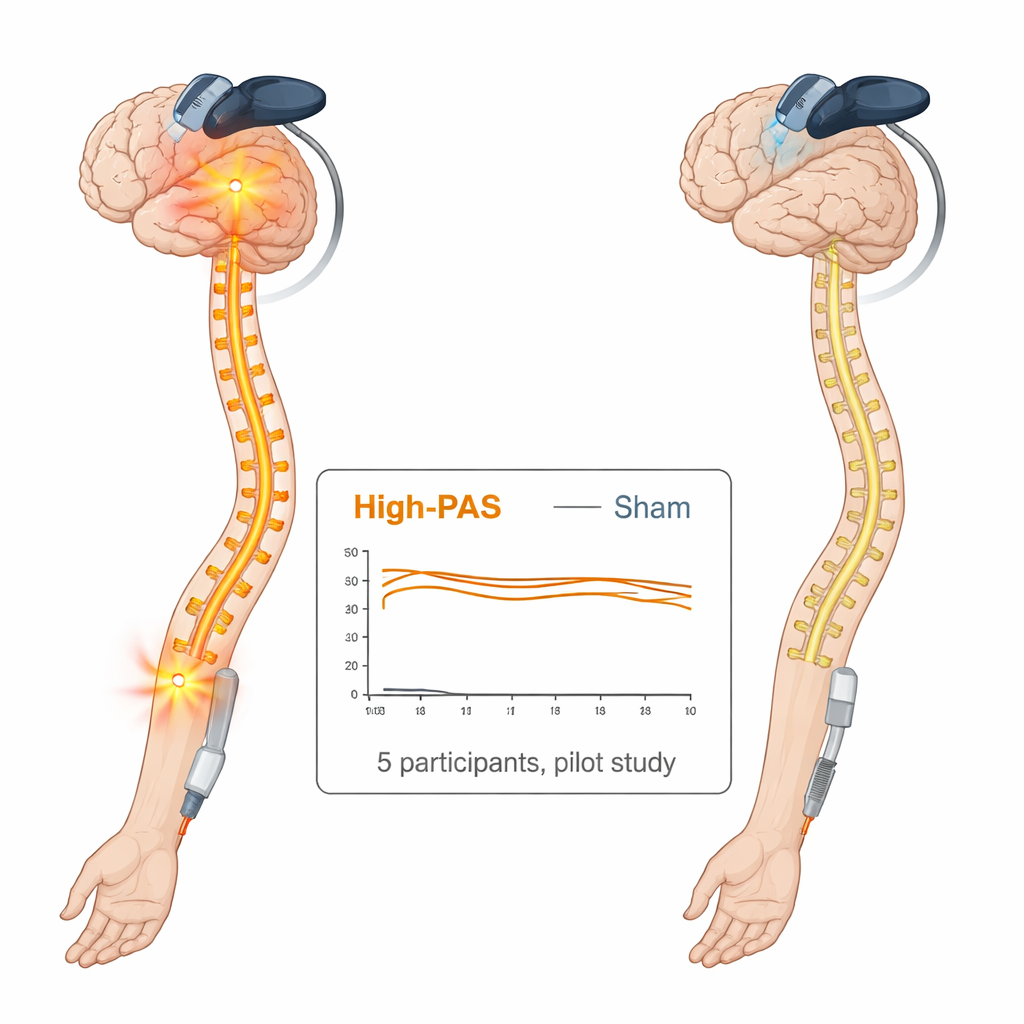
Qué significa esto para las personas que viven con dolor
En términos simples, este estudio piloto cuidadosamente ciego encontró que la forma específica de estimulación asociativa pareada evaluada aquí no proporcionó un alivio claramente superior al de un tratamiento similar a placebo para el dolor neuropático severo en el brazo tras una lesión medular incompleta. Sin embargo, la técnica no empeoró el dolor y pareció segura, lo que sugiere que la presencia de dolor no debería excluir automáticamente su uso cuando el objetivo principal es mejorar el movimiento. Los autores señalan que informes positivos previos podrían deberse a dolor de menor intensidad, mecanismos del dolor distintos, mejoras en la actividad muscular o efectos placebo. Proponen que estudios futuros examinen el método en grupos más amplios y, de manera crucial, reorienten la estimulación hacia vías sensoriales más que motoras para ver si dirigirse directamente a los circuitos cerebrales y medulares implicados en el procesamiento del dolor puede producir un alivio clínicamente más relevante.
Cita: Holopainen, K., Pohjonen, M., Kirveskari, E. et al. Paired associative stimulation with a high-intensity cortical component and a high-frequency peripheral component in treatment of neuropathic pain after incomplete spinal cord injury – a pilot trial. Spinal Cord Ser Cases 12, 3 (2026). https://doi.org/10.1038/s41394-026-00729-1
Palabras clave: lesión medular, dolor neuropático, estimulación cerebral, rehabilitación, estimulación asociativa pareada