Clear Sky Science · es
Supresión de la producción de energía mitocondrial por un péptido cupredoxina bacteriano fotosintético inhibe el crecimiento tumoral
Convertir bacterias en combatientes contra el cáncer
Las células cancerosas tienen gran apetito energético. Dependen de pequeñas «centrales» internas llamadas mitocondrias para generar la energía que necesitan para crecer, diseminarse y resistir los tratamientos. Este estudio explora un aliado inesperado en la lucha contra el cáncer: un fragmento corto de una proteína originalmente hallada en bacterias fotosintéticas. Los investigadores muestran que este péptido diseñado puede infiltrarse en células tumorales, cortar su suministro de energía en la fuente y mejorar considerablemente la eficacia de la radioterapia—mientras en gran medida respeta a las células normales.
Un péptido diminuto con una gran misión
El equipo partió de un hallazgo anterior de que una proteína bacteriana llamada azurina puede frenar el crecimiento tumoral actuando sobre el famoso supresor tumoral p53. A continuación buscaron bacterias que viven dentro y alrededor de tumores humanos, centrándose en microbios fotosintéticos que usan la luz para generar energía. Estas bacterias portan una familia relacionada de proteínas llamadas cupredoxinas. Al comparar sus estructuras e historia evolutiva, los investigadores se centraron en una cupredoxina, auracianina B, y recortaron una región corta de 28 aminoácidos a la que llamaron aurB. Este fragmento es soluble en agua, puede cruzar membranas celulares y tiene una conformación que sugería que podría interactuar con maquinaria clave de producción de energía dentro de las células.
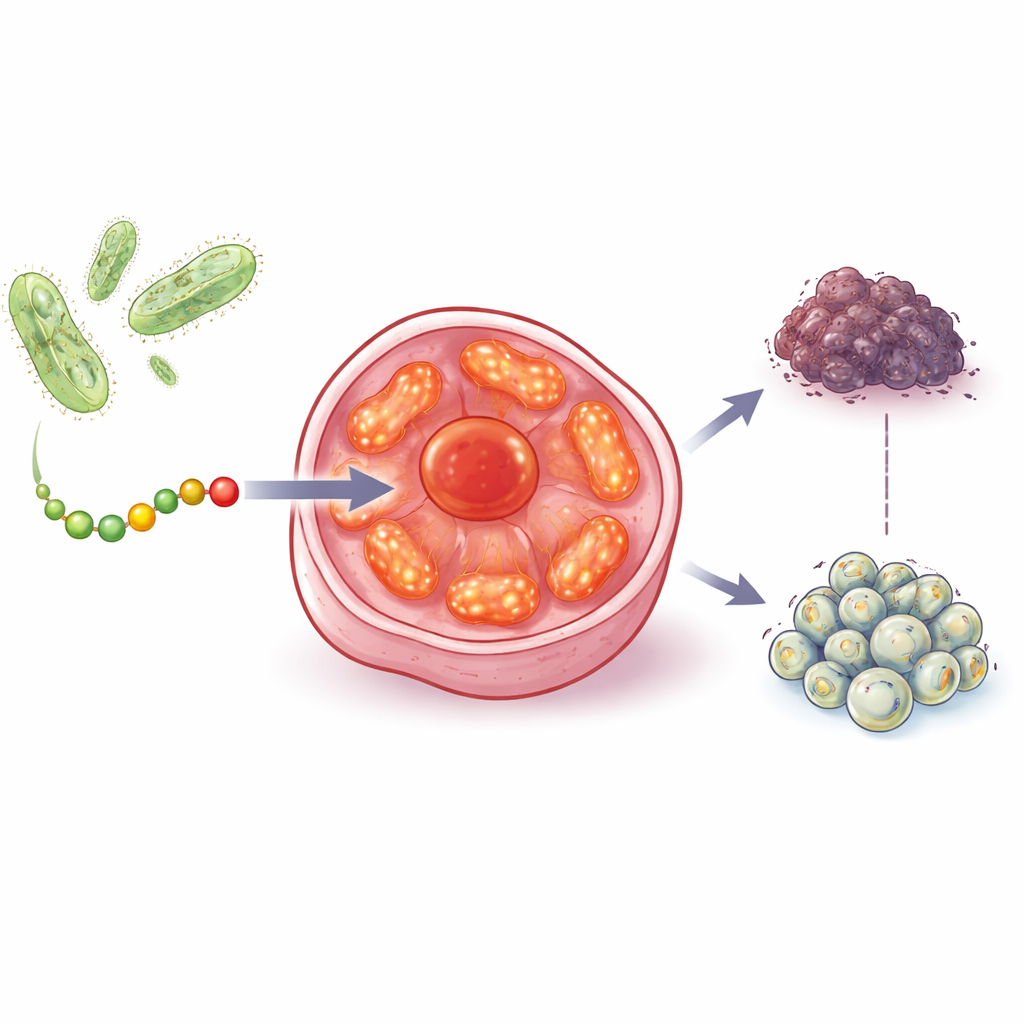
Encontrar y atacar las centrales energéticas del cáncer
En pruebas de laboratorio, aurB redujo la supervivencia de líneas celulares de cáncer de mama, próstata, colon y ovario, incluso cuando esas células carecían de p53 funcional o de receptores hormonales que requieren muchos fármacos actuales. De forma importante, aurB tuvo efectos mucho más débiles sobre células normales de próstata, corazón y músculo, pese a que esas células sanas son ricas en mitocondrias. Experimentos de imagen mostraron que aurB entraba preferentemente en células cancerosas y luego se concentraba dentro de sus mitocondrias. La microscopía electrónica, usando aurB unido a pequeñas barras de oro como marca visual, confirmó que el péptido realmente se acumulaba dentro de estos orgánulos.
Cortar el suministro de energía
Una vez dentro de las mitocondrias, aurB se unió a un componente específico de la ATP sintasa—la turbina molecular que fabrica ATP, la principal moneda energética de la célula. Experimentos bioquímicos de “pull-down” y espectrometría de masas identificaron a este socio como ATP5C, parte del núcleo central de la enzima. Mediciones por resonancia de plasmón superficial mostraron que aurB se adhiere a ATP5C con afinidad moderada y liberación lenta, consistente con una interacción estable. Ensayos funcionales revelaron entonces el efecto de esta unión: aurB redujo drásticamente los niveles mitocondriales de ATP en células de cáncer de próstata, disminuyó la tasa a la que consumían oxígeno y bloqueó tanto la respiración como la vía glucolítica de respaldo. Al colapsar la producción de energía, las células tumorales mostraron señales de muerte celular programada impulsada por la caspasa-3, una enzima ejecutora clave.
Bloquear tumores y potenciar la radiación
Los investigadores probaron después aurB en modelos murinos de cáncer de próstata agresivo. En animales portadores de tumores humanos de próstata bajo la piel, inyecciones regulares de aurB redujeron el crecimiento tumoral en aproximadamente dos tercios, comparable o superior al fármaco quimioterápico paclitaxel, pero sin pérdida de peso ni angustia aparente. Las muestras tumorales de los ratones tratados contenían menos células en división y muchas más células en muerte. En un segundo modelo que imita la metástasis ósea—un lugar común y letal de diseminación del cáncer de próstata—aurB por sí solo ralentizó la expansión tumoral en el hueso de la pierna y redujo el número de metástasis pulmonares. Sin embargo, cuando se combinó con una dosis moderada de radiación, el efecto fue espectacular: los tumores en la extremidad tratada quedaron casi eliminados y las metástasis pulmonares disminuyeron en más del 90 por ciento en comparación con los controles.
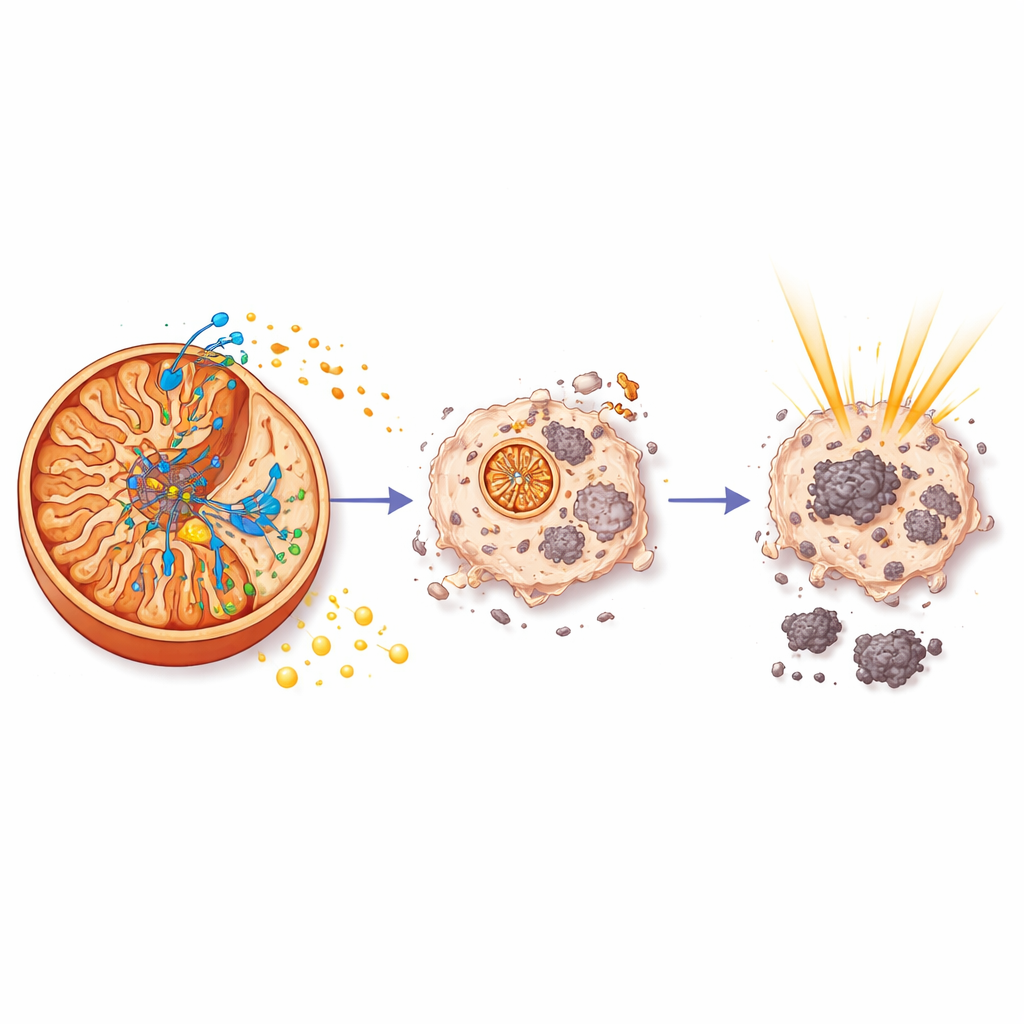
Por qué la energía importa para la radiación
Para entender por qué aurB mejora la radiación, el equipo examinó la actividad génica en tumores de ratones tratados. Encontraron que aurB, pero no la radiación sola, atenuaba una red de genes controlada por HIF-1, un regulador maestro que ayuda a las células cancerosas a adaptarse a la baja disponibilidad de oxígeno y alimenta la resistencia al tratamiento. Bajo las condiciones de escasez energética creadas por aurB, vías clave de crecimiento y supervivencia impulsadas por PI3K y c-Myc se vieron reducidas, y la maquinaria glucolítica que permite a los tumores prosperar en entornos adversos también fue suprimida. En esencia, al sabotear la producción de ATP directamente en la turbina mitocondrial, aurB empujó a las células tumorales a una crisis energética que las dejó mucho más vulnerables al daño por radiación.
Una nueva clase de bloqueadores energéticos de precisión
Este trabajo introduce una nueva estrategia para la terapia del cáncer: diseñar péptidos pequeños inspirados en bacterias que se dirigen a sistemas energéticos mitocondriales alterados en tumores. AurB, derivado de una proteína bacteriana fotosintética, se dirige selectivamente a un componente de la ATP sintasa que suele estar sobreactivado en cánceres como el de próstata, mama, ovario y cerebro. Al privar directamente a las células cancerosas de energía y debilitar sus defensas, especialmente frente a la radiación, tales péptidos podrían complementar los tratamientos existentes y ofrecer opciones donde los enfoques inmunológicos fracasan. Aunque queda mucho trabajo antes de que este concepto llegue a la clínica, el estudio demuestra que proteínas energéticas bacterianas ancestrales pueden reutilizarse como herramientas antitumorales modernas y altamente específicas.
Cita: Naffouje, S.A., Tran, D.B., Rademacher, D.J. et al. Suppression of mitochondrial energy production by a photosynthetic bacterial cupredoxin peptide inhibits tumor growth. Sig Transduct Target Ther 11, 124 (2026). https://doi.org/10.1038/s41392-026-02703-7
Palabras clave: sintasa de ATP mitocondrial, metabolismo del cáncer, péptidos terapéuticos, cáncer de próstata, sensibilización a la radiación